I. Berdasarkan nomor kelompok fungsional
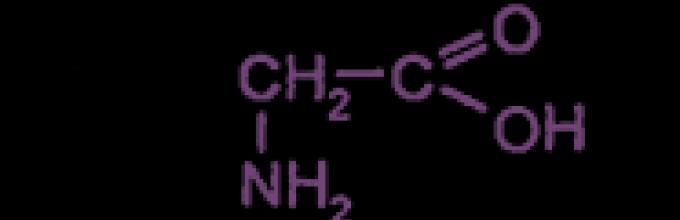
Monoaminomono asam karboksilat
perwakilan paling sederhana:

Asam monoaminodikarboksilat

Misalnya:

Asam diaminomonokarboksilat

Misalnya:

II. Menurut posisi relatif gugus karboksil dan amino
-α-asam amino

- asam β-amino

- asam γ-amino

Rumus dan nama beberapa asam α-amino yang residunya merupakan bagian dari protein

Protein adalah polimer alami yang makromolekulnya dibuat jumlah besar residu dari 20 asam α-amino yang berbeda. Dalam biokimia, nama pendek dan sepele serta sebutan tiga huruf biasanya digunakan untuk asam amino.
Asam monoaminomonokarboksilat
|
Asam aminoetanoat atau aminoasetat atau glisin (glikokol) |
|
|
Asam 2-aminopropanoat atau α-aminopropionat atau alanin |
|
|
2-amino-3-hidroksipropanoat, atau asam α-amino-β-hidroksipropionat, atau serin |
|
|
Asam 2-amino-3-mercaptopropanoic, atau β-mercaptoalanine, atau sistein |
|
|
Asam 2-amino-3-fenilpropanoat, atau β-fenilalanin, atau fenilalanin |
|
|
2-amino-3-(4-hidroksifenil)-asam propanoat, atau β-(n-hidroksifenil)-apanin, atau tirosin |
|
|
Asam 2-amino-3-metilbutanoat, atau asam α-aminoisovalerat, atau valin |
Asam monoaminodikarboksilat
Asam diaminomonokarboksilat
Klasifikasi asam amino alami
I. Asam amino tergantikan - dapat disintesis dalam tubuh manusia. Ini termasuk yang di atas: glisin, alanin, serin, sistein, tirosin, asam aspartat dan glutamat.
II. Asam amino esensial tidak dapat disintesis dalam tubuh manusia dan harus disuplai ke tubuh sebagai bagian dari protein makanan. Fenilalanin, valin, lisin bukanlah perwakilan asam amino nonesensial.
Properti fisik
Kebanyakan asam amino tidak berwarna zat kristal, sangat larut dalam air. Banyak asam amino yang memiliki rasa manis. Titik leleh berbagai asam amino berkisar antara 230-300°C.
Sifat kimia
Asam amino merupakan senyawa amfoter, hal ini disebabkan adanya gugus fungsi yang bersifat asam (-COOH) dan basa (-NH 2) dalam molekulnya.
1. Interaksi dengan basa

2. Interaksi dengan asam

3. Pembentukan garam internal (ion bipolar)
Dalam larutan air, asam amino terdapat dalam bentuk campuran kesetimbangan molekul dan ion bipolar, yang dalam lingkungan asam berubah menjadi bentuk kationik, dan dalam lingkungan basa menjadi bentuk anionik.
a) Asam monoaminomonokarboksilat

Ketika garam internal asam monoaminomonokarboksilat terbentuk, sifat medium tidak berubah. Oleh karena itu, asam amino ini disebut netral. Muatan total garam internal asam tersebut adalah nol.
Ketika asam (H+) ditambahkan, ion karboksilat terprotonasi dan hanya menyisakan muatan positif pada gugus -NH
b) Asam monoaminodikarboksilat

Oleh karena itu, ketika garam internal asam monoaminodikarboksilat terbentuk, ion hidrogen berlebih akan terbentuk larutan berair asam ini mempunyai pH
c) Asam diaminomonokarboksilat

Ketika garam internal asam diaminomonokarboksilat terbentuk, ion hidroksida berlebih terbentuk, sehingga larutan berairnya memiliki pH > 7. Asam amino semacam itu disebut basa. Muatan total garam internal asam amino basa adalah positif.
4. Pembentukan peptida
Ketika gugus karboksil dari satu molekul asam amino berinteraksi dengan gugus amino dari molekul asam amino lain, dipeptida terbentuk:

Ketika dua asam amino berbeda berinteraksi, campuran empat dipeptida terbentuk; Misalnya:

Dipeptida dapat menambahkan molekul asam amino lain untuk membentuk tripeptida. Demikian pula, tetrapeptida dapat diperoleh dari tripeptida, dll.
5. Pembentukan turunan pada gugus karboksil
Seperti asam karboksilat, asam amino dapat membentuk ester, asam klorida, dll. Misalnya:

6. Polikondensasi asam ε-aminokaproat

Metode memperoleh
1. Amonolisis asam α-halokarboksilat
2. Hidrolisis protein
Asam amino mengandung gugus amino dan karboksil dan menunjukkan semua sifat karakteristik senyawa dengan gugus fungsi tersebut. Saat menulis reaksi asam amino, rumus dengan gugus amino dan karboksi tidak terionisasi digunakan.
1) reaksi pada gugus amino. Gugus amino dalam asam amino menunjukkan sifat-sifat amina yang umum: amina adalah basa dan bertindak sebagai nukleofil dalam reaksi.
1. Reaksi asam amino sebagai basa. Ketika asam amino berinteraksi dengan asam, garam amonium terbentuk:
glisin hidroklorida, garam glisin hidroklorida
2. Aksi asam nitrat. Ketika asam nitrat bekerja, asam hidroksi terbentuk dan nitrogen serta air dilepaskan:
Reaksi ini digunakan untuk penentuan kuantitatif gugus amina bebas dalam asam amino, serta protein.
3. Pembentukan turunan N - asil, reaksi asilasi.
Asam amino bereaksi dengan anhidrida dan asam halida, membentuk turunan N - asil dari asam amino:
Garam natrium benzil eter N karbobenzoksiglisin - glisin kloroformik
Asilasi adalah salah satu cara untuk melindungi gugus amino. Turunan N-asil memiliki sangat penting dalam sintesis peptida, karena turunan N-asil mudah dihidrolisis untuk membentuk gugus amino bebas.
4. Pembentukan basis Schiff. Ketika asam a-amino berinteraksi dengan aldehida, imina tersubstitusi (basa Schiff) terbentuk melalui tahap pembentukan karbinolamin:
alanin formaldehida N-metilol turunan dari alanin
5. Reaksi alkilasi. Gugus amino dalam asam a-amino dialkilasi membentuk turunan N-alkil:
Nilai tertinggi bereaksi dengan 2,4 - dinitrofluorobenzene. Turunan dinitrofenil yang dihasilkan (turunan DNP) digunakan dalam pembentukan rangkaian asam amino peptida dan protein. Interaksi asam a-amino dengan 2,4-dinitrofluorobenzena merupakan contoh reaksi substitusi nukleofilik pada cincin benzena. Karena adanya dua gugus penarik elektron yang kuat pada cincin benzena, halogen menjadi bergerak dan mengalami reaksi substitusi:
 |
2.4 – dinitro -
fluorobenzena N - 2,4 - dinitrofenil - a - asam amino
(DNPB) DNP - turunan dari a - asam amino
6.Reaksi dengan fenil isothiocyanate. Reaksi ini banyak digunakan dalam menentukan struktur peptida. Fenil isothiocyanate merupakan turunan dari asam isothiocyanic H-N=C=S. Interaksi asam a-amino dengan fenil isotiosianat berlangsung melalui mekanisme reaksi adisi nukleofilik. Produk yang dihasilkan kemudian mengalami reaksi substitusi intramolekul, yang mengarah pada pembentukan Amida tersubstitusi siklik: feniltiohidantoin.
Senyawa siklik diperoleh dalam hasil kuantitatif dan merupakan turunan fenil dari tiohidantoin (turunan PTH) - asam amino. Turunan PTG berbeda dalam struktur radikal R.
Selain garam biasa, asam a-amino dapat membentuk, dalam kondisi tertentu, garam intrakompleks dengan kation logam berat. Semua asam a-amino dicirikan oleh garam tembaga intrakompleks (kelat) yang mengkristal dengan indah dan berwarna sangat biru):
Alanin etil ester
Pembentukan ester merupakan salah satu cara untuk melindungi gugus karboksil dalam sintesis peptida.
3. Pembentukan asam halida. Ketika bekerja pada asam a-amino dengan gugus amino yang dilindungi dengan sulfur oksidiklorida (tionil klorida) atau fosfor oksida triklorida (fosfor oksiklorida), asam klorida terbentuk:
Produksi asam halida merupakan salah satu cara untuk mengaktifkan gugus karboksil dalam sintesis peptida.
4.Memperoleh anhidrida asam amino a. Asam halida memiliki kadar yang sangat tinggi reaktivitas, yang mengurangi selektivitas reaksi saat menggunakannya. Oleh karena itu, metode yang lebih umum digunakan untuk mengaktifkan gugus karboksil dalam sintesis peptida adalah dengan mengubahnya menjadi gugus anhidrida. Anhidrida kurang aktif dibandingkan asam halida. Ketika asam a-amino yang memiliki gugus amino terlindungi berinteraksi dengan asam etil kloroformat (etil kloroformat), ikatan anhidrida terbentuk:
5. Dekarboksilasi. a - Asam amino yang memiliki dua gugus penarik elektron pada atom karbon yang sama mudah mengalami dekarboksilasi. Dalam kondisi laboratorium, hal ini dilakukan dengan memanaskan asam amino dengan barium hidroksida.Reaksi ini terjadi di dalam tubuh dengan partisipasi enzim dekarboksilase dengan pembentukan amina biogenik:
ninhidrin
Hubungan asam amino dengan panas. Ketika asam a-amino dipanaskan, Amida siklik yang disebut diketopiperazin terbentuk:

Diketopiperazine
g - dan d - Asam amino dengan mudah memisahkan air dan bersiklisasi untuk membentuk Amida internal, laktam:
g - laktam (butirolaktam)
Dalam kasus di mana gugus amino dan karboksil dipisahkan oleh lima atau lebih atom karbon, ketika dipanaskan, terjadi polikondensasi dengan pembentukan rantai polimer poliamida dengan eliminasi molekul air.
Asam amino bersifat organik senyawa amfoter. Mereka mengandung dua gugus fungsi yang sifatnya berlawanan dalam molekul: gugus amino dengan sifat basa dan gugus karboksil dengan sifat asam. Asam amino bereaksi dengan asam dan basa:
H 2 N -CH 2 -COOH + HCl → Cl [H 3 N-CH 2 -COOH],
H 2 N -CH 2 -COOH + NaOH → H 2 N-CH 2 -COONa + H 2 O.
Ketika asam amino dilarutkan dalam air, gugus karboksil menghilangkan ion hidrogen, yang dapat menempel pada gugus amino. Dalam hal ini, garam internal terbentuk, yang molekulnya merupakan ion bipolar:
H 2 N-CH 2 -COOH + H 3 N -CH 2 -COO - .
Transformasi asam basa asam amino dalam berbagai lingkungan dapat digambarkan dengan diagram umum berikut:

Larutan asam amino dalam air memiliki lingkungan netral, basa atau asam tergantung pada jumlah gugus fungsi. Jadi, asam glutamat membentuk larutan asam (dua gugus -COOH, satu -NH 2), lisin membentuk larutan basa (satu gugus -COOH, dua -NH 2).
Menyukai amina primer, asam amino bereaksi dengan asam nitrat, dan gugus amino diubah menjadi gugus hidrokso, dan asam amino menjadi asam hidroksi:
H 2 N-CH(R)-COOH + HNO 2 → HO-CH(R)-COOH + N 2 + H 2 O
Mengukur volume nitrogen yang dilepaskan memungkinkan kita menentukan jumlah asam amino ( Metode Van Slyke).
Asam amino dapat bereaksi dengan alkohol dengan adanya gas hidrogen klorida, berubah menjadi ester(lebih tepatnya, ke dalam garam hidroklorida eter):
H 2 N-CH(R)-COOH + R’OH H 2 N-CH(R)-COOR’ + H 2 O.
Ester asam amino tidak memiliki struktur bipolar dan merupakan senyawa yang mudah menguap.
Sifat paling penting dari asam amino adalah kemampuannya untuk berkondensasi membentuk peptida.
Reaksi kualitatif.
1) Semua asam amino dioksidasi oleh ninhidrin

dengan terbentuknya produk berwarna biru-ungu. Prolin asam imino memberi warna kuning dengan ninhidrin. Reaksi ini dapat digunakan untuk mengukur asam amino dengan spektrofotometri.
2) Saat memanaskan asam amino aromatik dengan pekat asam sendawa terjadi nitrasi cincin benzena dan terbentuk senyawa yang berwarna kuning. Reaksi ini disebut xanthoprotein(dari bahasa Yunani xanthos - kuning).
Yang berkinerja penting fungsi biologis dalam organisme hidup, berpartisipasi dalam biosintesis protein, bertanggung jawab atas aktivitas normal sistem saraf dan mengatur proses metabolisme. Asam aminoasetat, yang diturunkan secara artifisial, digunakan dalam bidang farmasi, obat-obatan dan Industri makanan.
Bahan tambahan makanan E640 menggabungkan asam aminoasetat (glisin) dengan nomor label yang sama dan garam natriumnya - senyawa yang digunakan untuk mengoptimalkan rasa dan aroma produk. Suplemen ini aman dan disetujui secara resmi di sebagian besar negara di dunia.
Glisin dan garam natriumnya: informasi umum
Glisin, juga dikenal sebagai asam aminoasetat atau aminoetanoat, termasuk dalam sejumlah asam amino non-esensial - struktur organik paling sederhana yang merupakan bagian dari protein dan senyawanya. Bahan yang diperoleh secara artifisial berupa bubuk tidak berwarna, tidak berbau dan mempunyai rasa manis.
Pada skala industri, glisin diproduksi dengan menggabungkan asam kloroasetat dan amonia. Asam aminoasetat, pada gilirannya, memiliki sifat membentuk garam kompleks (glisinat) dengan ion logam.
Natrium glisinat adalah garam natrium dan asam aminoasetat, yang juga merupakan zat asal sintetis. Meskipun glisin dan garamnya merupakan senyawa kimia yang berbeda, dalam industri makanan keduanya memiliki fungsi yang sama sebagai pengubah rasa dan aroma, digabungkan dalam satu nomor label dan dianggap sebagai aditif E640.
| Nama | Glisin |
|---|---|
| Sinonim | Asam aminoasetat (aminoetanoat), glikokol (usang) |
| Kelompok | Asam amino nonesensial |
| Rumus kimia | NH 2 – CH 2 – COOH |
| Struktur | Kristal monoklinik halus (bubuk kristal) |
| Warna | Putih (tidak berwarna) |
| Bau | Absen |
| Mencicipi | Manis |
| Kelarutan | Larut sempurna dalam, larut sebagian dalam. Tidak larut dalam eter |
| Kode aditif | E640 (termasuk garam natrium) |
| Asal | Sintetis |
| Toksisitas | Aman bila dikonsumsi dalam batas normal |
| Area penggunaan | Industri makanan, farmasi, kedokteran, tata rias |
Peran biologis glisin dan sumbernya
Glisin lebih sering ditemukan dalam molekul protein daripada asam amino lainnya dan melakukan fungsi biologis yang penting. Dalam tubuh manusia, asam amino ini disintesis melalui transaminasi (transfer reversibel gugus amino) glioksilat atau pembelahan enzimatik kolin dan serin.
Namun, asam aminoasetat adalah prekursor porfirin dan purin, yang biosintesisnya terjadi pada sel hidup peran biologis Koneksi ini tidak terbatas pada fungsi-fungsi ini. Glisin juga merupakan neurotransmitter yang terlibat dalam transmisi impuls saraf, mengatur produksi asam amino lain dan memiliki efek “penghambatan” pada neuron dan neuron motorik.
Tubuh orang sehat secara mandiri mensintesis asam amino dalam jumlah yang dibutuhkan, sehingga penggunaannya dalam obat-obatan dan suplemen makanan biasanya tidak diperlukan. Makanan sumber asam aminoasetat antara lain produk hewani (hati sapi), kacang-kacangan dan beberapa buah-buahan.
Pengaruh glisin dan garam natriumnya pada tubuh manusia
Asam aminoasetat sebagai neurotransmitter melakukan fungsi pengaturan dan terutama mempengaruhi sistem saraf pusat dan perifer. Glisin memiliki sifat nootropik, menormalkan metabolisme, mengaktifkan fungsi pelindung sistem saraf pusat dan memiliki efek menenangkan ringan.
Efek positif glisin pada tubuh manusia:
- pengurangan ketegangan emosional, kecemasan, stres, agresivitas;
- peningkatan mood dan normalisasi tidur;
- relaksasi otot dan meredakan kram;
- peningkatan kinerja;
- pelemahan efek samping mengonsumsi obat-obatan psikotropika;
- mengurangi keparahan gangguan vegetatif-vaskular;
- mengurangi keinginan untuk alkohol dan permen.
Sebagai bagian dari suplemen E640, glisin dan garamnya tidak memiliki sifat di atas dan tidak memiliki efek positif maupun negatif pada tubuh manusia bila dikonsumsi dalam batas normal. Bahan tambahan makanan tidak menimbulkan ancaman bagi kesehatan, tetapi jika terjadi intoleransi individu dapat memicu reaksi alergi.
Potensi bahaya dapat berasal dari pengotor pada bahan tambahan dan produk makanan berkualitas rendah, yang dalam pembuatannya digunakan pengoptimal rasa dan aroma.
Penerapan glisin dan garam natriumnya
Penerapan glisin dan natrium glisinat terutama terbatas pada industri makanan, obat-obatan dan obat-obatan. Namun, asam aminoasetat juga digunakan dalam industri kosmetik karena efek hipoalergenisitas dan antioksidannya.
Kosmetik yang mengandung aditif E640:
- sampo obat untuk rambut lemah dan produk anti kebotakan;
- kosmetik anti penuaan, krim pelembab dan masker untuk semua jenis kulit;
- serum pembersih dan toner;
- lipstik dan balsem.
Tablet glisin yang dihancurkan dapat digunakan untuk membuat produk perawatan kulit buatan sendiri dan ditambahkan ke masker dan krim pelembab. Asam aminoasetat mendorong penetrasi komponen nutrisi yang berharga ke lapisan dalam dermis dan meningkatkan efek kosmetik obat.
Aditif E640 dalam industri makanan
 Glisin dan natrium glisinat secara aktif digunakan dalam proses teknologi produksi minuman beralkohol. Aditif E640, khususnya, termasuk dalam vodka elit, yang membantu menetralkan bau tidak sedap dan melembutkan rasa keras. Ada juga yang berpendapat bahwa keberadaan glisin dalam minuman beralkohol membantu mengurangi efek toksik alkohol pada sistem saraf dan mencegah mabuk.
Glisin dan natrium glisinat secara aktif digunakan dalam proses teknologi produksi minuman beralkohol. Aditif E640, khususnya, termasuk dalam vodka elit, yang membantu menetralkan bau tidak sedap dan melembutkan rasa keras. Ada juga yang berpendapat bahwa keberadaan glisin dalam minuman beralkohol membantu mengurangi efek toksik alkohol pada sistem saraf dan mencegah mabuk.
Produk makanan yang mengandung aditif E640:
- minuman beralkohol kuat;
- selai, manisan, jeli, ;
- jus kemasan dengan ampas;
- masakan yang diperkaya;
- minuman yang diperkaya olahraga;
- saus, bumbu dan rempah-rempah.
Asam aminoasetat digunakan tidak hanya untuk mengoptimalkan rasa dan transportasi biologis zat aktif, tetapi juga sebagai agen antibakteri. Secara khusus, digunakan untuk mengolah daging, ikan, dan makanan laut untuk menetralisir E. coli yang berbahaya.
Penggunaan medis
Glisin secara aktif digunakan untuk pengobatan dan pencegahan penyakit yang berhubungan dengan pusat dan perifer sistem saraf. Zat ini merupakan bagian dari sediaan farmasi dengan efek nootropik, sedatif, antikonvulsan dan hipnotis, serta memiliki efek antidepresan ringan dan obat penenang.
Indikasi medis penggunaan asam aminoasetat sebagai obat:
- penurunan kinerja mental, gangguan tidur dan ingatan;
- ketegangan emosional, situasi stres, neurosis;
- ketidakstabilan emosi dan peningkatan rangsangan;
- konsekuensi dari stroke iskemik, cedera otak traumatis dan infeksi saraf;
- distonia vegetatif-vaskular, iskemia;
- peningkatan tonus otot, kram otot;
- kecanduan alkohol dan obat-obatan, efek toksik obat-obatan yang menekan sistem saraf pusat.
Terbukti konsumsi 3 g glisin per hari memberikan efek positif terhadap kemampuan mental dan keadaan emosi seseorang secara umum, menghilangkan rasa kantuk di siang hari dan menormalkan tidur malam. Obat ini juga diresepkan untuk ibu hamil untuk mengurangi kecemasan, anak-anak dan remaja yang mengalami kesulitan dalam adaptasi sosial dan konsentrasi.
Aditif E640 dan undang-undang
Pengoptimal rasa dan bau E640 digunakan dalam produksi makanan di sebagian besar negara di dunia, tetapi tidak ada informasi tentang bahan tambahan tersebut dalam Codex Alimentarius. Belum ada kasus keracunan glisin dan natrium glisinat bila dikonsumsi sebagai makanan, sehingga pengubah E640 dinilai aman.
Aditif ini termasuk dalam daftar produk yang disetujui secara resmi untuk digunakan dalam industri makanan di Uni Eropa, Amerika Serikat dan Kanada. Perundang-undangan Federasi Rusia dan Belarus juga mengizinkan keberadaan E640 dalam produk dalam standar yang diizinkan yang ditetapkan oleh SanPiN. Tidak ada data tentang penggunaan E640 sebagai penambah rasa dan bahan penyedap di Ukraina.
Terlepas dari kenyataan bahwa glisin dan garamnya tidak memiliki efek toksik pada tubuh manusia dan disetujui untuk digunakan, produk yang mengandung E640 hampir tidak dapat disebut bermanfaat. Kebanyakan perasa dan wewangian digunakan untuk menarik perhatian pembeli terhadap produk berkualitas rendah, yang penggunaannya harus diminimalkan.
Glisin (asam aminoasetat, glikokol, Gly, G)
H2NCH2COOH
Massa molekul 75,07; kristal tidak berwarna; tidak meleleh 232-236°C (dengan dekomposisi); sangat larut dalam air, tidak larut dalam sebagian besar pelarut organik. Pada 25°C hal Ka 2,34 (COOH) dan 9,6 (NH 2); R SAYA 5,97.
Dilihat dari sifat kimianya, glisin adalah asam α-amino alifatik yang khas. Penentuan kuantitatif didasarkan pada pembentukan produk berwarna dengan o-phthalaldehyde (reaksi Zimmermann). Ini lebih sering ditemukan dalam protein dibandingkan asam amino lainnya. Berfungsi sebagai prekursor dalam biosintesis senyawa porfirin dan basa purin. Glisin adalah asam amino berkode, non-esensial; biosintesisnya dilakukan melalui transaminasi asam glioksilat, pembelahan enzimatik serin dan treonin. Lisin disintesis dari asam kloroasetat dan NH 3 . Pada spektrum NMR pada D 2 O, pergeseran kimia proton gugus CH 2 adalah 3,55 ppm. Garam bagian dalam glisin (CH 3) 3 + NCH 2 COO disebut betaine.
Glisin digunakan untuk sintesis peptida sebagai komponen solusi penyangga, dicampur dengan asam amino lain - untuk nutrisi parenteral.