И историски информации.
1) М.В. Ломоносов, спроведувајќи хармонично расудување и едноставни експерименти, дошол до заклучок дека „причината за топлината лежи во внатрешното движење на честичките од врзаната материја... Познато е дека топлината се возбудува со движење: рацете се загреваат од взаемно триење, дрвото се запали, искри излетуваат кога силикон удира во челик, железото се загрева кога неговите честички се коваат со силни удари.
2) Б. Рамфорд, работејќи во фабрика за производство на топови, забележал дека при дупчење топовска цевка станува многу жешко. На пример, тој стави метален цилиндар тежок околу 50 кг во кутија со вода и, бушејќи во цилиндерот со дупчалка, ја доведе водата во кутијата да зоврие за 2,5 часа.
3) Дејви извршил интересен експеримент во 1799 година. Две парчиња мраз, кога се тријат едно со друго, почнале да се топат и да се претвораат во вода.
4) Лекарот на бродот Роберт Мајер во 1840 година, додека пловел кон островот Јава, забележал дека по бура водата во морето е секогаш потопла отколку пред неа.
Пресметка на работа.
Во механиката, работата се дефинира како производ на модулите на сила и поместување: A=FS. Кога се разгледуваат термодинамичките процеси механичко движењемакротелата како целина не се разгледуваат. Концептот на работа овде е поврзан со промена на волуменот на телото, т.е. движење на делови од макротело релативно едни на други. Овој процес доведува до промена на растојанието помеѓу честичките, а исто така често и до промена на брзината на нивното движење, според тоа, до промена на внатрешната енергија на телото.
Нека има гас во цилиндар со подвижен клип на температура Т 1 (сл.). Полека ќе го загреваме гасот на температура Т 2. Гасот ќе се прошири изобарично и клипот ќе се помести од положбата 1 да се позиционира 2 на растојание Δ л. Силата на притисокот на гасот ќе работи на надворешните тела. Бидејќи стр= const, потоа силата на притисокот Ф = pSисто така константна. Затоа, работата на оваа сила може да се пресмета со помош на формулата А=Ф Δ л=pS Δ л=стр Δ В, A= стр Δ В
каде Δ В- промена на волуменот на гасот. Ако волуменот на гасот не се промени (изохоричниот процес), тогаш работата што ја врши гасот е нула.
Зошто се менува внатрешната енергија на телото кога се собира или се шири? Зошто гасот се загрева кога се компресира и се лади кога се шири?
Причината за промената на температурата на гасот за време на компресија и проширување е следната: при еластични судири на молекулите со клипот што се движи, нивната кинетичка енергија се менува.
- Ако гасот е компресиран, тогаш за време на судир клипот што се движи кон него пренесува дел од својата механичка енергија на молекулите, како резултат на што гасот се загрева;
- Ако гасот се прошири, тогаш по судир со клипот што се повлекува, брзината на молекулите се намалува. Како резултат на тоа, гасот се лади.
Со компресија и проширување, се менува и просекот потенцијална енергијаинтеракција на молекулите, бидејќи тоа го менува просечното растојание помеѓу молекулите.
Работа на надворешни сили кои делуваат на гас
- Кога гасот е компресиран, когаΔ V= V 2 – V 1 < 0 , A>0, насоките на сила и поместување се совпаѓаат;
- При проширување, когаΔ V= V 2 – V 1 > 0, А<0, направления силы и перемещения противоположны.
Да ја напишеме равенката Клапејрон-Менделев за две гасни состојби:
pV 1 = m/M*RT 1 ; pV 2 =m/M* RT 2 ⇒
стр(В 2 − В 1 )= m/M*Р(Т 2 − Т 1 ).
Затоа, во изобаричен процес
А= m/M*РΔ Т.
Ако м = М(1 мол идеален гас), потоа на Δ Τ = 1 K добиваме Р = А. Од ова произлегува физичко значење на универзалната гасна константа: бројно е еднаква на работата што ја врши 1 мол идеален гас кога се загрева изобарно за 1 К.
Геометриска интерпретација на делото:
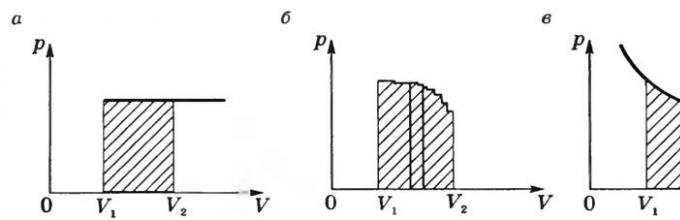
На графиконот p = f(V) за изобарен процес, работата е еднаква на плоштината на засенчениот правоаголник на слика а).
Ако процесот не е изобаричен (сл. б), тогаш кривата стр = ѓ(В) може да се претстави како прекината линија која се состои од голем број изохори и изобари. Работата на изохоричните делови е нула, а вкупната работа на сите изобарични делови ќе биде еднаква на површината на засенчената фигура. Во изотермичен процес ( Т= const) работата е еднаква на површината на засенчената фигура прикажана на слика в.

>>Физика: Работа во термодинамика
Како резултат на кои процеси може да се промени внатрешната енергија? Веќе знаете дека постојат два вида на такви процеси: работа и пренос на топлина. Да почнеме со работа. На што е еднакво при компресија и ширење на гас и други тела?
Работа во механика и термодинамика.ВО механикаработата се дефинира како производ на модулот на силата, модулот на поместување на точката на неговата примена и косинус на аголот меѓу нив. Кога на тело во движење дејствува сила, работата е еднаква на промената на неговата кинетичка енергија.
ВО движењето на телото како целина не се разгледува, зборуваме за движење на делови од макроскопско тело релативно едни на други. Како резултат на тоа, волуменот на телото може да се промени, но неговата брзина останува еднаква на нула. Работата во термодинамиката е дефинирана на ист начин како и во механиката, но таа е еднаква не на промената на кинетичката енергија на телото, туку на промената на неговата внатрешна енергија.
Промена на внатрешната енергија при вршење на работа.Зошто се менува внатрешната енергија на телото кога телото се собира или се шири? Зошто, особено, воздухот се загрева при надувување на гума на велосипед?
Причината за промената на температурата на гасот за време на неговата компресија е како што следува: при еластични судири на молекулите на гасот со клипот што се движи, нивната кинетичка енергија се менува. Значи, кога се движи кон молекулите на гасот, клипот им пренесува дел од својата механичка енергија за време на судири, како резултат на што гасот се загрева. Клипот делува како фудбалер да се сретне со влезна топка со удар. Стапалото и дава брзина на топката што е значително поголема од онаа што ја поседувала пред ударот.
Спротивно на тоа, ако гасот се прошири, тогаш по судир со клипот што се повлекува, брзините на молекулите се намалуваат, како резултат на што гасот се лади. Фудбалерот постапува на ист начин, за да ја намали брзината на летечката топка или да ја запре - ногата на фудбалерот се оддалечува од топката, како да ѝ отстапува.
Кога ќе дојде до компресија или проширување, се менува и просечната потенцијална енергија на интеракција помеѓу молекулите, бидејќи просечното растојание помеѓу молекулите исто така се менува.
Пресметка на работа.Ајде да ја пресметаме работата во зависност од промената на волуменот користејќи го примерот на гас во цилиндар под клипот ( Сл.13.1).
Најлесен начин е прво да не се пресмета работата на силата што дејствува на гасот од надворешното тело (клипот), туку работата што ја врши силата на притисокот на гасот што дејствува на клипот со сила од . Според третиот закон на Њутн  . Модулот на сила што дејствува од гасот на клипот е еднаков на
. Модулот на сила што дејствува од гасот на клипот е еднаков на ![]() , Каде стр- притисок на гасот и С- површината на клипот. Нека гасот се прошири изобарично и клипот се помести во насока на силата за мало растојание
, Каде стр- притисок на гасот и С- површината на клипот. Нека гасот се прошири изобарично и клипот се помести во насока на силата за мало растојание ![]() . Бидејќи притисокот на гасот е константен, работата што ја врши гасот е:
. Бидејќи притисокот на гасот е константен, работата што ја врши гасот е:
Оваа работа може да се изрази во однос на промената на волуменот на гасот. Нејзиниот почетен волумен V 1 = Ш 1, и финалето V 2 = Ш 2. Затоа
каде е промената на волуменот на гасот.
Кога се шири, гасот врши позитивна работа, бидејќи насоката на силата и насоката на движење на клипот се совпаѓаат.
Ако гасот е компримиран, тогаш формулата (13.3) за работата со гас останува валидна. Но сега ![]() , а со тоа и
, а со тоа и ![]() (Сл.13.2).
(Сл.13.2).

Работа Аизведена од надворешни тела на гас се разликува од работата што ја врши самиот гас А„Само познато: ![]() , бидејќи силата што делува на гасот е насочена против силата и движењето на клипот останува исто. Според тоа, работата на надворешните сили што делуваат на гасот е еднаква на:
, бидејќи силата што делува на гасот е насочена против силата и движењето на клипот останува исто. Според тоа, работата на надворешните сили што делуваат на гасот е еднаква на:
Кога гасот е компресиран, кога , работата на надворешната сила се покажува како позитивна. Така треба да биде: кога гасот е компресиран, насоките на силата и поместувањето на точката на неговата примена се совпаѓаат.
Ако притисокот не се одржува константен, тогаш за време на експанзијата гасот губи енергија и ја пренесува на околните тела: клип што се крева, воздух итн. Гасот се лади. Кога гасот е компримиран, напротив, надворешните тела му пренесуваат енергија и гасот се загрева.
Геометриска интерпретација на делото.Работа А'гас за случај на постојан притисок може да се даде едноставна геометриска интерпретација.
Ајде да конструираме графикон за зависноста на притисокот на гасот од волуменот што го зафаќа ( Сл.13.3). Еве ја областа на правоаголникот abdc, ограничен со распоред стр 1=конст, оска Ви сегменти abИ ЦД, еднаков на притисокот на гасот, нумерички е еднаков на работата (13.3):

Во принцип, притисокот на гасот не останува константен. На пример, за време на изотермалниот процес се намалува обратно пропорционално на волуменот ( Сл.13.4). Во овој случај, за да ја пресметате работата, треба да ја поделите вкупната промена на волуменот на мали делови и да ја пресметате елементарната (мала) работа, а потоа да ги соберете сите. Работата што ја врши гасот е сè уште нумерички еднаква на површината на фигурата ограничена со графикот на зависност строд В, оска Ви сегменти abИ ЦД, еднакво на притисокот стр 1, стр2во почетната и крајната состојба на гасот.

???
1. Зошто гасовите се загреваат кога се компресирани?
2. Дали надворешните сили вршат позитивна или негативна работа за време на изотермалниот процес прикажан на слика 13.2?
G.Ya.Myakishev, B.B.Bukhovtsev, N.N.Sotsky, физика 10 одделение
Содржина на лекцијата белешки за лекцијатаподдршка на рамка лекција презентација методи забрзување интерактивни технологии Вежбајте задачи и вежби работилници за самотестирање, обуки, случаи, потраги прашања за дискусија за домашни задачи реторички прашања од ученици Илустрации аудио, видео клипови и мултимедијафотографии, слики, графики, табели, дијаграми, хумор, анегдоти, шеги, стрипови, параболи, изреки, крстозбори, цитати Додатоци апстрактистатии трикови за љубопитните креветчиња учебници основни и дополнителен речник на поими друго Подобрување на учебниците и лекциитекорекција на грешки во учебникотажурирање фрагмент во учебник, елементи на иновација во лекцијата, замена на застарените знаења со нови Само за наставници совршени лекции календарски планза една година насокипрограми за дискусија Интегрирани лекцииАко имате корекции или предлози за оваа лекција,
Основни формули на термодинамика и молекуларна физика кои ќе ви бидат корисни. Уште еден одличен ден за практична вежбање физика. Денеска ќе ги составиме формулите кои најчесто се користат за решавање на проблеми во термодинамиката и молекуларната физика.
Значи, да одиме. Да се обидеме накратко да ги претставиме законите и формулите на термодинамиката.
Идеален гас
Идеален гас е идеализација, исто како материјална точка. Молекулите на таков гас се материјални точки, а судирите на молекулите се апсолутно еластични. Ја занемаруваме интеракцијата на молекулите на далечина. Во проблемите во термодинамиката, вистинските гасови често се сметаат за идеални. Многу е полесно да се живее на овој начин и не мора да се занимавате со многу нови поими во равенките.
Значи, што се случува со молекулите на идеалниот гас? Да, тие се движат! И разумно е да се праша, со која брзина? Се разбира, покрај брзината на молекулите, нè интересира и општата состојба на нашиот гас. Каков притисок P врши на ѕидовите на садот, колкав волумен V зафаќа, која е неговата температура Т.
За да се дознае сето ова, постои идеална равенка на гас на состојбата, или Клапејрон-Менделев равенка
Еве м - маса на гас, М - неговата молекуларна тежина (ја наоѓаме од периодниот систем), Р – универзална гасна константа еднаква на 8,3144598(48) J/(mol*kg).
Универзалната гасна константа може да се изрази во однос на други константи ( Болцмановата константа и бројот на Авогадро )

Масана , пак, може да се пресмета како производ густина И волумен .

Основна равенка на молекуларната кинетичка теорија (МКТ)
Како што веќе рековме, молекулите на гасот се движат, и колку е повисока температурата, толку побрзо. Постои врска помеѓу притисокот на гасот и просечната кинетичка енергија E на неговите честички. Оваа врска се нарекува основна равенка на молекуларната кинетичка теорија и има форма:

Еве n - концентрација на молекулите (односот на нивниот број до волуменот), Е – просечна кинетичка енергија. Тие можат да се најдат, како и коренот на средната квадратна брзина на молекулите, соодветно, користејќи ги формулите:

Заменете ја енергијата во првата равенка и добиваме друга форма на основната равенка МКТ

Првиот закон на термодинамиката. Формули за изопроцеси
Да потсетиме дека првиот закон за термодинамика вели: количината на топлина што се пренесува на гасот оди за промена на внатрешната енергија на гасот U и за извршување на работата А од гасот. Формулата на првиот закон за термодинамика е напишана како следи:

Како што знаете, нешто се случува со гасот, можеме да го компресираме, можеме да го загрееме. Во овој случај, ние сме заинтересирани за процеси кои се случуваат на еден константен параметар. Ајде да погледнеме како изгледа првиот закон на термодинамиката во секој од нив.
Патем! Сега има попуст за сите наши читатели 10% на секаков вид на работа.
Изотермална процес се јавува на константна температура. Овде се применува законот Бојл-Мариот: во изотермалниот процес, притисокот на гасот е обратно пропорционален на неговиот волумен. Во изотермичен процес:

продолжува со постојан волумен. Овој процес се карактеризира со законот на Чарлс: При постојан волумен, притисокот е директно пропорционален на температурата. Во изохорен процес, целата топлина што се доставува до гасот оди да ја промени неговата внатрешна енергија.

работи со постојан притисок. Законот на Геј-Лусак вели дека при постојан притисок на гасот, неговиот волумен е директно пропорционален на температурата. Во изобаричен процес, топлината оди и за да ја промени внатрешната енергија и да ја изврши работата на гасот.

. Адијабатски процес е процес кој се јавува без размена на топлина со животната средина. Ова значи дека формулата на првиот закон за термодинамика за адијабатски процес изгледа вака:

Внатрешна енергија на монатомски и двотомски идеален гас

Топлински капацитет
Специфична топлина еднаква на количината на топлина потребна за загревање на еден килограм супстанција за еден степен Целзиусов.

Во прилог на специфичен топлински капацитет, постои моларен топлински капацитет (количината на топлина потребна за загревање на еден мол од супстанцијата за еден степен) при постојан волумен и моларен топлински капацитет при постојан притисок. Во формулите подолу, i е бројот на степени на слобода на молекулите на гасот. За еднотомски гас i=3, за дијатомски гас – 5.

Термички машини. Формула за ефикасност во термодинамиката
Топлински мотор , во наједноставен случај, се состои од грејач, фрижидер и работна течност. Грејачот дава топлина на работната течност, таа работи, потоа се лади во фрижидер и сè се повторува. О v. Типичен пример за топлински мотор е мотор со внатрешно согорување.
Коефициент корисна акција топлински мотор се пресметува со формулата

Така ги собравме основните формули на термодинамиката кои ќе бидат корисни при решавање на проблеми. Секако, ова не се сите формули од темата термодинамика, но познавањето на нив навистина може добро да ви послужи. И ако имате какви било прашања, запомнете студентска служба, чии специјалисти се подготвени да дојдат на помош во секое време.
Работа во термодинамика
Во термодинамиката, за разлика од механиката, не се разгледува движењето на телото како целина, туку само релативната промена на делови од термодинамичкиот систем, како резултат на што се менува неговиот волумен.
Да ја разгледаме работата на гасот за време на изобарична експанзија.
Дозволете ни да ја пресметаме работата што ја врши гасот кога тој делува на клипот со сила $(F")↖(→)$, еднаква по големина и спротивна во насока на силата што дејствува $(F")↖(→)$ на гасот од клипот: $ (F")↖(→)=-(F")↖(→)$ (според третиот закон на Њутн), $F"=pS$, каде што $p$ е притисокот на гасот и $S$ е површината на клипот.Ако поместувањето на клипот $∆h$ како резултат на проширување е мало, тогаш притисокот на гасот може да се смета за константен и работата на гасот е еднаква на:
$A"=F"∆h=pS∆h=p∆V$
Ако гасот се прошири, тој прави позитивна работа, бидејќи движењето на клипот се совпаѓа во насока со силата $(F")↖(→)$. Ако гасот е компримиран, тогаш работата на гасот е негативна, бидејќи движењето на клипот е спротивно на силата $(F")↖ (→)$. Во формулата $A"=F"∆h=pS∆h=p∆V$ ќе се појави знакот минус: $∆V

Работата на надворешните сили $A$, напротив, е позитивна кога гасот е компресиран и негативен кога се шири:
Со вршење на позитивна работа на гасот, надворешните тела му префрлаат дел од својата енергија. Кога гасот се шири, надворешните тела одземаат дел од неговата енергија од гасот - работата на надворешните сили е негативна.

На графиконот на притисок наспроти волуменот $p(V)$, работата е дефинирана како област ограничена со кривата $p(V)$, оската $V$ и сегментите $ab$ и $cd$ еднакви на притисок $p_1$ во почетната ($V_1 $) и $р_2$ во крајните ($V_2$) состојби, и за изобарични и за изотермални процеси.
Првиот закон на термодинамиката
Првиот закон (првиот закон) на термодинамиката е законот за зачувување и трансформација на енергијата за термодинамички систем.
Според првиот закон за термодинамика, работата може да се изврши само со топлина или некоја друга форма на енергија. Следствено, работата и количината на топлина се мерат во исти единици - џули (како и енергија).
Првиот закон на термодинамиката бил формулиран од германскиот научник Ј. Л. Мајер во 1842 година и експериментално потврден од англискиот научник Џ. Џул во 1843 година.
Првиот закон на термодинамикатае формулиран на следниов начин:
Промената на внатрешната енергија на системот за време на неговиот премин од една состојба во друга е еднаква на збирот на работата на надворешните сили и количината на топлина пренесена во системот:
каде што $∆U$ е промената на внатрешната енергија, $A$ е работата на надворешните сили, $Q$ е количината на топлина пренесена во системот.
Од $∆U=A+Q$ следува закон за зачувување на внатрешната енергија.Ако системот е изолиран од надворешни влијанија, $A=0$ и $Q=0$, и затоа $∆U=0$.
За време на сите процеси што се случуваат во изолиран систем, неговата внатрешна енергија останува константна.
Ако работата ја врши системот, а не надворешните сили, тогаш равенката ($∆U=A+Q$) се запишува како:
каде што $A"$ е работата што ја врши системот ($A"=-A$).
Количината на топлина пренесена во системот оди за да ја промени неговата внатрешна енергија и да врши работа на надворешни тела од системот.
Првиот закон на термодинамиката може да се формулира како неможност за постоење машина за постојано движењеод првиот вид, кој би работел без црпење енергија од кој било извор, односно само на сметка на внатрешната енергија.
Навистина, ако на телото не му се доставува топлина ($Q=0$), тогаш работата $A"$, според равенката $Q=∆U+A"$, се изведува само поради намалувањето на внатрешната енергија. $A"=-∆U$ Откако ќе се потроши енергетската резерва, моторот престанува да работи.
Треба да се запомни дека и работата и количината на топлина се карактеристики на процесот на промена на внатрешната енергија, така што не може да се каже дека системот содржи одредена количина на топлина или работа. Систем во која било држава има само одредена внатрешна енергија.
Примена на првиот закон за термодинамика на различни процеси
Да ја разгледаме примената на првиот термодинамички закон за различни термодинамички процеси.
Изохорен процес.Зависноста $p(T)$ од термодинамичкиот дијаграм е прикажана изохора.
Изохорен (изохорен) процес е термодинамички процес што се случува во систем со постојан волумен.
Изохоричниот процес може да се изврши во гасови и течности затворени во сад со постојан волумен.
За време на изохорен процес, волуменот на гасот не се менува ($∆V=0$), а според првиот термодинамички закон $Q=∆U+A"$,
т.е., промената на внатрешната енергија е еднаква на количината на пренесена топлина, бидејќи работата ($A=p∆V=0$) не ја врши гасот.

Ако гасот се загрева, тогаш $Q > 0$ и $∆U > 0$, неговата внатрешна енергија се зголемува. При ладење гас $Q
Изотермален процесприкажан графички изотерм.
Изотермалниот процес е термодинамички процес кој се јавува во систем на константна температура.
Бидејќи за време на изотермалниот процес внатрешната енергија на гасот не се менува ($T=const$), тогаш целата количина на топлина пренесена на гасот оди за извршување на работата:
Кога гасот добива топлина ($Q > 0$), тој прави позитивна работа ($A" > 0$). Ако гасот испушта топлина на околината, $Q
Изобарен процесТермодинамичкиот дијаграм покажува изобар.
Изобарен (изобарен) процес е термодинамички процес што се случува во систем со постојан притисок $p$.
Пример за изобаричен процес е проширувањето на гасот во цилиндар со натоварен клип што слободно се движи.
Во изобарен процес, според формулата $Q=∆U+A"$, количината на топлина пренесена на гасот оди да ја промени неговата внатрешна енергија $∆U$ и да изврши работа $A"$ при постојан притисок:
Работата на идеален гас е одредена од графикот $p(V)$ за изобарен процес ($A"=p∆V$).
За идеален гас во изобарен процес, волуменот е пропорционален на температурата; кај реалните гасови, дел од топлината се троши на промена на просечната енергија на интеракцијата на честичките.
Адијабатски процес
Адијабатски процес (адијабатски процес) е термодинамички процес што се случува во систем без размена на топлина со околината ($Q=0$).
Адијабатската изолација на системот приближно се постигнува во садовите Девар, во таканаречените адијабатски школки. Адијабатски изолираниот систем не е под влијание на промените во температурата на околните тела. Неговата внатрешна енергија може да се промени само поради работата што ја вршат надворешните тела на системот, или самиот систем.
Според првиот закон на термодинамиката ($∆U=A+Q$), во адијабатски систем
каде што $A$ е работа на надворешни сили.
При адијабатско ширење на гасот $A
Оттука,
$∆U=(i)/(2)·(m)/(M)R∆T
што значи намалување на температурата при адијабатско проширување. Тоа води до фактот дека притисокот на гасот се намалува посилно отколку за време на изотермалниот процес.

На сликата, adiabat $1-2$, поминувајќи помеѓу две изотерми, јасно го илустрира она што е кажано. Површината под адијабатот е нумерички еднаква на работата што ја врши гасот за време на неговото адијабатско проширување од волуменот $V_1$ до $V_2$.
Адијабатската компресија доведува до зголемување на температурата на гасот, бидејќи како резултат на еластични судири на молекулите на гасот со клипот, нивната просечна кинетичка енергија се зголемува, за разлика од експанзијата, кога се намалува (во првиот случај, брзините на молекулите на гасот се зголемуваат , во втората се намалуваат).
Остро загревање на воздухот за време на адијабатска компресија се користи во Дизел моторите.
Принцип на работа на топлинските мотори
Топлински мотор е уред кој ја претвора внатрешната енергија на горивото во механичка енергија.
Според вториот закон за термодинамика, топлинскиот мотор може постојано да врши периодичен циклус механичка работапоради ладењето на околните тела, ако не само што прима топлина од потопло тело (грејач), туку во исто време дава топлина на помалку загреано тело (фрижидер). Следствено, не се користи целата количина на топлина добиена од грејачот за извршување на работата, туку само дел од неа.
Така, главните елементи на секој топлински мотор се:
- работна течност (гас или пареа) вршење работа;
- грејач што дава енергија на работната течност;
- фрижидер кој апсорбира дел од енергијата од работниот флуид.

Ефикасност на топлинскиот мотор
Според законот за зачувување на енергијата, работата што ја врши моторот е еднаква на:
$A"=|Q_1|-|Q_2|$
каде што $Q_1$ е количината на топлина добиена од грејачот, $Q_2$ е количината на топлина дадена на фрижидерот.
Фактор на ефикасност(Ефикасност) на топлинскиот мотор е односот на работата $A"$ што ја извршува моторот до количината на топлина добиена од грејачот:
$η=(A")/(|Q_1|)=(|Q_1|-|Q_2|)/(|Q_1|)=1-(|Q_2|)/(|Q_1|)$
Бидејќи сите мотори пренесуваат одредена количина на топлина во фрижидерот, тогаш $η
Ефикасноста на топлинскиот мотор е пропорционална на температурната разлика помеѓу грејачот и фрижидерот. Кога $T_1 - T_2=0$ моторот не може да работи.
Циклус Карно
Циклусот Карно е кружен реверзибилен процес кој се состои од два изотермални и два адијабатски процеси.
Овој процес првпат бил разгледан од францускиот инженер и научник Н.Л.С. Карно во 1824 година во книгата „Рефлексии за движечка силаоган и за машини способни да ја развијат оваа сила“.
Целта на истражувањето на Карно беше да ги открие причините за несовршеноста на топлинските мотори од тоа време (тие имаа ефикасност од $< 5%$)и поиски путей их усовершенствования.
Изборот на два изотермални и два адијабатски процеси се должи на тоа што работата на гасот за време на изотермалното проширување се остварува поради внатрешната енергија на грејачот, а за време на адијабатски процес, поради внатрешната енергија на гасот што се шири. Во овој циклус, контактот на тела со различни температури е исклучен, па затоа е исклучен пренос на топлина без работа.
Циклусот Карно е најефикасен од сите. Неговата ефикасност е максимална.

Сликата ги прикажува термодинамичките процеси на циклусот. Во процесот на изотермална експанзија ($1-2$) на температура $T_1$, работата се врши со промена на внатрешната енергија на грејачот, т.е. со снабдување на количината на топлина $Q_1$ на гасот:
$A_(12)=Q_1.$ Ладењето со гас пред компресија ($3-4$) се случува при адијабатско проширување ($2-3$). Промената на внатрешната енергија $∆U_(23)$ за време на адијабатски процес ($Q=0$) целосно се претвора во механичка работа:
$A_(23)=-∆U_(23)$
Температурата на гасот како резултат на адијабатско проширување ($2-3$) се намалува до температурата на фрижидерот $T_2
Циклусот завршува со процесот на адијабатска компресија ($4-1$), при што гасот се загрева до температура од $T_1$.
Максимална вредност на ефикасноста на идеалните топлински мотори на гас според циклусот Карно:
$η=(T_1-T_2)/(T_1)=1-(T_2)/(T_1)$
Суштината на формулата $η=(T_1-T_2)/(T_1)=1-(T_2)/(T_1)$ е изразена во теоремата докажана од С. Карно дека ефикасноста кој било топлински мотор не може да ја надмине ефикасноста на циклусот Карно што се изведува на иста температура на грејачот и фрижидерот.
Примената на оптоварување на која било структура предизвикува нејзиното деформирање. Во овој случај, делови од структурата ја напуштаат состојбата на мирување и добиваат одредени брзини и забрзувања. Ако оптоварувањето полека се зголемува, тогаш овие забрзувања се мали, и затоа инерцијалните сили што се развиваат при преминот на системот во деформирана состојба може да се занемарат. Таквата мазна (постепена) примена на оптоварување се нарекува статична.
Дозволете ни да ја одредиме работата на надворешно оптоварување, на пример, сила P, статички применета на некој еластичен систем (сл. 1.11), чиј материјал го задоволува Хуковиот закон.
За мали деформации, принципот на независно дејство на силите е применлив за овој систем, и затоа движењата на поединечните точки и делови од конструкцијата се директно пропорционални со големината на оптоварувањето што ги предизвикува. ВО општ погледоваа зависност може да се изрази со еднаквоста
Овде A е поместувањето во насока на силата P; а е одреден коефициент во зависност од материјалот, дизајнот и големината на конструкцијата.
Да ја зголемиме силата P за бесконечно мала количина. Овој прираст ќе предизвика зголемување на поместувањето за износот
Дозволете ни да составиме израз за елементарната работа на надворешната сила на поместување, отфрлајќи ги бесконечно малите количества од вториот ред на малечок:
Вредноста врз основа на формулата (1.11) ја заменуваме со изразот
Интегрирање на овој израз во целосна променасила од нула до нејзината крајна вредност, добиваме формула за одредување на работата направена од статички применета надворешна сила P:

Бидејќи добиената формула може да се претстави во форма
Општо земено, насоката на силата P може да не се совпаѓа со насоката на движењето предизвикано од неа. Бидејќи големината на работата е одредена од производот на силата и патеката помината во насока на оваа сила, вредноста А мора да се разбере како проекција на вистинското (вкупно) поместување на точката на примена на силата на насоката на силата. На пример, кога силата P се применува под агол на хоризонталната оска (сл. 2.11), поместувањето А се мери со сегмент (што ја претставува проекцијата на вистинското поместување на насоката на силата P).


Во случај кога на системот се применуваат пар сили со вртежен момент (концентриран момент), изразот за работата може да се добие на сличен начин. Во овој случај, неопходно е да се избере типот на движење што одговара на концентрираниот момент; ова ќе биде аголот на ротација пресекзрак на кој се применува моментот.
На пример, работата на моментот статички се применува на зракот прикажан на сл. 3.11,
каде што O е аголот на ротација (во радијани) на делот од гредата на кој се применува моментот Ш.
Значи, работата на надворешната сила при нејзиното статичко дејство на која било еластична структура е еднаква на половина од производот од вредноста на оваа сила и вредноста на соодветното поместување.
За да се генерализира добиениот заклучок, со сила го разбираме секое влијание применето на еластичен систем, т.е. не само концентрирана сила, туку и момент, рамномерно распределен товар итн.; Под движење го подразбираме видот на движење во кој дадена моќја врши работата. Концентрираната сила P одговара на линеарно поместување, момент - аголна и рамномерно дистрибуиран товар- област на дијаграмот за поместување во областа на оптоварување.
Кога група надворешни сили делуваат статички на структурата, работата на овие сили е еднаква на половина од збирот на производите на секоја сила и количината на нејзиното соодветно поместување предизвикано од дејството на целата група сили.
Така, на пример, кога дејствувате на зракот прикажан на сл. 4.11, концентрирани сили и концентрирани моменти, работа на надворешни сили

Знакот минус пред последниот член на изразот е усвоен затоа што насоката на аголот на вртење на пресекот на зракот во кој се применува моментот е спротивна на насоката на овој момент.
Работата на надворешните сили на поместувањата што ги предизвикуваат може да се изрази и на друг начин, имено: преку моменти на свиткување, надолжни и попречни сили кои произлегуваат во пресеците на конструктивните прачки.


Да избереме од праволиниска прачка со два пресеци нормални на неговата оска (сл. 5.11) бесконечно мал елемент со должина (елемент). Прачката се состои од бесконечно голем бројтаквите елементи. На елемент во општиот случај проблем со авионотсе применуваат надолжната сила N, моментот на свиткување M и попречната сила
Силите N, M, Q се внатрешни сили во однос на целата прачка. Меѓутоа, за одбран елемент тие се надворешни сили и затоа работата А може да се добие како збир на работата извршена со статички зголемување на силите N, M, Q на соодветните деформации на елементите.Да го разгледаме посебно влијанието на секоја од овие сили на елементот
Елемент кој е подложен на само надолжни сили N е прикажан на сл. 6.11. Ако неговиот лев дел се смета за неподвижен, тогаш десниот дел, под влијание на надолжната сила, ќе се помести надесно за износот.При ова движење, статички растечката сила N ќе изврши работа
Елемент кој е подложен на само моменти на свиткување M е прикажан на сл. 7.11.


Ако неговиот лев дел не е подвижно фиксиран, тогаш меѓусебниот агол на ротација на крајните делови на елементот ќе биде еднаков на аголотсвртете се кон нејзиниот десен дел [види. формулата (16.7) и сл. 33,7]:
![]()
На ова аголно поместување, статички растечкиот момент М ќе работи
Елемент кој е подложен на само сили на смолкнување Q е прикажан на сл. 8.11, а. Откако го фиксиравме неговиот лев пресек (слика 8.11, б), применуваме тангентални сили на десната, чиј резултат е попречна сила
Да претпоставиме дека тангенцијалните напрегања се рамномерно распоредени на целата површина F на пресекот, т.е. тогаш поместувањето (сл. 8.11б) предизвикано од дејството на попречната сила Q, што е поместување на крајните делови на елемент релативно еден на друг, врз основа на формулата (3.4) ќе се определи од изразот
и работата на статички растечката сила Q на ова поместување