Shuningdek qarang: Kimyoviy elementlarning atom sonlari bo'yicha ro'yxati va alfavit bo'yicha kimyoviy elementlarning ro'yxati Mundarija 1 Hozirgi belgilar ... Vikipediya
Shuningdek qarang: Belgilar bo'yicha kimyoviy elementlarning ro'yxati va alfavit bo'yicha kimyoviy elementlar ro'yxati Bu atom sonlarining o'sish tartibida saralangan kimyoviy elementlarning ro'yxati. Jadvalda ... ... Vikipediyada element, belgi, guruh va davr nomi ko'rsatilgan
- (ISO 4217) Valyutalar va mablag'larni namoyish qilish uchun kodlar (Ingliz tili) Kodlar la représentation des monnaies et types de fonds (frantsuzcha) ... Vikipediya
Kimyoviy usullar bilan aniqlash mumkin bo'lgan moddalarning eng oddiy shakli. Bular oddiy va murakkab moddalarning tarkibiy qismlari bo'lib, ular bir xil yadro zaryadi bo'lgan atomlar to'plamidir. Atom yadrosining zaryadi ... tarkibidagi protonlar soni bilan aniqlanadi. Collier ensiklopediyasi
Mundarija 1 Paleolit \u200b\u200bdavri 2 Miloddan avvalgi 10-ming yillik e. Miloddan avvalgi 3-ming yillik uh ... Vikipediya
Mundarija 1 Paleolit \u200b\u200bdavri 2 Miloddan avvalgi 10-ming yillik e. Miloddan avvalgi 3-ming yillik uh ... Vikipediya
Ushbu atama boshqa ma'nolarga ega, rus tiliga qarang (ma'nolari). Ruslar ... Vikipediya
Terminologiya 1 :: dw hafta kuni. "1" dushanba kuniga to'g'ri keladi. Turli xil hujjatlardagi atama ta'riflari: dw DUT UTC va UTC o'rtasidagi farq, soat sonining butun sonida ko'rsatilgan. Terminning ta'riflari ... ... Normativ-texnik hujjatlar atamalarining lug'at-ma'lumotnomasi
"Kimyoviy element - oltingugurt" - Tabiiy oltingugurt kristallarining tabiiy agregati. Yopiq (S4, S6) zanjirli va ochiq zanjirli molekulalar mumkin. Oltingugurt rudalari har xil usulda qazib olinadi - vujudga kelish sharoitlariga qarab. Tabiiy oltingugurt minerallari. Uning o'z-o'zidan yonishi ehtimoli haqida unutmasligimiz kerak. Rudani ochiq usulda qazib olish. Yuradigan ekskavatorlar ruda yotadigan tosh qatlamlarini olib tashlaydi.
"Kimyoviy elementlar to'g'risida savollar" - barqaror va radioaktiv, sun'iy va tabiiy bo'lishi mumkin. Asosiy kichik guruhlarda energiya darajasi sonining o'zgarishi bilan bog'liq. 8. Qaysi element Davriy jadvalda doimiy "ro'yxatdan o'tishga" ega emas? Doimiy harakatda. Telluriy, 2) selen, 3) osmiy, 4) germaniy. Mishyak qayerda to'planadi?
"H2O va H2S" - sulfat ioni. Y \u003d? K K2 \u003d 1,23 × 10 × 13 mol / l. Olingan: Na2SO3 + S \u003d Na2SO3S (+ t, aq.r-r). Suvli eritmada: + Hcl (efir). Sulfat MSO4 · 5 (7) H2O (M - Cu, Fe, Ni, Mg ...). Oltingugurt kislotasi H2SO4. SO32– va HSO3– anionlarining tuzilishi. \u003d y. SO3 molekulasi qutbsiz va diamagnetikdir. ? ... Gidrosulfit ioni: tautomerizm.
"Kimyoviy elementlarning davriy jadvali" - 8. Uchinchi energiya darajasida maksimal elektronlar soni qancha bo'lishi mumkin? Elementlarni metall xususiyatlarini ortish tartibida joylashtiring. Mamlakat nomi: "Kimyoviy elementar". Matn so'zlari Stepan Shchipachev. A. 17 B. 35 C. 35,5 D. 52 6. Ftor atomidagi yadro atrofida qancha elektron aylanadi?
"Kaltsiy Ca" - Ca birikmalari. Ca ning kimyoviy xossalari. Ca ning fizik xususiyatlari. Kaltsiy umumiy elementlardan biridir. Ilova. Sanoatda kaltsiy olish. Kaltsiy Ca. Ca ning fizikaviy xususiyatlarini aytib bering. Tabiatda bo'lish. Takrorlash uchun topshiriq. Kaltsiy Ca - kumushrang oq va juda qattiq metall, engil.
"Element fosfor" - Fosfor tabiatda eng ko'p tarqalgan 12-element. Oddiy moddalar - metall bo'lmagan moddalar bilan o'zaro ta'sirlashish. Metall bilan o'zaro ta'sir. Kaltsiy birikmalarini bog'lash uchun kvarts qumi qo'shiladi. Oq fosforni gidroksidi eritmasida qizdirganda u mutanosib bo'ladi. Fosfor. Qora fosfor.
Hammasi bo'lib 46 ta taqdimot mavjud
Davriy jadvaldan qanday foydalanish kerak? Ma'lum bo'lmagan odam uchun davriy jadvalni o'qish gnome uchun qadimgi elf rinalariga qarashga o'xshaydi. Va davriy jadval dunyo haqida ko'p narsalarni aytib berishi mumkin.
Bu sizga imtihonda xizmat qilishi bilan bir qatorda, juda ko'p sonli kimyoviy va fizikaviy muammolarni hal qilishda shunchaki almashtirib bo'lmaydi. Ammo uni qanday o'qish kerak? Yaxshiyamki, bugungi kunda hamma ushbu san'atni o'rganishi mumkin. Ushbu maqolada biz sizga davriy jadvalni qanday tushunishni aytib beramiz.
Kimyoviy elementlarning davriy jadvali (davriy jadval) - bu elementlarning turli xil xususiyatlarining atom yadrosi zaryadiga bog'liqligini o'rnatadigan kimyoviy elementlarning tasnifi.
Jadval yaratish tarixi
Dmitriy Ivanovich Mendeleyev oddiy kimyochi emas edi, agar kimdir shunday deb hisoblasa. U kimyogar, fizik, geolog, metrolog, ekolog, iqtisodchi, neftchi, aeronavt, asbobsoz va o'qituvchi bo'lgan. Olim hayoti davomida turli xil bilim sohalarida ko'plab fundamental tadqiqotlar o'tkazishga muvaffaq bo'ldi. Masalan, aroqning ideal kuchini - 40 darajani hisoblagan Mendeleyev bo'lgan degan fikr keng tarqalgan.
Mendeleyevning aroqqa qanday munosabatda bo'lganligini bilmaymiz, ammo "Alkogolning suv bilan birikmasi bo'yicha nutq" mavzusidagi dissertatsiyasi aroq bilan hech qanday aloqasi bo'lmaganligi va spirtning 70 darajadan konsentratsiyasini ko'rib chiqqanligi aniq ma'lum. Olimning barcha yutuqlari bilan tabiatning asosiy qonunlaridan biri bo'lgan kimyoviy elementlarning davriy qonunini kashf etish unga eng keng ommalashishni olib keldi.

Bir afsona bor, unga ko'ra olim davriy tizimni orzu qilgan, shundan keyin u faqat paydo bo'lgan g'oyani takomillashtirishga to'g'ri kelgan. Ammo, agar hamma narsa shunchalik sodda bo'lsa edi ... Davriy jadvalni yaratishning ushbu versiyasi, afsonadan boshqa narsa emas. Stol qanday ochilgani haqidagi savolga Dmitriy Ivanovichning o'zi javob berdi: " Men bu haqda ehtimol yigirma yildan beri o'ylayapman, lekin siz o'ylaysiz: men o'tirdim va to'satdan ... bu amalga oshdi. "
O'n to'qqizinchi asrning o'rtalarida ma'lum kimyoviy elementlarga buyurtma berishga urinishlar (63 ta element ma'lum bo'lgan) bir vaqtning o'zida bir nechta olimlar tomonidan qilingan. Masalan, 1862 yilda Aleksandr Emil Chankourtua spiral chiziq bo'ylab elementlarni joylashtirdi va kimyoviy xususiyatlarning tsiklik takrorlanishini qayd etdi.
Kimyogar va musiqachi Jon Aleksandr Newlands 1866 yilda davriy tizimning o'z versiyasini taklif qildi. Qizig'i shundaki, olim elementlarning joylashishida ba'zi sirli musiqiy uyg'unlikni topishga harakat qildi. Boshqa urinishlar qatorida Mendeleevning urinishi ham muvaffaqiyat qozondi.

1869 yilda jadvalning birinchi sxemasi nashr etildi va 1869 yil 1 mart davriy qonun ochilgan kun deb hisoblanadi. Mendeleyev kashfiyotining mohiyati shundaki, atom massasi oshgan elementlarning xossalari bir xilda emas, balki davriy ravishda o'zgarib turadi.
Jadvalning birinchi versiyasida faqat 63 ta element bor edi, ammo Mendeleyev bir qator juda nostandart echimlarni ishlab chiqardi. Shunday qilib, u kashf qilinmagan elementlar uchun jadvalda bo'sh joy qoldirishni taxmin qildi va ba'zi elementlarning atom massalarini ham o'zgartirdi. Mendeleyev tomonidan chiqarilgan qonunning tubdan to'g'riligi olimlar tomonidan bashorat qilingan galliy, skandiy va germaniy kashf qilingandan keyin tez orada tasdiqlandi.
Davriy tizimning zamonaviy ko'rinishi
Quyida jadvalning o'zi joylashgan
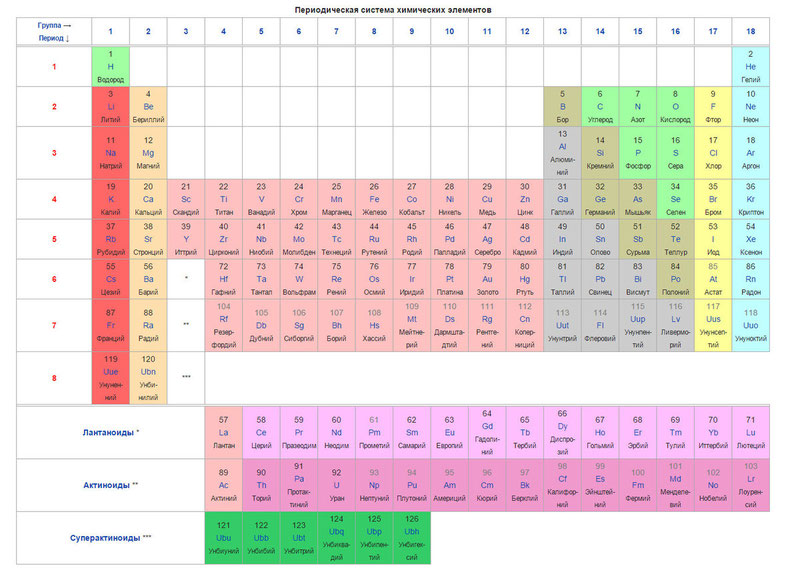
Bugungi kunda elementlarga buyurtma berish uchun atom og'irligi (atom massasi) o'rniga atom raqami (yadrodagi proton soni) tushunchasi qo'llanilmoqda. Jadvalda 120 ta element mavjud bo'lib, ular chapdan o'ngga atom sonining o'sish tartibida (protonlar soni) joylashgan
Jadvalning ustunlari guruhlar deb ataladi va qatorlar nuqta. Jadval 18 guruh va 8 davrni o'z ichiga oladi.
- Elementlarning metall xossalari davr bo'ylab chapdan o'ngga siljish paytida kamayadi va teskari yo'nalishda ko'payadi.
- Davrlar davomida chapdan o'ngga harakatlanayotganda atomlarning o'lchamlari kamayadi.
- Guruhda yuqoridan pastgacha harakatlanayotganda qaytaruvchi metall xossalari oshadi.
- Chapdan o'ngga davr bo'ylab harakatlanayotganda oksidlovchi va metall bo'lmagan xususiyatlar ortadi.
Jadvaldagi buyum haqida nimani bilib olamiz? Masalan, jadvaldagi uchinchi element - litiyni olamiz va batafsil ko'rib chiqamiz.

Avvalo, biz element belgisini va uning ostida uning nomini ko'ramiz. Yuqoridagi chap burchakda element jadvalda joylashgan tartibda elementning atom raqami joylashgan. Atom raqami, allaqachon aytib o'tilganidek, yadrodagi protonlar soniga teng. Ijobiy protonlarning soni odatda atomdagi manfiy elektronlar soniga teng (izotoplardan tashqari).
Atom massasi atom raqami ostida ko'rsatilgan (jadvalning ushbu versiyasida). Agar biz atom massasini butun songacha yaxlitlasak, massa deb ataladigan sonni olamiz. Massa raqami bilan atom raqami orasidagi farq yadrodagi neytronlar sonini beradi. Shunday qilib, geliy yadrosidagi neytronlar soni ikkitani, litiyda esa to'rttani tashkil qiladi.
Shunday qilib bizning "Dummies uchun davriy jadval" kursimiz yakunlandi. Xulosa qilib aytganda, biz sizni tematik videoni ko'rishga taklif qilamiz va davriy jadvaldan qanday foydalanish masalasi siz uchun yanada aniqroq bo'ldi deb umid qilamiz. Sizga shuni eslatib o'tamizki, yangi mavzuni yolg'iz emas, balki tajribali ustoz yordamida o'rganish har doimgidan ham samaralidir. Shu sababli, siz o'zingizning bilimingiz va tajribangizni xursandchilik bilan baham ko'radigan talabalar xizmati haqida hech qachon unutmasligingiz kerak.
Agar davriy jadvalni tushunish qiyin bo'lsa, siz yolg'iz emassiz! Uning printsiplarini tushunish qiyin bo'lsa-da, u bilan ishlashni bilish sizga fanlarni o'rganishda yordam beradi. Dastlab, jadvalning tuzilishini va undan har bir kimyoviy element haqida qanday ma'lumot olish mumkinligini o'rganing. Keyin har bir elementning xususiyatlarini o'rganishni boshlashingiz mumkin. Va nihoyat, davriy jadval yordamida ma'lum bir kimyoviy element atomidagi neytronlar sonini aniqlash mumkin.
Qadamlar
1-qism
Jadval tuzilishi-
Ko'rib turganingizdek, har bir keyingi element oldingi elementga qaraganda bitta ko'proq protonga ega. Bu atom raqamlariga qaraganingizda aniq bo'ladi. Chapdan o'ngga siljiganingizda atom sonlari bittaga ko'payadi. Ob'ektlar guruhlarga ajratilganligi sababli jadvaldagi ba'zi kataklar bo'sh.
- Masalan, jadvalning birinchi qatorida atom raqami 1 bo'lgan vodorod va atom raqami 2 bo'lgan geliy mavjud, ammo ular qarama-qarshi qirralarda joylashgan, chunki ular turli guruhlarga tegishli.
-
Fizikaviy va kimyoviy xususiyatlariga o'xshash elementlarni o'z ichiga olgan guruhlar haqida ma'lumot oling. Har bir guruh elementlari tegishli vertikal ustunda joylashgan. Odatda, ular bir xil rang bilan ko'rsatiladi, bu fizikaviy va kimyoviy xususiyatlarga o'xshash elementlarni aniqlashga va ularning xatti-harakatlarini taxmin qilishga yordam beradi. U yoki bu guruhning barcha elementlari tashqi qobiqda bir xil miqdordagi elektronga ega.
- Vodorodni ham gidroksidi metal guruhiga, ham halogen guruhiga kiritish mumkin. Ba'zi jadvallarda u ikkala guruhda ham ko'rsatilgan.
- Ko'pgina hollarda, guruhlar 1 dan 18 gacha raqamlanadi, jadvalning yuqori yoki pastki qismida raqamlar mavjud. Xonalarni rim (masalan, IA) yoki arabcha (masalan, 1A yoki 1) raqamlar bilan ko'rsatish mumkin.
- Ustun bo'ylab yuqoridan pastga harakatlanish "guruhni ko'rish" deb aytiladi.
-
Jadvalda nima uchun bo'sh kataklar mavjudligini bilib oling. Elementlar nafaqat atom soniga qarab, balki guruhlarga ko'ra ham tartiblanadi (bir guruh elementlari o'xshash fizikaviy va kimyoviy xususiyatlarga ega). Bu u yoki bu element o'zini qanday tutishini tushunishni osonlashtiradi. Biroq, atom sonining o'sishi bilan, tegishli guruhga kiradigan elementlar har doim ham topilmaydi, shuning uchun jadvalda bo'sh hujayralar mavjud.
- Masalan, dastlabki 3 qatorda bo'sh hujayralar mavjud, chunki o'tish metallari faqat 21 atom raqamidan topilgan.
- 57 dan 102 gacha bo'lgan atom raqamlari bo'lgan elementlar noyob tuproq elementlari deb tasniflanadi va odatda jadvalning pastki o'ng burchagidagi alohida kichik guruhda keltirilgan.
-
Jadvaldagi har bir satr nuktani bildiradi. Xuddi shu davrdagi barcha elementlar atomlaridagi elektronlar joylashgan bir xil miqdordagi atom orbitallariga ega. Orbitallar soni davr soniga to'g'ri keladi. Jadvalda 7 qator, ya'ni 7 nuqta bor.
- Masalan, birinchi davr elementlari atomlari bitta orbitalga, ettinchi davr elementlari atomlari esa 7 orbitalga ega.
- Odatda, davrlar jadvalning chap qismidagi 1 dan 7 gacha bo'lgan raqamlar bilan belgilanadi.
- Chapdan o'ngga chiziq bo'ylab harakatlanish "nuqta ko'rish" deb aytiladi.
-
Metalllarni, metalloidlarni va metall bo'lmaganlarni farqlashni o'rganing. Elementning qaysi turiga mansubligini aniqlasangiz, uning xususiyatlarini yaxshiroq tushunasiz. Qulaylik uchun ko'pgina jadvallarda metallar, metalloidlar va metall bo'lmaganlar turli xil ranglar bilan ko'rsatilgan. Jadvalning chap tomonida metalllar, o'ng tomonida esa metall bo'lmaganlar joylashgan. Metalloidlar ular orasida joylashgan.
2-qism
Element belgilari-
Har bir element bir yoki ikkita lotin harflari bilan belgilanadi. Odatda element belgisi tegishli katak markazida katta harflar bilan ko'rsatiladi. Ramz - bu elementning qisqartirilgan nomi, aksariyat tillarda bir xil. Eksperimentlar o'tkazishda va kimyoviy tenglamalar bilan ishlashda odatda elementlarning belgilaridan foydalaniladi, shuning uchun ularni eslab qolish foydalidir.
- Odatda, elementlarning ramzlari ularning lotincha ismining qisqartmalaridir, garchi ba'zilar uchun, ayniqsa yaqinda kashf etilgan elementlar, ular umumiy nomdan kelib chiqqan. Masalan, geliy He belgisi bilan belgilanadi, aksariyat tillarda umumiy nomga yaqin. Shu bilan birga, temirni Fe deb atashadi, bu uning lotincha nomining qisqartmasi.
-
Jadvalda ko'rsatilgan bo'lsa, elementning to'liq nomiga e'tibor bering. Elementning ushbu "nomi" oddiy matnda ishlatiladi. Masalan, "geliy" va "uglerod" elementlarning nomlari. Odatda, har doim ham bo'lmasa ham, elementlarning to'liq nomlari ularning kimyoviy belgisi ostida keltirilgan.
- Ba'zan jadvalda elementlarning nomlari ko'rsatilmagan va faqat ularning kimyoviy belgilari berilgan.
-
Atom raqamini toping. Odatda elementning atom raqami mos keladigan katakchaning yuqori qismida, o'rtada yoki burchakda joylashgan. Shuningdek, u belgi yoki element nomi ostida ko'rinishi mumkin. Elementlar 1 dan 118 gacha bo'lgan atom raqamlariga ega.
- Atom raqami har doim butun son hisoblanadi.
-
Atom raqami atomdagi proton soniga mos kelishini unutmang. Elementning barcha atomlarida bir xil miqdordagi proton mavjud. Elektronlardan farqli o'laroq, element atomlaridagi protonlar soni doimiy bo'lib qoladi. Aks holda, yana bir kimyoviy element paydo bo'lgan bo'lar edi!
- Elementning atom raqami, shuningdek, atomdagi elektronlar va neytronlar sonini aniqlay oladi.
-
Odatda elektronlar soni protonlar soniga teng. Istisno - atom ionlashtirilganda. Protonlar musbat, elektronlar esa salbiy zaryadga ega. Atomlar odatda neytral bo'lganligi sababli ular tarkibida bir xil miqdordagi elektron va proton mavjud. Biroq, atom elektronlarni ushlashi yoki yo'qotishi mumkin, bu holda u ionlashadi.
- Ionlar elektr zaryadiga ega. Agar ionda ko'proq proton bo'lsa, u holda musbat zaryad bo'ladi va bu holda element belgisidan keyin plyus belgisi qo'yiladi. Agar ion ko'proq elektronni o'z ichiga olsa, manfiy zaryadga ega, bu minus belgisi bilan ko'rsatiladi.
- Agar atom ion bo'lmasa, ortiqcha va minus belgilaridan foydalanilmaydi.
-
Davriy jadval yoki kimyoviy elementlarning davriy jadvali yuqori chap burchakdan boshlanadi va jadvalning so'nggi satrining oxirida (pastki o'ng burchakda) tugaydi. Jadvaldagi elementlar chapdan o'ngga atom sonining o'sish tartibida joylashtirilgan. Atom raqami bitta atomda qancha proton borligini ko'rsatadi. Bundan tashqari, atom sonining ko'payishi bilan atom massasi ham ko'payadi. Shunday qilib, elementning davriy jadvaldagi joylashuvi bo'yicha siz uning atom massasini aniqlashingiz mumkin.
Qadimgi yunon donishmandlari "element" so'zini birinchi bo'lib aytishgan va bu bizning davrimizdan besh asr oldin sodir bo'lgan. To'g'ri, qadimgi yunonlar "elementlarni" temir, kislorod, vodorod, azot va hozirgi kimyochilarning boshqa elementlari emas, balki er, suv, havo va olov deb hisoblashgan.
O'rta asrlarda olimlar allaqachon bilishgan o'nta kimyoviy element - Yetti metallar (oltin, kumush, mis, temir, qalay, qo'rg'oshin va simob) va uchta metall bo'lmagan (oltingugurt, uglerod va surma).
"Simob" nima ekanligini boshqa lug'atlarda ko'ring
Inson tanasidagi eng qiyin material tish emalidir. Tishlarimiz tishlash va chaynash uchun bizga butun umr xizmat qilishi uchun qiyin bo'lishi kerak; ammo, tish emalining kimyoviy hujumga moyil bo'lishi mumkin. Ba'zi oziq-ovqat mahsulotlarida mavjud bo'lgan yoki tishimizdagi oziq-ovqat qoldiqlari bilan oziqlanadigan bakteriyalar ishlab chiqaradigan kislotalar emalni eritishi mumkin. Tish emaldan himoyalanmagan holda chiriy boshlaydi, shu bilan bo'shliqlar va boshqa tish muammolari paydo bo'ladi.
Bir necha yillik izlanishlardan so'ng, ichimlik suvidagi ortiqcha ftorli birikmalar ushbu ikkala ta'sir uchun ham javobgar ekanligi aniqlandi. Ftoridning himoya ta'siri oddiy kimyoviy tushuntirishga ega. Tish emallari asosan kaltsiy, fosfor, kislorod va vodoroddan tashkil topgan gidroksiapatit mineralidan iborat. Endi biz bilamizki, ftor gidroksiapatit bilan birikib ftorapatit ishlab chiqaradi, bu esa gidroksiapatitga qaraganda kislota parchalanishiga ancha chidamli. Ushbu ataylab ftorlash, ftorli tish pastalaridan foydalanish va og'iz gigienasining yaxshilanishi bilan birgalikda bolalarda kariesning 60% kamayishiga olib keldi.
Alkimyogarlar juda uzoq vaqt til topishdilar kimyoviy formulalarsiz... Amalda g'alati piktogrammalar mavjud edi va deyarli har bir kimyogar o'zlarining nomlash tizimidan foydalangan. Va kimyoviy o'zgarishlarning tavsiflari ertak va afsonalarga o'xshardi.
Masalan, alkimyogarlar simob oksidi (qizil modda) bilan xlorid (xlorid) kislota reaktsiyasini qanday ta'rifladilar:
Tish chirishining butun mamlakat bo'ylab kamayishi tarixda sog'liqni saqlashning muhim yutug'i sifatida qayd etilgan. Tilda so'zlar tuziladigan alifbo bo'lganidek, kimyoda materiya tasvirlangan alifbo mavjud. Biroq, kimyoviy alifbo biz yozish uchun ishlatiladigan alifbodan kattaroqdir. Ehtimol siz allaqachon kimyoviy alifbo kimyoviy elementlardan tashkil topganligini tushungan bo'lishingiz mumkin. Ularning roli kimyo uchun muhim ahamiyatga ega, chunki ular birlashib, millionlab va millionlab ma'lum birikmalarni hosil qiladi.
Element materiyaning asosiy kimyoviy blokidir; bu eng oddiy kimyoviy moddadir. Kimyoviy belgilar moddada mavjud bo'lgan elementlarning qisqa muddatli namoyishi uchun foydalidir.
- Kimyoviy elementni aniqlang va har xil elementlarning ko'pligiga misollar keltiring.
- Kimyoviy elementni kimyoviy belgi bilan ifodalaydi.
- Natriy simob fosforli kaliyli yod.
- Har bir kimyoviy belgi qaysi element bilan ifodalanadi?
- Kardinallik qanday o'zgarganiga bir nechta misollar keltiring.
- Nima uchun kimyoviy belgilar juda foydali?
- Kimyoviy belgining yozuv manbai nima?
- Elementlar atrofimizdagi atomlarning kichik foizidan 30% gacha.
- Harflar odatda element nomidan keladi.
- Barcha materiya elementlardan iborat.
- Kimyoviy elementlar bitta yoki ikkita harfli belgilar bilan ifodalanadi.
- Natriy suvi suyultirilgan azotdir.
"U erda qizil sher bor edi - u kuyov edi,
Va iliq suyuqlikda ular unga toj kiydilar
Chiroyli nilufar bilan ularni olov bilan isitdi,
Va ular kemadan idishga ko'chirildi ... "
(J. V. Gyote, "Faust")
Alkimyogarlar kimyoviy elementlar yulduzlar va sayyoralar bilan bog'liq deb hisobladilar va ularga astrolojik belgilarni tayinladilar. Oltin Quyosh deb nomlangan va nuqta bilan doira bilan belgilangan; mis - Venera, bu metalning ramzi "Venera oynasi", temir esa Mars edi; urush xudosiga yarasha, bu metallning nomi qalqon va nayzani o'z ichiga olgan:
Karbonli beton qog'oz. ... Har bir element uchun kimyoviy belgini yozing. Element element emas, element emas, element emas. ... Odatdagidek element belgisidagi ikkinchi harf har doim kichik harflar bilan yoziladi.
- Qanday qilib barcha moddalar atomlardan iboratligini tushuntiring.
- Hozirgi atom nazariyasini tavsiflab bering.
Parchalar hali ham alyumin folga ekanligi aniq bo'lishi kerak; ular shunchaki kichrayib borishadi. Ammo, hech bo'lmaganda nazariy jihatdan ushbu mashqni qay darajada bajarishingiz mumkin? Siz alyuminiy folga tobora ikkiga bo'laklarga bo'linib, kichikroq va kichikroq bo'laklarni yasashda davom eta olasizmi? Yoki alyumin folga uchun eng kichik, biron bir cheklov bormi?
18-asrda elementlarni belgilash tizimi (shu davrda uch o'nlab kishilarga ma'lum bo'lgan) geometrik shakllar - aylana, yarim doira, uchburchak, kvadrat shaklida ildiz otgan. Kimyoviy moddalarni tasvirlashning bu usuli ingliz olimi, fizigi va kimyogari Jon Dalton tomonidan ixtiro qilingan.
Biroq, kitoblarda va ilmiy jurnallarda turli xil elementlarning kimyoviy belgilarini ajratish juda qiyin edi. Va o'sha paytdagi bosmaxonalarda bosmaxona sifatida ishlash qanday edi! Qanday qilib ular qattiq chiziq bilan chizilgan va markazida bir nuqta bo'lgan uchta kontsentrik doiradan iborat bo'lgan vodorod belgisini kislorod belgisidan - shuningdek uchta kontsentrik doiradan, ulardan biri kesilgan va nuqta bo'lmasdan ajratib olishlari mumkin edi?
Dalton foydalangan kislorod, oltingugurt, vodorod va azotning ramzlari:
Ishga yo'naltirilganligi: Klinik kimyogar
11-rasm Davriy jadvaldagi tendentsiyalar.
Atomlarning nisbiy kattaligi davriy jadval tuzilishiga oid bir necha tendentsiyalarni ko'rsatadi. Atomlar ustundan kattalashib boradi va davr mobaynida kamroq harakatlanadi. Klinik kimyo - bu inson tanasining sog'lig'ini aniqlash uchun tana suyuqligini tahlil qilish bilan bog'liq bo'lgan kimyo sohasi. Klinik kimyogarlar natriy va kaliy kabi oddiy elementlardan tortib, qon, siydik va boshqa tana suyuqliklaridagi oqsil va fermentlar kabi murakkab molekulalargacha bo'lgan moddalarni o'lchaydilar.
 Va nihoyat, 1814 yilda kimyochilar shu kungacha ishlatib kelayotgan kimyoviy elementlarning ramzlari va nomlari paydo bo'ldi. Shvetsiyalik kimyogar Yens-Yakob Berzelius kimyoviy elementlarni elementning lotincha nomining birinchi harfi (yoki birinchi va quyidagi harflardan biri) bilan belgilashni taklif qildi.
Va nihoyat, 1814 yilda kimyochilar shu kungacha ishlatib kelayotgan kimyoviy elementlarning ramzlari va nomlari paydo bo'ldi. Shvetsiyalik kimyogar Yens-Yakob Berzelius kimyoviy elementlarni elementning lotincha nomining birinchi harfi (yoki birinchi va quyidagi harflardan biri) bilan belgilashni taklif qildi.
Masalan, vodorod (lotincha "gidrogenium", Gidrogenium) - N ("kul" ni o'qing), uglerod (lotin tilida "carbononeum", Karbonum) - C, (lotincha "aurum", Aurum) - Au (shuningdek, "aurum" ni o'qing).
Moddaning yo'qligi yoki mavjudligi yoki g'ayritabiiy darajada past yoki yuqori miqdori kasallik yoki sog'liq alomatining belgisi bo'lishi mumkin. Ko'pgina klinik kimyogarlar o'z ishlarida murakkab texnika va murakkab kimyoviy reaktsiyalarni qo'llaydilar, shuning uchun ular nafaqat asosiy kimyo fanini tushunishlari, balki maxsus asboblar va test natijalarini qanday izohlashlari bilan tanishishlari kerak.
Elementlar atom raqami bo'yicha tartiblangan. davriy jadvalning chap uch choragida, davriy jadvalning o'ng choragi davriy jadvalning keyingi so'nggi ustuni - davriy jadvalning o'rta qismi. Davriy sistemadan o'tayotganda atom radiusi kamayadi; davriy jadvalga tushganda, atom radiusi ko'payadi.
Ko'pgina elementlarning ruscha nomlari lotin tilidan mutlaqo farq qiladi, ammo siz nima qila olasiz - kimyoviy belgilar yoddan o'rganiladi, chunki tibbiyot talabalari va bo'lajak shifokorlar lotin atamalarini o'rganadilar.
Barcha belgilar va elementlarning nomlarini birdaniga yodlash (va hozirda ularning 114 tasi ma'lum) imkonsiz vazifa ekanligi aniq. Shuning uchun, siz o'zingizni eng keng tarqalgan narsalar bilan cheklashingiz mumkin:
Elementlarning ayrim xususiyatlari ularning davriy jadvaldagi mavqei bilan bog'liq. Magniyga o'xshash kimyoviy xususiyatlarga ega bo'lgan qaysi elementlar? natriy ftorli kaltsiy bariy selenium. Kimyoviy elementlar davriy jadval deb nomlangan diagramma bo'yicha joylashtirilgan. ... Qaysi elementlar litiyga o'xshash kimyoviy xususiyatlarga ega?
Natriy kaltsiy berilyum bariy kaliy. ... Qaysi elementlar xlorga o'xshash kimyoviy xususiyatlarga ega? Ushbu bobdagi materialni tushunish uchun quyidagi qalin atamalarning ma'nosini ko'rib chiqing va ushbu bobdagi mavzular bilan qanday bog'liqligini o'zingizdan so'rang.
| Ruscha ism | Elementning kimyoviy belgisi va atom raqami | Lotin ism |
Belgining talaffuzi |
| Azot | 7 N | Nitrogenium | uz |
| Alyuminiy | 13 Al | Alyuminiy | alyuminiy |
| Brom | 35 Br | Bromum | brom |
| Vodorod | 1 H | Gidrogenium | kul |
| Geliy | 2 U | Geliy | geliy |
| Temir | 26 Fe | Ferrum | ferrum |
| Oltin | 79 Au | Aurum | aurum |
| Yod | 53 I | Yod | yod |
| Kaliy | 19 K | Kalium | kaliy |
| Kaltsiy | 20 Ca | Kaltsiy | kaltsiy |
| Kislorod | 8 O | Oksigenium | haqida |
| Silikon | 14 Si | Silisium | kremniy |
| Magniy | 12 Mg | Magniy | magniy |
| Mis | 29 Cu | Cuprum | krujka |
| Natriy | 11 Na | Natrium | natriy |
| Qalay | 50 Sn | Stannum | stannum |
| Qo'rg'oshin | 82 Pb | Plumbum | plumbum |
| Oltingugurt | 16 S | Oltingugurt | es |
| Kumush | 47 yosh | Argentum | argentum |
| Uglerod | 6 S | Karbonum | tse |
| Fosfor | 15 p | Fosfor | pe |
| Ftor | 9 F | Fluorum | ftor |
| Xlor | 17 Cl | Chlorum | xlor |
| Xrom | 24 Kr | Xrom | xrom |
| Sink | 30 Zn | Sinkum | rux |
Kimyoviy elementlarning nomlari va ramzlari
§ 4. Kimyoviy belgilar va formulalar
Kimyoda ramziy modellarga kimyoviy elementlarning alomatlari yoki ramzlari, moddalar formulalari va "kimyoviy yozuv" asosida yotadigan kimyoviy reaktsiyalar tenglamalari kiradi. Uning asoschisi shved kimyogari Yens Yakob Berzeliusdir. Berzeliy yozuvi kimyoviy tushunchalardan eng muhimi - "kimyoviy element" ga asoslangan. Kimyoviy element - bu bir xil atomlarning bir turi.
Element bu oddiy kimyoviy moddalarga ajratib bo'lmaydigan moddadir. Faqat 90 ga yaqin tabiiy elementlar ma'lum. Ular Yerda va tanada turli xil mo'lliklarga ega. Har bir element bir yoki ikki harfli kimyoviy belgiga ega. Zamonaviy atom nazariyasi elementning eng kichik qismi atom ekanligini ta'kidlaydi. Alohida atomlar juda kichik, ularning bo'ylab 10 -10 m gacha tartibda. Elementlarning aksariyati sof shaklda individual atomlar sifatida mavjud, ammo ba'zilari diatomik molekulalar sifatida mavjud.
Atomlarning o'zi subatomik zarralardan iborat. Elektron - manfiy zaryadga ega bo'lgan kichik subatomik zarra. Proton musbat zaryadga ega va kichik bo'lsa ham, elektronga qaraganda ancha katta. Neytron ham elektronga qaraganda ancha katta, ammo elektr zaryadi yo'q.
Berzelius kimyoviy elementlarni lotin nomlarining birinchi harfi bilan belgilashni taklif qildi. Shunday qilib, uning lotin nomidagi birinchi harfi kislorodning belgisiga aylandi: kislorod - O ("o" o'qing, chunki ushbu elementning lotincha nomi) oksigenium). Shunga ko'ra, vodorod H belgisini oldi ("ash" ni o'qing, chunki bu elementning lotincha nomi gidrogenium), uglerod - C ("tse" ni o'qing, chunki ushbu elementning lotincha nomi karbonum). Biroq, xromning lotincha nomlari ( xrom), xlor ( chlorum) va mis ( krujka) uglerod bilan bir qatorda, "C" dan boshlang. Qanday bo'lish kerak? Berzelius mohirona echim taklif qildi: birinchi va keyingi harflardan birini, ko'pincha ikkinchisini yozing. Shunday qilib, xrom Cr ("xrom" ni o'qing), xlor - Cl ("xlor" ni o'qing), mis - Cu ("cuprum" ni o'qing) deb belgilanadi.
Protonlar, neytronlar va elektronlar atomda o'ziga xos tartibga ega. Proton va neytronlar atomning markazida, yadroga birlashtirilgan. Elektronlar yadro atrofida loyqa bulutlarda. Har bir element yadrosida xarakterli proton soniga ega. Ushbu protonlar soni elementning atom raqamidir. Element atomlari yadrosida har xil miqdordagi neytronlarga ega bo'lishi mumkin; bunday atomlarga izotoplar deyiladi. Vodorodning ikkita izotopi deyteriy bo'lib, uning yadrosida proton va neytron, tritiyda esa proton va ikkita neytron bor.
Rus va lotin nomlari, 20 ta kimyoviy elementning belgilari va ularning talaffuzi jadvalda keltirilgan. 2018-04-02 121 2.
Bizning jadvalimizda faqat 20 ta element mavjud. Bugungi kunga qadar ma'lum bo'lgan barcha 110 elementni ko'rish uchun D.I.Mendeleyevning kimyoviy elementlari jadvaliga qarash kerak.
2-jadval
Ba'zi kimyoviy elementlarning nomlari va belgilari
|
Ruscha ism Yadrodagi proton va neytronlar sonining yig'indisi massa soni deyiladi va izotoplarni bir-biridan ajratish uchun ishlatiladi. Alohida atomlarning massalari atom massasi birliklari bilan o'lchanadi. Elementning har xil izotoplari har xil massaga ega bo'lganligi sababli, elementning atom massasi bu elementning tabiiy ravishda uchraydigan barcha izotoplarining o'rtacha tortilgan massasi. Elektronlarning xatti-harakatlarining zamonaviy nazariyasi kvant mexanikasi deb ataladi. Ushbu nazariyaga ko'ra, atomlardagi elektronlar faqat o'ziga xos yoki miqdoriy energiyaga ega bo'lishi mumkin. Elektronlar qobiq deb nomlangan umumiy mintaqalarga, ularning ichida esa subhells deb ataladigan aniqroq mintaqalarga guruhlanadi. Subhelllarning to'rt turi mavjud va ularning har bir turi maksimal miqdordagi elektronni o'z ichiga olishi mumkin. Elektronlarning qobiq va pastki qobiqlarda taqsimlanishi atomning elektron konfiguratsiyasi hisoblanadi. Kimyo odatda valentlik qobig'i elektronlari deb ataladigan har xil atomlarning tashqi qobig'ining elektronlari o'rtasidagi o'zaro ta'sirdan kelib chiqadi. |
Kimyoviy belgi |
Talaffuz |
Lotin nomi |
|
Alyuminiy Ichki qobiqdagi elektronlar yadroning elektronlari deyiladi. Elementlar davriy jadval deb nomlangan diagrammada o'xshash kimyoviy xususiyatlariga ko'ra guruhlangan. Elementlarning vertikal ustunlari guruhlar yoki oilalar deb nomlanadi. Elementlarning ayrim guruhlari gidroksidi metallar, ishqoriy er metallari, galogenlar va zo'r gazlar kabi nomlarga ega. Elementlarning gorizontal qatori nuqta deb ataladi. Davrlar va guruhlar tarkibida turli xil sonli elementlar mavjud. Davriy jadval elementlarni metall, metall va yarim metallarga ajratadi. |
Alyuminiy |
||
|
Gidrargirum Davriy jadval shuningdek asosiy guruh elementlari, o'tish metallari, lantanid elementlari va aktinid elementlariga bo'linadi. Lantanid va aktinid elementlari ichki o'tish metall elementlari deb ham ataladi. Davriy jadvalning shakli atomlardagi chig'anoqlar va qobiqlarning ketma-ket to'ldirilishini aks ettiradi. Davriy jadval bizga atomlarning ayrim xususiyatlarining tendentsiyalarini tushunishga yordam beradi. Ushbu xususiyatlardan biri bu atomlarning atom radiusi. Elektronlar katta va katta qobiqlarni egallaganligi sababli davriy jadvalning yuqoridan pastgacha atomlari kattalashadi. Chapdan o'ngga, davriy jadval orqali elektronlar bir xil qobiqni to'ldiradi, ammo yadrodan tobora ortib borayotgan ijobiy zaryad ularni jalb qiladi va shuning uchun atomlar kichrayadi. |
|||
|
Argentum |
|||
Ko'pincha moddalar tarkibiga bir nechta kimyoviy elementlarning atomlari kiradi. Siz avvalgi darsda bo'lgani kabi, to'p modellari yordamida moddaning eng kichik zarrasini, masalan, molekulani tasvirlashingiz mumkin. Shakl. 33-da suv molekulalarining volumetrik modellari tasvirlangan (a), oltingugurt dioksidi (b), metan (ichida) va karbonat angidrid (d).
Atom massasi birliklarida elektronning massasi qanday? Ushbu bobdagi izohda alfa zarrachasi 2 ta proton va 2 neytron bo'lgan zarracha deb ta'riflangan. Alfa zarrachasining massasi necha grammga teng? Afsonaviy dunyoning atom massasi nima? Izotoplarning tarqalishi Quyosh tizimidagi turli sayyoralarda turlicha bo'lganligi sababli har qanday elementning o'rtacha atom massasi sayyoradan sayyoraga farq qiladi. Merkuriyda vodorodning atom massasi qancha? Yana qanday kimyoviy elementlar mavjud?
Va bu savolga javob berish oddiy bo'lsa-da, savollar yanada qiziqroq: biz cheksiz ko'p kimyoviy elementlarni kashf qila olamizmi yoki ular bizga nima xizmat qiladi? Ularning nomlari va ramzlari qanday tanlangan? kimyoviy moddalarmi?
Ko'pincha, kimyogarlar moddani belgilash uchun moddiy modellardan foydalanmaydi, balki ramziy ma'noga ega. Moddalarning formulalari kimyoviy elementlar va indekslarning belgilaridan foydalangan holda yoziladi. Indeksda ma'lum bir elementning qancha atomlari moddaning molekulasiga kiritilganligi ko'rsatilgan. U quyida kimyoviy element belgisining o'ng tomonida yozilgan. Masalan, yuqoridagi moddalarning formulalari quyidagicha yozilgan: H 2 O, SO 2, CH 4, CO 2.
Kimyoviy formula bizning fanimizdagi asosiy ramziy modeldir. Bu kimyogar uchun juda muhim ma'lumotlarni o'z ichiga oladi. Kimyoviy formulada quyidagilar ko'rsatilgan: ma'lum bir modda; ushbu moddaning bitta zarrasi, masalan bitta molekula; sifat tarkibi moddalar, ya'ni elementlari berilgan moddaning bir qismi bo'lgan atomlari; miqdoriy tarkibi, ya'ni har bir elementning qancha atomlari moddaning molekulasiga kiritilgan.
Moddaning formulasi bo'yicha siz uning oddiy yoki murakkabligini ham aniqlashingiz mumkin.
Oddiy moddalar bitta element atomlaridan tashkil topgan moddalar deyiladi. Murakkab moddalar ikki yoki undan ortiq turli xil elementlarning atomlari tomonidan hosil bo'ladi.
Masalan, vodorod H 2, temir Fe, kislorod O 2 oddiy moddalar, suv H 2 O, karbonat angidrid CO 2 va sulfat kislota H 2 SO 4 murakkabdir.
1. Qaysi kimyoviy element belgilarida katta S harfi mavjud? Ularni yozing va ayting.
2. Stoldan. 2 metall elementlar va metall bo'lmagan elementlarning belgilarini alohida yozing. Ularning ismlarini ayting.
3. Kimyoviy formula nima? Quyidagi moddalarning formulalarini yozing:
a) oltingugurt kislotasi, agar uning molekulasida ikkita vodorod, bitta oltingugurt atomi va to'rtta kislorod atomlari borligi ma'lum bo'lsa;
b) molekulasi ikki vodorod atomidan va bitta oltingugurt atomidan iborat vodorod sulfidi;
v) molekulasida bitta oltingugurt atomi va ikkita kislorod atomlari bo'lgan oltingugurt dioksidi.
4. Ushbu moddalarning umumiy jihati nimada?
Plastilindan quyidagi moddalarning molekulalarining hajm modellarini yarating:
a) molekulasida bitta azot atomi va uchta vodorod atomlari bo'lgan ammiak;
b) molekulasi bitta vodorod atomi va bitta xlor atomidan iborat vodorod xlorid;
v) xlor, uning molekulasi ikkita xlor atomidan iborat.
Ushbu moddalar uchun formulalarni yozing va ularni o'qing.
5. Ohak suvi analitik bo'lganida va u reaktiv bo'lganida o'zgarishlarga misollar keltiring.
6. Ovqat tarkibidagi kraxmalni aniqlash uchun uy tajribasini o'tkazing. Buning uchun qanday reaktiv ishlatdingiz?
7. Shakl. 33-rasmda to'rtta kimyoviy moddalarning molekulyar modellari ko'rsatilgan. Ushbu moddalar nechta kimyoviy elementlarni hosil qiladi? Ularning belgilarini yozing va ismlarini ayting.
8. To'rt rangdagi plastilinni oling. Eng kichik oq to'plarni aylantiring - bular vodorod atomlarining modellari, kattaroq ko'k sharlar - kislorod atomlari modellari, qora to'plar - uglerod atomlari modellari va nihoyat, eng katta sariq to'plar - oltingugurt atomlarining modellari. (Albatta, biz aniqlik uchun atomlarning rangini shartli ravishda tanladik.) To'p-atomlardan foydalanib, shaklda ko'rsatilgan molekulalarning uch o'lchovli modellarini tuzing. 33.
; 2) 9-chi sinf... Birinchi qism albatta ... balanddan boshlang qo'llab-quvvatlash bilan ...
"7-sonli umumta'lim maktabi" shahar byudjet ta'lim muassasasining boshlang'ich umumiy ta'limining asosiy ta'lim dasturi
Asosiy ta'lim dasturi...: fizika, kimyo, biologiya, geografiya ... boshlang, s 6.2-6.0 6.7-6.3 7.2-7.0 6.3-6.1 6.9-6.5 7.2-7.0 1000 m vaqt sarflamasdan yugurish 2018-04-02 121 2 SINF ... Dastur albatta Ingliz tilidan "Enjoy English" ga uchun 2 - 9 o'quvchilar sinflar umumiy ta'lim muassasalar. ...
Samara viloyati davlat byudjet ta'limi muassasasining ochiq hisoboti (1)
Ommaviy hisobot... . Kimyo 8-11 sinf. Dastur albatta kimyo uchun 8-11 sinflar umumiy ta'lim muassasalar./ muallif E.E.Minchenkov, T.V.Smirnova, L.A.Tsvetkov. M.: Bustard, 2008 yil. Kimyo.8-dars sinf ..., piyoda yurish, “Merry boshlanadi", Ochiq sport turlari ...
"Matematika. 2-sinf" kursi bo'yicha uslubiy tavsiyalar / Arginskaya I. I., Kormishina S. N Samara: "Uchebnaya literatura" nashriyoti: "Fedorov" nashriyoti, 2012.336 b. (Dasturlar va rejalashtirish) Nusxalari: jami: 2 sosh3 (2)
Ko'rsatmalarIsh daftariga tavsiyalar «Maktab boshlang". Soroko-Tsyupa AO. 27. Gabrielyan OS dasturi albatta kimyo uchun 8-11 sinflar umumiy ta'lim muassasalar/ Gabrielyan O.S. - M.: Bustard, 2011. ...







