Во живата клетка, протокот на информации помеѓу јадрото и цитоплазмата никогаш не пресушува, но разбирањето на сите негови „вртења“ и дешифрирањето на информациите кодирани во неа е навистина херкулова задача. Еден од најважните откритија во биологијата од минатиот век може да се смета за откривање на информациски (или матрични) молекули на РНК (мРНК или мРНК), кои служат како посредници кои носат информациски „пораки“ од јадрото (од хромозомите) до цитоплазмата. . Одлучувачката улога на РНК во синтезата на протеини беше предвидена уште во 1939 година во работата на Торбјорн Касперсон ( Торбјорн Касперсон), Жан Браше ( Жан Браше) и Џек Шулц ( Џек Шулц), а во 1971 година Џорџ Марбеис ( Џорџ Марбе) ја активираше синтезата на хемоглобинот во ооцитите од жаба со инјектирање на првата изолирана РНК гласник на зајаци што го кодира овој протеин.
Во 1956-1957 година во Советскиот Сојуз, А.Н. Белозерски и А.С. Спирин независно го докажаа постоењето на mRNA, а исто така открија дека најголемиот дел од РНК во клетката не е шаблон, туку рибозомална РНК(rRNA). Рибозомална РНК - вториот „главен“ тип на клеточна РНК - го формира „скелетот“ и функционалниот центар на рибозомите кај сите организми; Тоа е rRNA (а не протеини) што ги регулира главните фази на синтезата на протеините. Во исто време, беше опишан и проучен третиот „главен“ тип на РНК - преносни РНК (tRNA), кои во комбинација со две други - mRNA и rRNA - формираат единствен комплекс за синтеза на протеини. Според прилично популарната хипотеза „светот на РНК“, токму оваа нуклеинска киселина лежи во самото потекло на животот на Земјата.
Поради фактот што РНК е значително похидрофилна во споредба со ДНК (поради замената на деоксирибозата со рибоза), таа е полабилна и може релативно слободно да се движи во клетката, па затоа испорачува краткотрајни реплики генетски информации(mRNA) до местото каде што започнува синтезата на протеините. Сепак, вреди да се забележи „непријатноста“ поврзана со ова - РНК е многу нестабилна. Таа е многу полошо складирана од ДНК (дури и внатре во клетката) и се деградира при најмала промена на условите (температура, pH). Покрај „својата“ нестабилност, огромен придонесприпаѓа на рибонуклеази (или RNases) - класа на ензими за расцепување на РНК кои се многу стабилни и „сеприсутни“ - дури и кожата на рацете на експериментаторот содржи доволно од овие ензими за да го негира целиот експеримент. Поради ова, работата со РНК е многу потешка отколку со протеините или ДНК - вторите генерално може да се складираат стотици илјади години без практично никакво оштетување.
Фантастична грижа за време на работата, три-дестилат, стерилни ракавици, лабораториски стакларија за еднократна употреба - сето тоа е неопходно за да се спречи деградација на РНК, но одржувањето на таквите стандарди не беше секогаш можно. Затоа, долго време, тие едноставно не обрнуваа внимание на кратките „фрагменти“ на РНК, кои неизбежно ги контаминираа растворите. Меѓутоа, со текот на времето, стана јасно дека, и покрај сите напори да се одржи стерилноста на работната површина, природно продолжи да се откриваат „остатоци“, а потоа се покажа дека илјадници кратки двоверижни РНК секогаш се присутни во цитоплазмата. , извршуваат многу специфични функции и се апсолутно неопходни за нормален развој на клетките и организмот.
Принцип на интерференција на РНК
Фармацевтите исто така се заинтересираа за можноста за користење на siRNA, бидејќи способноста за специфично регулирање на функционирањето на поединечни гени ветува невидени изгледи во лекувањето на низа болести. Малата големина и високата специфичност на дејството ветуваат висока ефикасност и ниска токсичност на лековите базирани на siRNA; сепак реши го проблемот испорака siRNA за заболените клетки во телото сè уште не е успешна - ова се должи на кревкоста и кревкоста на овие молекули. И иако десетици тимови сега се обидуваат да најдат начин да ги насочат овие „магични куршуми“ точно кон целта (внатре во заболените органи), тие сè уште не постигнале видлив успех. Покрај ова, има и други тешкотии. На пример, во случај на антивирусна терапија, високата селективност на дејството на siRNA може да биде лоша услуга - бидејќи вирусите брзо мутираат, модифицираниот вид многу брзо ќе ја изгуби чувствителноста на siRNA избрана на почетокот на терапијата: познато е дека заменувањето на само еден нуклеотид во siRNA води до значително намалување на интерферентниот ефект.
Во овој момент вреди да се потсетиме повторно - откриени се siRNAs само кај растенијата, безрбетниците и едноклеточните организми; Иако хомолози на протеини за интерференција на РНК (Dicer, RISC комплекс) се исто така присутни кај виши животни, siRNA не беа откриени со конвенционални методи. Какво изненадување беше кога вештачки воведенсинтетичките аналози на siRNA предизвикаа силен специфичен дозно зависен ефект во клеточни култури на цицачи! Ова значеше дека во клетките на 'рбетниците, РНК интерференцијата повеќе не беше заменета комплексни системиимунитет, но еволуираше заедно со организмите, претворајќи се во нешто „понапредно“. Следствено, кај цицачите беше неопходно да не се бараат точни аналози на siRNA, туку нивните еволутивни наследници.
Играч #2 - микроРНК
Навистина, врз основа на еволутивно прилично античкиот механизам на интерференција на РНК, кај поразвиените организми се појавија два специјализирани системи за контролирање на работата на гените, секој користејќи своја група мали РНК - микроРНК(микроРНК) и пиРНК(пиРНК, РНК со интеракција со Пиви). И двата системи се појавија во сунѓери и колентерати и еволуираа заедно со нив, поместувајќи ја сиРНК и механизмот на „гола“ интерференција на РНК. Нивната улога во обезбедувањето имунитет се намалува, бидејќи оваа функција е преземена од понапредните механизми на клеточниот имунитет, особено интерферонскиот систем. Сепак, овој систем е толку чувствителен што ја активира и самата siRNA: појавата на мала двоверижна РНК во клетка на цицач предизвикува „алармен сигнал“ (го активира лачењето на интерферон и предизвикува изразување на гени зависни од интерферон, кои целосно ги блокира сите процеси на превод). Во овој поглед, механизмот на интерференција на РНК кај повисоките животни е посредуван главно од микроРНК и пиРНК - едноверижни молекули со специфична структура кои не се откриени од системот на интерферон.
Како што геномот стана покомплексен, микроРНК и пиРНК се повеќе се вклучени во регулирањето на транскрипцијата и транслацијата. Со текот на времето, тие се претворија во дополнителен, прецизен и суптилен систем на регулација на геномот. За разлика од siRNA, микроРНК и пиРНК (откриени во 2001 година, види Поле 3) не се произведуваат од туѓи двоверижни молекули на РНК, туку првично се кодирани во геномот на домаќинот.
Запознајте: микроРНК
Претходникот на микроРНК е транскрибиран од двете нишки на геномната ДНК со РНК полимераза II, што резултира со појава на средна форма - при-микроРНК - која ги носи карактеристиките на обичната мРНК - m7 G-капа и полиА опашка. Овој претходник формира јамка со две едножилни „опашки“ и неколку неспарени нуклеотиди во центарот (сл. 3). Таквата јамка се подложува на обработка во две фази (сл. 4): прво, ендонуклеазата Дроша ги отсекува едноверижните „опашки“ на РНК од шнолата, по што исечената фиба (пред-микроРНК) се извезува во цитоплазмата, каде што е препознаен од Dicer, кој прави уште две резови (се отсекува двожичен пресек, означен со боја на слика 3). Во оваа форма, зрелата микроРНК, слична на siRNA, е вклучена во комплексот RISC.
Слика 3. Структура на двоверижна прекурсорска молекула на микроРНК.Главни карактеристики: присуство на зачувани секвенци кои формираат фиба; присуство на комплементарна копија (микроРНК*) со два „екстра“ нуклеотиди на крајот од 3'; специфична секвенца (2-8 bp) која формира место за препознавање на ендонуклеази. Самата микроРНК е означена со црвено - ова го отсекува Dicer.
Механизмот на дејство на многу микроРНК е сличен на дејството на siRNA: кратка (21-25 нуклеотиди) едноверижна РНК како дел од протеинскиот комплекс RISC се врзува со висока специфичност за комплементарното место во 3' непреведениот регион на целна мРНК. Врзувањето доведува до расцепување на mRNA од протеинот Аго. Сепак, активноста на микроРНК (во споредба со сиРНК) е веќе подиференцирана - ако комплементарноста не е апсолутна, целната мРНК можеби нема да се разградува, туку само реверзибилно блокирана (нема да има транслација). Може да се користи и истиот комплекс RISC вештачки воведен siRNA. Ова објаснува зошто siRNA направени по аналогија со протозои се активни и кај цицачите.
Така, можеме да ја надополниме илустрацијата за механизмот на дејство на интерференцијата на РНК кај повисоките (билатерално симетрични) организми со комбинирање на една слика на акциониот дијаграм на микроРНК и биотехнолошки воведените siRNA (сл. 5).

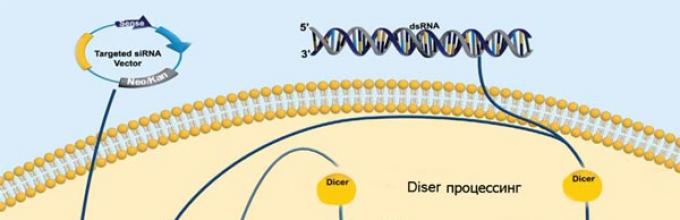
Слика 5. Генерализирана шема на дејство на вештачките микроРНК и сиРНК(вештачки siRNA се внесуваат во клетката со помош на специјализирани плазмиди - таргетирање на вектор siRNA).
Функции на микроРНК
Физиолошките функции на микроРНК се исклучително разновидни - всушност, тие дејствуваат како главни непротеински регулатори на онтогенезата. микроРНК не се откажуваат, туку ја надополнуваат „класичната“ шема на генска регулација (индуктори, супресори, набивање на хроматин, итн.). Покрај тоа, синтезата на самите микроРНК е сложено регулирана (одредени базени на микроРНК може да се вклучат со интерферони, интерлеукини, фактор на туморска некроза α (TNF-α) и многу други цитокини). Како резултат на тоа, се појавува мрежа на повеќе нивоа на подесување на „оркестар“ од илјадници гени, неверојатна по својата сложеност и флексибилност, но ова не завршува тука.
микроРНК се повеќе „универзални“ од siRNA: гените „одделенија“ не мора да бидат 100% комплементарни - регулацијата исто така се спроведува преку делумна интеракција. Денес една од најжешките теми во молекуларна биологија- пребарување на микроРНК кои делуваат како алтернативни регулатори на познатите физиолошки процеси. На пример, микроРНК вклучени во регулирањето на клеточниот циклус и апоптозата кај растенијата, Drosophila и нематодите веќе се опишани; кај луѓето, микроРНК го регулираат имунолошкиот систем и развојот на хематопоетски матични клетки. Употребата на технологии засновани на биочипови (скрининг со микро низа) покажа дека цели групи на мали РНК се вклучуваат и исклучуваат во различни фази од животот на клетките. За биолошки процесиидентификувани десетици специфични микроРНК, чие ниво на изразување под одредени услови се менува илјадници пати, нагласувајќи ја исклучителната контролираност на овие процеси.
До неодамна се веруваше дека микроРНК само ја потиснуваат - целосно или делумно - работата на гените. Сепак, неодамна се покажа дека дејството на микроРНК може радикално да се разликува во зависност од состојбата на клетката! Во клетка која активно се дели, микроРНК се врзува за комплементарна секвенца во 3' регионот на mRNA и ја инхибира синтезата на протеини (превод). Меѓутоа, во состојба на одмор или стрес (на пример, кога растете во лоша средина), истиот настан доведува до сосема спротивен ефект - зголемена синтеза на целниот протеин!
Еволуција на микроРНК
Бројот на сорти на микроРНК во повисоките организми сè уште не е целосно утврден - според некои податоци, тој надминува 1% од бројот на гени кои кодираат протеини (кај луѓето, на пример, велат дека има 700 микроРНК, а овој број е постојано расте). микроРНК ја регулираат активноста на околу 30% од сите гени (целите за многу од нив сè уште не се познати), а има и сеприсутни и ткивни специфични молекули - на пример, еден таков важен базен на микроРНК го регулира созревањето на стеблото на крвта клетки.
Широк изразен профил во различни ткива различни организмии биолошкото изобилство на микроРНК сугерира еволутивно античко потекло. МикроРНК за првпат биле откриени во нематоди, и долго време се верувало дека овие молекули се појавуваат само во сунѓери и колентерати; сепак, подоцна биле откриени во едноклеточни алги. Интересно, како што организмите стануваат посложени, бројот и хетерогеноста на базенот на miRNA исто така се зголемува. Ова индиректно укажува дека сложеноста на овие организми е обезбедена, особено, преку функционирањето на микроРНК. Можната еволуција на miRNA е прикажана на Слика 6.

Слика 6. Разновидност на микроРНК кај различни организми.Колку е поголема организацијата на организмот, толку повеќе микроРНК се наоѓаат во него (бројот во загради). Видовите во кои се пронајдени се означени со црвено. синглмикроРНК.
Може да се направи јасна еволутивна врска помеѓу siRNA и microRNA, врз основа на следните факти:
- дејството на двата типа е заменливо и е посредувано од хомологни протеини;
- siRNAs внесени во клетките на цицачите конкретно ги „исклучуваат“ саканите гени (и покрај одредено активирање на заштитата од интерферон);
- микроРНК се откриваат во се повеќе антички организми.
Овие и други податоци укажуваат на потеклото на двата системи од заеднички „предок“. Исто така, интересно е да се забележи дека имунитетот на „РНК“ како независен претходник на протеинските антитела ја потврдува теоријата за потеклото на првите форми на живот засновани на РНК, а не на протеини (да потсетиме дека ова е омилената теорија на академик А.С. Спирин). .
Колку подалеку одите, толку повеќе станува збунувачки. Играч #3 - пиРНК
Додека имаше само двајца „играчи“ во арената на молекуларната биологија - siRNA и microRNA - главната „цел“ на интерференцијата на РНК изгледаше сосема јасна. Навистина: збир на хомологни кратки РНК и протеини во различни организми извршуваат слични дејства; Како што организмите стануваат покомплексни, така се зголемува и функционалноста.
Меѓутоа, во процесот на еволуција, природата создала друг, еволутивно најнов и високо специјализиран систем заснован на истиот успешен принцип на интерференција на РНК. Зборуваме за пиРНК (пиРНК, од РНК со интеракција на пиви).
Колку е покомплексен геномот организиран, толку е поразвиен и поадаптиран организмот (или обратно? ;-). Сепак, зголемувањето на сложеноста на геномот има и негативна страна: станува сложен генетски систем нестабилна. Ова доведува до потреба од механизми одговорни за одржување на интегритетот на геномот - инаку спонтано „мешање“ на ДНК едноставно ќе го оневозможи. Мобилни генетски елементи ( MGE) - еден од главните фактори за нестабилност на геномот - се кратки нестабилни региони кои можат автономно да се транскрибираат и да мигрираат низ геномот. Активирањето на таквите транспонирани елементи доведува до повеќекратни прекини на ДНК во хромозомите, што може да има смртоносни последици.
Бројот на MGE се зголемува нелинеарно со големината на геномот и нивната активност мора да биде содржана. За да го направите ова, животните, почнувајќи од колентератите, го користат истиот феномен на интерференција на РНК. Оваа функција ја вршат и кратки РНК, но не оние за кои веќе се дискутираше, туку трет тип од нив - пиРНК.
„Портрет“ на пиРНК
Функции на пиРНК
Главната функција на пиРНК е да ја потисне активноста на MGE на ниво на транскрипција и транслација. Се верува дека пиРНК се активни само за време на ембриогенезата, кога непредвидливото мешање на геномот е особено опасно и може да доведе до смрт на ембрионот. Ова е логично - кога имунолошкиот систем сè уште не почнал да работи, на клетките на ембрионот им е потребна едноставна, но ефикасна заштита. Ембрионот е сигурно заштитен од надворешни патогени со плацентата (или лушпата од јајцето). Но, покрај ова, неопходна е и одбрана од ендогени (внатрешни) вируси, првенствено MGE.
Оваа улога на пиРНК е потврдена со искуство - „нокаут“ или мутации на гените Ago3, Piwi или Aub доведуваат до сериозни развојни нарушувања (и нагло зголемување на бројот на мутации во геномот на таков организам), а исто така предизвикуваат неплодност поради нарушување на развојот на герминативните клетки.
Дистрибуција и еволуција на пиРНК
Првите пиРНК веќе се наоѓаат во морските анемони и сунѓери. Растенијата очигледно тргнаа по поинаков пат - во нив не беа пронајдени протеини од Piwi, а улогата на „муцка“ за транспозоните ја вршат ендонуклеазата Ago4 и siRNA.
Кај повисоките животни - вклучително и луѓето - системот на пиРНК е многу добро развиен, но може да се најде само во ембрионските клетки и во амнионскиот ендотел. Зошто дистрибуцијата на пиРНК во телото е толку ограничена, останува да се види. Може да се претпостави дека, како и секоја моќно оружјепиРНК се корисни само под многу специфични услови (за време на феталниот развој), а кај возрасното тело нивната активност ќе предизвика повеќе штета отколку корист. Сепак, бројот на пиРНК е поредок поголем од бројот на познати протеини, а неспецифичните ефекти на пиРНК во зрелите клетки е тешко да се предвидат.
| siRNA | микроРНК | пиРНК | |
|---|---|---|---|
| Ширење | Растенија, Дрософила, C. elegans. Не се наоѓа кај 'рбетниците | Еукариоти | Ембрионски клетки на животни (почнувајќи со колентерати). Не во протозои и растенија |
| Должина | 21-22 нуклеотиди | 19-25 нуклеотиди | 24-30 нуклеотиди |
| Структура | Двојно-верижна, 19 комплементарни нуклеотиди и два неспарени нуклеотиди на крајот од 3' | Комплексна структура со еден синџир | Комплексна структура со еден синџир. U на 5′ крај, 2′ крај О-метилиран 3' крај |
| Обработка | Dicer-зависен | Dicer-зависен | Dicer-независен |
| Ендонуклеази | Пред 2 | Аго1, Аго2 | Ago3, Piwi, Aub |
| Активност | Деградација на комплементарни mRNA, ацетилација на геномната ДНК | Деградација или инхибиција на транслацијата на целната mRNA | Деградација на мРНК што го кодира МГЕ, регулирање на транскрипцијата на МГЕ |
| Биолошка улога | Антивирусна имунолошка одбрана, потиснување на активноста на сопствените гени | Регулирање на генската активност | Сузбивање на активноста на MGE за време на ембриогенезата |
Заклучок
Како заклучок, би сакал да дадам табела која ја илустрира еволуцијата на протеинскиот апарат вклучен во интерференцијата на РНК (сл. 9). Може да се види дека протозоите имаат најразвиен siRNA систем (протеински семејства Ago, Dicer), и како што организмите стануваат посложени, акцентот се префрла на поспецијализирани системи - бројот на протеински изоформи за микроРНК (Дроша, Паша) и пиРНК ( Piwi, Hen1) се зголемува. Во исто време, разновидноста на ензимите кои посредуваат во дејството на siRNA се намалува.

Слика 9. Разновидност на протеини вклучени во интерференција на РНК(броевите го означуваат бројот на протеини од секоја група). Синасе истакнуваат елементите карактеристични за siRNA и microRNA и црвено- протеин Иповрзани со пиРНК.
Феноменот на интерференција на РНК почна да се користи од наједноставните организми. Врз основа на овој механизам, природата создаде прототип имунолошки системи како што организмите стануваат покомплексни, интерференцијата на РНК станува незаменлив регулатор на активноста на геномот. Два различни механизми плус три типа кратки РНК ( цм.таб. 1) - како резултат на тоа, гледаме илјадници фини регулатори на различни метаболички и генетски патишта. Оваа впечатлива слика ја илустрира разновидноста и еволутивната адаптација на молекуларната биолошки системи. Кратките РНК повторно докажуваат дека нема „мали нешта“ во клетката - има само мали молекули, целосното значење на чија улога само што почнуваме да го разбираме.
(Точно, таквата фантастична сложеност повеќе сугерира дека еволуцијата е „слепа“ и дејствува без однапред одобрена „ мастер план» »;
Метафората што лежи во основата на името на феноменот на интерференција на РНК се однесува на експериментот со петунија, кога вештачки внесените гени на розова и виолетова пигментна синтетаза во растението не го зголемија интензитетот на бојата, туку, напротив, го намалија. Слично на тоа, во „обични“ пречки, суперпозицијата на два бранови може да доведе до меѓусебно „откажување“.
Во живата клетка, протокот на информации помеѓу јадрото и цитоплазмата никогаш не пресушува, но разбирањето на сите негови „вртења“ и дешифрирањето на информациите кодирани во неа е навистина херкулова задача. Еден од најважните откритија во биологијата од минатиот век може да се смета за откривање на информациски (или матрични) молекули на РНК (мРНК или мРНК), кои служат како посредници кои носат информациски „пораки“ од јадрото (од хромозомите) до цитоплазмата. . Одлучувачката улога на РНК во синтезата на протеините беше предвидена уште во 1939 година во работата на Торбјорн Касперсон, Жан Браше и Џек Шулц, а во 1971 година Џорџ Марбе ја започна синтезата на хемоглобин во ооцити жаби со инјектирање на првиот изолиран зајачки протеин кој го пренесува РНК. .
Во 1956-57 година, во Советскиот Сојуз, А.Н. Белозерски и А. Рибозомалната РНК, вториот „главен“ тип на клеточна РНК, го формира „скелетот“ и функционалниот центар на рибозомите кај сите организми; Тоа е rRNA (а не протеини) што ги регулира главните фази на синтезата на протеините. Во исто време, беше опишан и проучен третиот „главен“ тип на РНК - преносни РНК (tRNA), кои во комбинација со две други - mRNA и rRNA - формираат единствен комплекс за синтеза на протеини. Според прилично популарната хипотеза „светот на РНК“, токму оваа нуклеинска киселина лежи во самото потекло на животот на Земјата.
Поради фактот што РНК е многу похидрофилна во споредба со ДНК (поради замената на деоксирибозата со рибоза), таа е полабилна и може релативно слободно да се движи во клетката и затоа дава краткотрајни реплики на генетски информации (mRNA) до местото каде што започнува синтезата на протеините. Сепак, вреди да се забележи „непријатноста“ поврзана со ова - РНК е многу нестабилна. Таа е многу полошо складирана од ДНК (дури и внатре во клетката) и се деградира при најмала промена на условите (температура, pH). Покрај „сопствената“ нестабилност, голем придонес имаат рибонуклеазите (или RNases) - класа на ензими за расцепување на РНК кои се многу стабилни и „сеприсутни“ - дури и кожата на рацете на експериментаторот содржи доволно од овие ензими за да ги негира целиот експеримент. Поради ова, работата со РНК е многу потешка отколку со протеините или ДНК - вторите генерално може да се складираат стотици илјади години без практично никакво оштетување.
Фантастична грижа за време на работата, тридистилат, стерилни ракавици, лабораториски стакларија за еднократна употреба - сето тоа е неопходно за да се спречи деградација на РНК, но одржувањето на таквите стандарди не беше секогаш можно. Затоа, долго време, тие едноставно не обрнуваа внимание на кратките „фрагменти“ на РНК, кои неизбежно ги контаминираа растворите. Меѓутоа, со текот на времето, стана јасно дека, и покрај сите напори да се одржи стерилноста на работната површина, природно продолжи да се откриваат „остатоци“, а потоа се покажа дека илјадници кратки двоверижни РНК секогаш се присутни во цитоплазмата. , извршуваат многу специфични функции и се апсолутно неопходни за нормален развој на клетките и организмот.
Принцип на интерференција на РНК
Денес, проучувањето на малите регулаторни РНК е една од најбрзо развиваните области на молекуларната биологија. Откриено е дека сите кратки РНК ги извршуваат своите функции врз основа на феноменот наречен РНК интерференција (суштината на овој феномен е потиснување на генската експресија во фазата на транскрипција или транслација со активно учество на мали молекули на РНК). Механизмот на интерференција на РНК е прикажан многу шематски на Сл. 1:
Ориз. 1. Основи на РНК интерференција
Двоверижните молекули на РНК (dsRNA) се невообичаени во нормалните клетки, но тие се суштински чекор во животниот циклус на многу вируси. Специјален протеин наречен Dicer, откако откри dsRNA во клетката, ја „сече“ на мали фрагменти. Антисенсната влакно на таков фрагмент, која веќе може да се нарече кратка интерферентна РНК (siRNA, од siRNA - мала интерферентна РНК), е врзана со комплекс од протеини наречени RISC (РНК-индуциран комплекс за замолчување), чиј централен елемент е ендонуклеаза од семејството Аргонаут. Врзувањето за siRNA го активира RISC и предизвикува пребарување во клетката за молекули на ДНК и РНК кои се комплементарни на „шаблонот“ siRNA. Судбината на таквите молекули е да бидат уништени или деактивирани од комплексот RISC.
Да резимираме, кратките „пресеци“ на туѓа (вклучувајќи намерно воведена) двоверижна РНК служат како „шаблон“ за големо пребарување и уништување на комплементарната mRNA (и ова е еквивалентно на потиснување на изразувањето на соодветниот ген) , не само во една ќелија, туку и во соседните. За многу организми - протозои, мекотели, црви, инсекти, растенија - овој феномен е еден од главните начини на имунолошка одбрана од инфекции.
Во 2006 година, Ендрју Фајр и Крег Мело добија Нобелова наградапо физиологија и медицина „За откривање на феноменот на интерференција на РНК - механизмот на замолчување на гените со учество на dsRNA“. Иако самиот феномен на интерференција на РНК беше опишан многу порано (на почетокот на 1980-тите), тоа беше дело на Фајр и Мело во општ прегледго утврди регулаторниот механизам на малите РНК и наведе дотогаш непозната област на молекуларно истражување. Еве ги главните резултати од нивната работа:
- За време на интерференцијата на РНК, мРНК (и ниедна друга) се расцепува;
- Двоверижна РНК делува (предизвикува расцеп) многу поефикасно од едноверижна РНК. Овие две набљудувања го предвидоа постоењето на специјализиран систем кој посредува во дејството на dsRNA;
- dsRNA, комплементарна на дел од зрела mRNA, предизвикува расцепување на второто. Ова укажува на цитоплазматска локализација на процесот и присуство на специфична ендонуклеаза;
- Мала количина на dsRNA (неколку молекули по клетка) е доволна за целосно „исклучување“ на целниот ген, што укажува на постоење на каскаден механизам на катализа и/или засилување.
Овие резултати ја поставија основата за цела област на модерната молекуларна биологија - интерференција на РНК - и го одреди векторот на работа на многу истражувачки групи низ светот со децении. До денес, откриени се три големи групи на мали РНК кои играат на молекуларното поле како „тим за интерференција на РНК“. Ајде да ги запознаеме подетално.
Играч #1 – кратка интерферентна РНК
Специфичноста на интерференцијата на РНК се одредува со кратки интерферентни РНК (siRNA) - мали двоверижни РНК молекули со јасно дефинирана структура (види Сл. 2).
siRNA се најраните во еволуцијата и се најраспространети кај растенијата, едноклеточните организми и безрбетниците. Кај 'рбетниците, практично не се наоѓаат siRNAs, бидејќи тие беа заменети со подоцнежни „модели“ на кратки РНК (види подолу).
siRNA - „шаблони“ за пребарување во цитоплазмата и уништување на мРНК молекули - имаат должина од 20-25 нуклеотиди и „посебна карактеристика“: 2 неспарени нуклеотиди на 3' краевите и фосфорилирани 5' краеви. Антисмислената siRNA е способна (се разбира, не сама по себе, туку со помош на комплексот RISC) да ја препознае mRNA и конкретно да предизвика нејзина деградација: целната mRNA е исечена на точното место комплементарно на 10-тиот и 11-тиот нуклеотиди на анти-смислен siRNA синџир.

Ориз. 2. Механизам на „интерференција“ помеѓу mRNA и siRNA
Кратките молекули на РНК кои „попречуваат“ можат или да навлезат во клетката однадвор или да бидат „отсечени“ на место од подолгата двоверижна РНК. Главниот протеин потребен за сечење на dsRNA е Dicer ендонуклеазата. „Исклучувањето“ на генот со механизмот за интерференција го врши siRNA заедно со протеинскиот комплекс RISC, кој се состои од три протеини - ендонуклеазата Ago2 и два помошни протеини PACT и TRBP. Подоцна беше откриено дека комплексите Dicer и RISC можат да користат како „семе“ не само dsRNA, туку и едноверижна РНК што формира двоверижна фиба, како и готова siRNA (последната го заобиколува „сечењето“ фаза и веднаш се врзува за RISC).
Функциите на siRNA во клетките на безрбетниците се доста разновидни. Првата и главната работа е имунолошка заштита. „Традиционалниот“ имунолошки систем (лимфоцити + леукоцити + макрофаги) е присутен само во сложени повеќеклеточни организми. Кај едноклеточните организми, безрбетниците и растенијата (кои или немаат таков систем или е во повој), имунолошката одбрана се заснова на интерференција на РНК. Имунитетот базиран на интерференција на РНК не бара сложени органи за „тренинг“ за прекурсори на имуните клетки (слезина, тимус); во исто време, разновидноста на теоретски можните кратки РНК секвенци (421 варијанта) е во корелација со бројот на можни протеински антитела на вишите животни. Дополнително, siRNA се синтетизираат врз основа на „непријателската“ РНК што ја инфицирала клетката, што значи, за разлика од антителата, тие веднаш се „прилагодени“ за специфичен тип на инфекција. И иако заштитата базирана на интерференција на РНК не функционира надвор од клетката (барем, сè уште нема такви податоци), таа обезбедува интрацелуларен имунитет повеќе од задоволително.
Пред сè, siRNA создава антивирусен имунитет со уништување на mRNA или геномска РНК на заразни организми (на пример, вака се откриени siRNAs кај растенијата). Воведувањето на вирусна РНК предизвикува моќно засилување на специфичните siRNA врз основа на молекулата на прајмерот - самата вирусна РНК. Покрај тоа, siRNA го потиснува изразот на различни мобилни генетски елементи (MGEs), и затоа обезбедува заштита од ендогени „инфекции“. Мутациите во гените на комплексот RISC често доведуваат до зголемена нестабилност на геномот поради високата активност на MGE; siRNA може да дејствува како ограничувач на изразувањето на сопствените гени, предизвикувајќи како одговор на нивната прекумерна експресија. Регулирањето на функцијата на генот може да се случи не само на ниво на транслација, туку и за време на транскрипцијата - преку метилација на гените кај хистон H3.
Во модерната експериментална биологија, важноста на интерференцијата на РНК и кратките РНК тешко може да се прецени. Развиена е технологија за „исклучување“ (или соборување) на поединечни гени in vitro (на клеточни култури) и in vivo (на ембриони), што веќе стана де факто стандард при проучување на кој било ген. Понекогаш, дури и за да се утврди улогата на поединечните гени во некој процес, тие систематски ги „исклучуваат“ сите гени по ред.
Фармацевтите исто така се заинтересираа за можноста за користење на siRNA, бидејќи способноста за специфично регулирање на функционирањето на поединечни гени ветува невидени изгледи во лекувањето на низа болести. Малата големина и високата специфичност на дејството ветуваат висока ефикасност и ниска токсичност на лековите базирани на siRNA; Сепак, сè уште не е можно да се реши проблемот со испорака на siRNA до заболените клетки во телото - ова се должи на кревкоста и кревкоста на овие молекули. И иако десетици тимови сега се обидуваат да најдат начин да ги насочат овие „магични куршуми“ точно кон целта (внатре во заболените органи), тие сè уште не постигнале видлив успех. Покрај ова, има и други тешкотии. На пример, во случај на антивирусна терапија, високата селективност на дејството на siRNA може да биде лоша услуга - бидејќи вирусите брзо мутираат, модифицираниот вид многу брзо ќе ја изгуби чувствителноста на siRNA избрана на почетокот на терапијата: познато е дека заменувањето на само еден нуклеотид во siRNA води до значително намалување на интерферентниот ефект.
Во овој момент вреди да се потсетиме уште еднаш - siRNAs беа пронајдени само кај растенијата, безрбетниците и едноклеточните организми; Иако хомолози на протеини за интерференција на РНК (Dicer, RISC комплекс) се исто така присутни кај виши животни, siRNA не беа откриени со конвенционални методи. Какво изненадување беше кога вештачки воведените синтетички аналози на siRNA предизвикаа силен специфичен ефект зависен од дозата во клеточните култури на цицачи! Ова значеше дека во клетките на 'рбетниците, интерференцијата на РНК не беше заменета со посложени имунолошки системи, туку еволуираше заедно со организмите, претворајќи се во нешто „понапредно“. Следствено, кај цицачите беше неопходно да не се бараат точни аналози на siRNA, туку нивните еволутивни наследници.
Играч #2 – микроРНК
Навистина, врз основа на еволутивно античкиот механизам на интерференција на РНК, поразвиените организми развија два специјализирани системи за контролирање на работата на гените, секој користејќи своја група мали РНК - микроРНК и пиРНК (РНК со интеракција со Пиви). И двата системи се појавија во сунѓери и колентерати и еволуираа заедно со нив, поместувајќи ја сиРНК и механизмот на „гола“ интерференција на РНК. Нивната улога во обезбедувањето имунитет се намалува, бидејќи оваа функција е преземена од понапредните механизми на клеточниот имунитет, особено интерферонскиот систем. Сепак, овој систем е толку чувствителен што ја активира и самата siRNA: појавата на мала двоверижна РНК во клетка на цицач предизвикува „алармен сигнал“ (го активира лачењето на интерферон и предизвикува изразување на гени зависни од интерферон, кои целосно ги блокира сите процеси на превод). Во овој поглед, механизмот на интерференција на РНК кај повисоките животни е посредуван главно од микроРНК и пиРНК - едноверижни молекули со специфична структура кои не се откриени од системот на интерферон.
Како што геномот стана покомплексен, микроРНК и пиРНК се повеќе се вклучени во регулирањето на транскрипцијата и транслацијата. Со текот на времето, тие се претворија во дополнителен, прецизен и суптилен систем на регулација на геномот. За разлика од сиРНК, микроРНК и пиРНК (откриени во 2001 г., види Сл. 3, А-Б) не се произведуваат од туѓи двоверижни РНК молекули, туку првично се кодирани во геномот на организмот домаќин.
Претходникот на микроРНК е транскрибиран од двете нишки на геномната ДНК со РНК полимераза II, што резултира со појава на средна форма - при-микроРНК - што ги носи карактеристиките на редовна мРНК - капа од m7G и опашка од полиА. Овој претходник формира јамка со две едножилни „опашки“ и неколку неспарени нуклеотиди во центарот (сл. 3А). Таквата јамка се подложува на обработка во две фази (сл. Б): прво, ендонуклеазата Дроша ги отсекува едноверижните РНК „опашки“ од шнолата, по што исечената фиба (пред-микроРНК) се извезува во цитоплазмата, каде што е препознаен од Dicer, кој прави уште две резови (сече со двојно жица е отсечено, боја кодирана на Сл. 3А). Во оваа форма, зрелата микроРНК, слична на siRNA, е вклучена во комплексот RISC.
Механизмот на дејство на многу микроРНК е сличен на дејството на siRNA: кратка (21-25 нуклеотиди) едноверижна РНК како дел од протеинскиот комплекс RISC се врзува со висока специфичност за комплементарното место во 3'-непреведениот регион на целната mRNA. Врзувањето доведува до расцепување на mRNA од протеинот Аго. Сепак, активноста на микроРНК (во споредба со сиРНК) е веќе подиференцирана - ако комплементарноста не е апсолутна, целната мРНК можеби нема да се разградува, туку само реверзибилно блокирана (нема да има транслација). Истиот RISC комплекс може да користи и вештачки воведени siRNAs. Ова објаснува зошто siRNA направени по аналогија со протозои се активни и кај цицачите.
Така, можеме да ја надополниме илустрацијата за механизмот на дејство на интерференцијата на РНК кај повисоките (билатерално симетрични) организми со комбинирање во една слика на акциониот дијаграм на микроРНК и биотехнолошки воведените siRNA (сл. 3Б).
Ориз. 3А: Структура на двоверижна прекурсорска молекула на микроРНК
Главни карактеристики: присуство на зачувани секвенци кои формираат фиба; присуство на комплементарна копија (микроРНК*) со два „екстра“ нуклеотиди на 3’ крај; специфична секвенца (2-8 bp) која формира место за препознавање на ендонуклеази. Самата микроРНК е означена со црвено - тоа е она што Dicer го отсекува.

Ориз. 3Б: Општ механизам на обработка на микроРНК и имплементација на нејзината активност

Ориз. 3Б: Генерализирана шема на дејство на вештачки микроРНК и сиРНК
Вештачките siRNA се внесуваат во клетката со помош на специјализирани плазмиди (таргетирање siRNA вектор).
Функции на микроРНК
Физиолошките функции на микроРНК се исклучително разновидни - всушност, тие дејствуваат како главни непротеински регулатори на онтогенезата. микроРНК не се откажуваат, туку ја надополнуваат „класичната“ шема на генска регулација (индуктори, супресори, набивање на хроматин, итн.). Покрај тоа, синтезата на самите микроРНК е сложено регулирана (одредени базени на микроРНК може да се вклучат со интерферони, интерлеукини, фактор на туморска некроза α (TNF-α) и многу други цитокини). Како резултат на тоа, се појавува мрежа на повеќе нивоа на подесување на „оркестар“ од илјадници гени, неверојатна по својата сложеност и флексибилност, но ова не завршува тука.
микроРНК се повеќе „универзални“ од siRNA: гените „одделенија“ не мора да бидат 100% комплементарни - регулацијата исто така се спроведува преку делумна интеракција. Денес, една од најжешките теми во молекуларната биологија е потрагата по микроРНК кои дејствуваат како алтернативни регулатори на познатите физиолошки процеси. На пример, микроРНК вклучени во регулирањето на клеточниот циклус и апоптозата кај растенијата, Drosophila и нематодите веќе се опишани; кај луѓето, микроРНК го регулираат имунолошкиот систем и развојот на хематопоетски матични клетки. Употребата на технологии засновани на биочипови (скрининг со микро низа) покажа дека цели групи на мали РНК се вклучуваат и исклучуваат во различни фази од животот на клетките. Идентификувани се десетици специфични микроРНК за биолошки процеси, чие ниво на изразување под одредени услови се менува илјадници пати, нагласувајќи ја исклучителната контролираност на овие процеси.
До неодамна, се веруваше дека микроРНК само ја потиснува - целосно или делумно - работата на гените. Сепак, неодамна се покажа дека дејството на микроРНК може радикално да се разликува во зависност од состојбата на клетката! Во клетка која активно се дели, микроРНК се врзува за комплементарна секвенца во 3' регионот на mRNA и ја инхибира синтезата на протеини (превод). Меѓутоа, во состојба на одмор или стрес (на пример, кога растете во лоша средина), истиот настан доведува до сосема спротивен ефект - зголемена синтеза на целниот протеин!
Еволуција на микроРНК
Бројот на сорти на микроРНК во повисоките организми сè уште не е целосно утврден; според некои податоци, тој надминува 1% од бројот на гени кои кодираат протеини (кај луѓето, на пример, велат дека има 700 микроРНК, а овој број е постојано расте). микроРНК ја регулираат активноста на околу 30% од сите гени (целите за многу од нив сè уште не се познати), а има и сеприсутни и ткивни специфични молекули - на пример, еден таков важен базен на микроРНК го регулира созревањето на стеблото на крвта клетки.
Широкиот профил на изразување во различни ткива на различни организми и биолошката распространетост на микроРНК укажуваат на еволутивно античко потекло. МикроРНК за првпат биле откриени во нематоди, и долго време се верувало дека овие молекули се појавуваат само во сунѓери и колентерати; сепак, подоцна биле откриени во едноклеточни алги. Интересно, како што организмите стануваат посложени, бројот и хетерогеноста на базенот на miRNA исто така се зголемува. Ова индиректно укажува дека сложеноста на овие организми е обезбедена, особено, преку функционирањето на микроРНК. Можната еволуција на miRNA е прикажана на Сл. 4.

Ориз. 4. Разновидност на микроРНК во различни организми
Колку е поголема организацијата на организмот, толку повеќе микроРНК се наоѓаат во него (бројот во загради). Видовите во кои се пронајдени единечни микроРНК се означени со црвено. Според .
Може да се направи јасна еволутивна врска помеѓу siRNA и microRNA, врз основа на следните факти:
- дејството на двата типа е заменливо и е посредувано од хомологни протеини;
- siRNAs внесени во клетките на цицачите конкретно ги „исклучуваат“ саканите гени (и покрај одредено активирање на заштитата од интерферон);
- микроРНК се откриваат во се повеќе антички организми.
Овие и други податоци укажуваат на потеклото на двата системи од заеднички „предок“. Исто така, интересно е да се забележи дека имунитетот на „РНК“ како независен претходник на протеинските антитела ја потврдува теоријата за потеклото на првите форми на живот засновани на РНК, а не на протеини (да потсетиме дека ова е омилената теорија на академик А.С. Спирин). .
Додека имаше само двајца „играчи“ во арената на молекуларната биологија – siRNA и microRNA – главната „цел“ на интерференцијата на РНК изгледаше сосема јасна. Навистина: збир на хомологни кратки РНК и протеини во различни организми извршуваат слични дејства; Како што организмите стануваат покомплексни, така се зголемува и функционалноста.
Меѓутоа, во процесот на еволуција, природата создала друг, еволутивно најнов и високо специјализиран систем заснован на истиот успешен принцип на интерференција на РНК. Зборуваме за пиРНК (пиРНК, од РНК со интеракција на Пиви).
Колку е покомплексен геномот организиран, толку е поразвиен и поадаптиран организмот (или обратно? ;-). Сепак, зголемената сложеност на геномот има и негативна страна: сложениот генетски систем станува нестабилен. Ова доведува до потреба од механизми одговорни за одржување на интегритетот на геномот - инаку спонтано „мешање“ на ДНК едноставно ќе го оневозможи. Мобилните генетски елементи (MGE), еден од главните фактори за нестабилност на геномот, се кратки нестабилни региони кои можат автономно да се транскрибираат и мигрираат низ геномот. Активирањето на таквите транспонирани елементи доведува до повеќекратни прекини на ДНК во хромозомите, што може да има смртоносни последици.
Бројот на MGE се зголемува нелинеарно со големината на геномот и нивната активност мора да биде содржана. За да го направите ова, животните, почнувајќи од колентератите, го користат истиот феномен на интерференција на РНК. Оваа функција се врши и од кратки РНК, но не од веќе дискутираните, туку од трет тип - пиРНК.
„Портрет“ на пиРНК
пиРНК се кратки молекули долги 24-30 нуклеотиди, кодирани во центромерните и теломерите области на хромозомот. Секвенците на многу од нив се комплементарни со познатите мобилни генетски елементи, но има и многу други пиРНК кои се совпаѓаат со региони на работни гени или со фрагменти од геном чии функции се непознати.
пиРНК (како и микроРНК) се кодирани во двете нишки на геномската ДНК; тие се многу променливи и разновидни (до 500.000 (!) видови во еден организам). За разлика од siRNA и microRNA, тие се формираат од еден синџир со карактеристична особина– урацил (U) на 5’ крај и метилиран 3’ крај. Постојат и други разлики:
- За разлика од siRNA и microRNAs, тие не бараат обработка од Dicer;
- ПиРНК гените се активни само во герминативните клетки (за време на ембриогенезата) и околните ендотелијални клетки;
- Протеинскиот состав на системот piRNA е различен - ова се ендонуклеази од класата Piwi (Piwi и Aub) и посебна сорта на Argonaute - Ago3.
Обработката и активноста на пиРНК сè уште се слабо разбрани, но веќе е јасно дека механизмот на дејство е сосема различен од другите кратки РНК - денес е предложен пинг-понг модел на нивната работа (сл. 5 А, Б).
Пинг-понг механизам на биогенезата на пиРНК

Ориз. 5А: Цитоплазматски дел од обработката на пиРНК
Биогенезата и активноста на пиРНК е посредувана од фамилијата на ендонуклеази Piwi (Ago3, Aub, Piwi). Активноста на пиРНК е обезбедена од двете едноверижни молекули на пиРНК - смисла и анти-смисла - од кои секоја се поврзува со специфична Piwi ендонуклеаза. ПиРНК го препознава комплементарниот регион на транспозонската mRNA (сина нишка) и го отсекува. Ова не само што го инактивира транспозонот, туку и создава нова пиРНК (поврзана со Ago3 преку метилација на 3' крај со Hen1 метилаза). Оваа пиРНК, пак, препознава мРНК со транскрипти од кластерот прекурсори на пиРНК (црвена нишка) - на овој начин циклусот се затвора и повторно се произведува саканата пиРНК.

Ориз. 5Б: пиРНК во јадрото
Покрај ендонуклеазата Aub, ендонуклеазата Piwi исто така може да врзе антисенс пиРНК. По врзувањето, комплексот мигрира во јадрото, каде што предизвикува деградација на комплементарните транскрипти и преуредување на хроматин, предизвикувајќи супресија на активноста на транспозоните.
Функции на пиРНК
Главната функција на пиРНК е да ја потисне активноста на MGE на ниво на транскрипција и транслација. Се верува дека пиРНК се активни само за време на ембриогенезата, кога непредвидливото мешање на геномот е особено опасно и може да доведе до смрт на ембрионот. Ова е логично - кога имунолошкиот систем сè уште не почнал да работи, на клетките на ембрионот им е потребна едноставна, но ефикасна заштита. Ембрионот е сигурно заштитен од надворешни патогени со плацентата (или лушпата од јајцето). Но, покрај ова, неопходна е и одбрана од ендогени (внатрешни) вируси, првенствено MGE.
Оваа улога на пиРНК е потврдена со искуство - „нокаут“ или мутации на гените Ago3, Piwi или Aub доведуваат до сериозни развојни нарушувања (и нагло зголемување на бројот на мутации во геномот на таков организам), а исто така предизвикуваат неплодност поради нарушување на развојот на герминативните клетки.
Дистрибуција и еволуција на пиРНК
Првите пиРНК веќе се наоѓаат во морските анемони и сунѓери. Растенијата очигледно тргнаа по поинаков пат - во нив не беа пронајдени протеини од Piwi, а улогата на „муцка“ за транспозоните ја извршуваат ендонуклеазата Ago4 и siRNA.
Кај повисоките животни, вклучително и луѓето, системот на пиРНК е многу добро развиен, но може да се најде само во ембрионските клетки и во амнионскиот ендотел. Зошто дистрибуцијата на пиРНК во телото е толку ограничена, останува да се види. Може да се претпостави дека, како и секое моќно оружје, пиРНК се корисни само под многу специфични услови (за време на развојот на фетусот), а кај возрасното тело нивната активност ќе предизвика повеќе штета отколку добро. Сепак, бројот на пиРНК го надминува бројот на познати протеини по ред на големина, а неспецифичните ефекти на пиРНК во зрелите клетки е тешко да се предвидат.
| siRNA | микроРНК | пиРНК | |
| Ширење | Растенија, Дрософила, C. elegans. Не се наоѓа кај 'рбетниците | Еукариоти | Ембрионски клетки на животни (почнувајќи со колентерати). Не во протозои и растенија |
| Должина | 21-22 нуклеотиди | 19-25 нуклеотиди | 24-30 нуклеотиди |
| Структура | Двојно-верижна, 19 комплементарни нуклеотиди и два неспарени нуклеотиди на 3' крај | Комплексна структура со еден синџир | Комплексна структура со еден синџир. U на 5'-крај, 2'- О-метилиран 3' крај |
| Обработка | Dicer-зависен | Dicer-зависен | Dicer-независен |
| Ендонуклеази | Пред 2 | Аго1, Аго2 | Ago3, Piwi, Aub |
| Активност | Деградација на комплементарни mRNA, ацетилација на геномната ДНК | Деградација или инхибиција на транслацијата на целната mRNA | Деградација на мРНК што го кодира МГЕ, регулирање на транскрипцијата на МГЕ |
| Биолошка улога | Антивирусна имунолошка одбрана, потиснување на активноста на сопствените гени | Регулирање на генската активност | Сузбивање на активноста на MGE за време на ембриогенезата |
Заклучок
Како заклучок, би сакал да дадам табела што ја илустрира еволуцијата на протеинскиот апарат вклучен во интерференцијата на РНК (сл. 6). Може да се види дека протозоите имаат најразвиен siRNA систем (протеински семејства Ago, Dicer), и како што организмите стануваат посложени, акцентот се префрла на поспецијализирани системи - бројот на протеински изоформи за микроРНК (Дроша, Паша) и пиРНК ( Piwi, Hen1) се зголемува. Во исто време, разновидноста на ензимите кои посредуваат во дејството на siRNA се намалува.

Ориз. 6. Разновидност на протеини вклучени во интерференција на РНК
И
Броевите го означуваат бројот на протеини во секоја група. Елементите карактеристични за siRNA и microRNA се означени со сино, а протеините поврзани со пиРНК се означени со црвено. Според .
Феноменот на интерференција на РНК почна да се користи од наједноставните организми. Врз основа на овој механизам, природата создаде прототип на имунолошкиот систем, а како што организмите стануваат покомплексни, интерференцијата на РНК станува незаменлив регулатор на активноста на геномот. Два различни механизми плус три типа на кратки РНК (види сумарна табела) - како резултат на тоа, гледаме илјадници фини регулатори на различни метаболички и генетски патишта. Оваа впечатлива слика ја илустрира разновидноста и еволутивната адаптација на молекуларните биолошки системи. Кратките РНК повторно докажуваат дека нема „мали нешта“ во клетката - има само мали молекули, целосното значење на чија улога само што почнуваме да го разбираме.
Точно, таквата фантастична сложеност повеќе сугерира дека еволуцијата е „слепа“ и дејствува без однапред одобрен „мастер план“.
Литература
- Gurdon J. B., Lane C. D., Woodland H. R., Marbaix G. (1971). Употреба на јајца од жаба и ооцити за проучување на гласник РНК и нејзин превод во живите клетки. Природа 233, 177-182;
- Spirin A. S. (2001). Биосинтеза на протеини, светот на РНК и потеклото на животот. Билтен на Руската академија на науките 71, 320-328;
- Елементи: „Од влакната сега може да се извлечат целосни митохондријални геноми на изумрени животни“;
- Fire A., Xu S., Montgomery M.K., Kostas S.A., Driver S.E., Mello C.C. (1998). Моќна и специфична генетска интерференција од двоверижна РНК во Caenorhabditis elegans. Nature 391, 806-311;
- Биомолекула: „МикроРНК откриени за прв пат во едноклеточен организам“;
- Covey S., Al-Kaff N., Lángara A., Turner D. (1997). Растенијата се борат против инфекцијата со замолчување на гените. Nature 385, 781-782;
- Биомолекула: „Молекуларно двојно работење: човечките гени работат за вирусот на грип“;
- Рен Б. (2010). Транскрипција: Зајакнувачите создаваат некодирачка РНК. Природа 465, 173–174;
- Таганов К.Д., Болдин М.П., Чанг К.Ј., Балтимор Д. (2006). NF-κB-зависна индукција на микроРНК miR-146, инхибитор насочен кон сигнализирање на протеините на вродените имунолошки одговори. Proc. Натл. акад. Sci. САД. 103, 12481-12486;
- O'Connell R. M., Rao D. S., Chaudhuri A. A., Boldin M. P., Taganov K. D., Nicoll J., Paquette R. L., Baltimore D. (2008). Одржливата експресија на микроРНК-155 во хематопоетските матични клетки предизвикува миелопролиферативно нарушување. J. Exp. Med. 205, 585-594;
- Биомолекула: „микроРНК – колку подалеку во шумата, толку повеќе огревно дрво“;
- Елементи: „Компликацијата на телото кај древните животни беше поврзана со појавата на нови регулаторни молекули“;
- Гримсон А., Сривастава М., Фахеј Б., Вудкрофт Б.Џ., Чианг Х.Р., Кинг Н., Дегнан Б.М., Роксар Д.С., Бартел Д.П. (2008). Рано потекло и еволуција на микроРНК и РНК со интеракција со Пиви кај животните. Природа 455, 1193–1197.
- Аравин А., Ханон Г., Бренеке Ј. (2007). Патеката Piwi-piRNA обезбедува адаптивна одбрана во трката за вооружување со транспосон. Наука 318, 761–764;
- Биомолекула:
Научниците веруваат дека неправилното изразување на малите РНК е една од причините за голем број болести кои сериозно влијаат на здравјето на многу луѓе ширум светот. Овие болести вклучуваат кардиоваскуларни 23 и рак 24 . Што се однесува до второто, тоа не е изненадувачки: ракот укажува на абнормалности во развојот на клетките и нивната судбина, а малите РНК играат клучна улога во соодветните процеси. Еве еден од најзначајните примери за огромното влијание што малите РНК го имаат врз телото за време на ракот. Станува збор за малигнен тумор, кој се карактеризира со неправилно изразување на оние гени кои дејствуваат во текот на почетниот развој на организмот, а не во постнаталниот период. Ова е еден вид тумор на мозокот кај детството кој обично се појавува пред двегодишна возраст. За жал, ова е многу агресивна форма на рак, а прогнозата овде е неповолна дури и со интензивно лекување. Онколошкиот процес се развива поради неправилна прераспределба на генетскиот материјал во мозочните клетки. Промотор кој вообичаено поттикнува силна експресија на еден од гените за кодирање на протеините се подложува на рекомбинација со специфичен кластер на мали РНК. Тогаш целиот овој преуреден регион се подложува на засилување: со други зборови, многу копии од него се создаваат во геномот. Следствено, малите РНК лоцирани „долуводно“ од преместениот промотер се изразени многу посилно отколку што би требало да бидат. Нивото на активни мали РНК е приближно 150-1000 пати повисоко од нормалното.
Ориз. 18.3.Мали РНК активирани од алкохол може да се комбинираат со гласник РНК кои не влијаат на отпорноста на телото на ефектите на алкохолот. Но, овие мали РНК не се врзуваат за молекулите на гласникот на РНК кои промовираат таков отпор. Ова резултира со релативна доминација на процентот на гласник РНК молекули кои ги кодираат протеинските варијации поврзани со толеранцијата на алкохол.
Овој кластер кодира повеќе од 40 различни мали РНК. Всушност, ова е генерално најголемото од таквите кластери пронајдени кај приматите. Обично се изразува само рано во човековиот развој, во првите 8 недели од ембрионалниот живот. Неговото силно активирање во мозокот на доенчињата доведува до катастрофални ефекти врз генетската експресија. Една последица е изразувањето на епигенетскиот протеин кој додава модификации на ДНК. Ова води до широки промени во целиот модел на метилација на ДНК, а со тоа и до абнормална експресија на сите видови гени, од кои многу треба да се изразат само кога незрелите мозочни клетки се делат за време на раните фазиразвој на телото. Вака започнува програмата за рак во клетките на бебето 25.
Таквата комуникација помеѓу малите РНК и епигенетската машинерија на клетката може да има значително влијание врз други ситуации кога клетките развиваат предиспозиција за рак. Овој механизам најверојатно резултира со ефектот на нарушување на експресијата на малата РНК што е зајакнат со промени во епигенетските модификации кои се пренесуваат на ќерките клетки од мајката. Ова може да создаде шема на потенцијално опасни промени во моделот на генска експресија.
Досега, научниците не ги сфатиле сите фази на интеракцијата на малите РНК со епигенетските процеси, но сепак можат да добијат некои навестувања за карактеристиките на она што се случува. На пример, се покажа дека одредена класа на мали РНК, кои ја зголемуваат агресивноста на ракот на дојката, таргетира одредени ензими во гласникот РНК кои ги отстрануваат клучните епигенетски модификации. Ова го менува моделот на епигенетските модификации во клетката на ракот и дополнително ја нарушува генетската експресија 26 .
Многу форми на рак е тешко да се следат кај пациент. Онколошки процеси може да се појават на тешко достапни места, што ја отежнува процедурата за земање мостри. Во такви случаи, на лекарот не му е лесно да го следи развојот на процесот на рак и одговорот на третманот. Често лекарите се принудени да се потпрат на индиректни мерења - да речеме, томографско скенирање на тумор. Некои истражувачи веруваат дека малите молекули на РНК би можеле да помогнат да се создаде нова техника за следење на развојот на туморот, која исто така би можела да го проучува неговото потекло. Кога клетките на ракот умираат, малите РНК ја напуштаат клетката кога таа ќе пукне. Овие мали непотребни молекули често формираат комплекси со клеточни протеини или се обвиткани во фрагменти клеточните мембрани. Поради ова, тие се многу стабилни во телесните течности, што значи дека таквите РНК може да се изолираат и анализираат. Бидејќи нивните количини се мали, истражувачите ќе мора да користат многу чувствителни методи за анализа. Сепак, тука ништо не е невозможно: чувствителност на секвенционирање нуклеински киселинипостојано се зголемува 27. Објавени се податоци кои го потврдуваат ветувањето за овој пристап во однос на ракот на дојката 28 , ракот на јајниците 29 и голем број други онколошки заболувања. Анализата на малите циркулирачки РНК кај пациенти со рак на белите дробови покажа дека овие РНК помагаат да се направи разлика помеѓу пациентите со осамен пулмонален јазол (не бара терапија) и пациентите кои развиваат малигни туморски јазли (кои бараат третман) 30 .
Мали РНК кои формираат шноли или кратки РНК кои формираат шноли (shRNA кратка шнола RNA, мала шнола RNA) молекули на кратки РНК кои формираат секундарна структуратесни стилети. ShRNA може да се користат за исклучување на изразување... ... Википедија
РНК полимераза- од клетка T. aquaticus при репликација. Некои елементи на ензимот се направени транспарентни, а синџирите на РНК и ДНК се појасно видливи. Јонот на магнезиум (жолт) се наоѓа на активното место на ензимот. РНК полимеразата е ензим кој врши ... ... Википедија
РНК интерференција- Испорака на мали РНК кои содржат шноли со помош на вектор базиран на лентивирус и механизмот на интерференција на РНК во клетките на цицачите РНК интерференција (а ... Википедија
РНК ген- Некодирачка РНК (ncRNA) се молекули на РНК кои не се преведуваат во протеини. Претходно користениот синоним, мала РНК (смРНК, мала РНК), повеќе не се користи, бидејќи некои некодирачки РНК може да бидат многу ... ... Википедија
Мали нуклеарни РНК- (snRNA, snRNA) класа на РНК што се наоѓа во јадрото на еукариотските клетки. Тие се транскрибираат со РНК полимераза II или РНК полимераза III и се вклучени во важни процеси како што се спојување (отстранување на интрони од незрела мРНК), регулација ... Википедија
Мали нуклеоларни РНК- (snoRNA, англиски snoRNA) класа на мали РНК вклучени во хемиски модификации (метилација и псеудуридилација) на рибозомалната РНК, како и tRNA и мала нуклеарна РНК. Според класификацијата MeSH, малите нуклеоларни РНК се сметаат за подгрупа... ... Википедија
мали нуклеарни (нуклеарни со мала молекуларна тежина) РНК- Широка група (105.106) мали нуклеарни РНК (100.300 нуклеотиди), поврзани со хетерогена нуклеарна РНК, се дел од малите рибонуклеопротеински гранули на јадрото; M.n.RNA се неопходна компонента на системот за спојување... ...
мали цитоплазматски РНК- Мали (100-300 нуклеотиди) РНК молекули локализирани во цитоплазмата, слични на малата нуклеарна РНК. [Арефјев В.А., Лисовенко Л.А. Англиски руски јазик Речникгенетски термини 1995 407 стр.] Теми генетика EN scyrpssмал цитоплазматски... ... Водич за технички преведувач
мали нуклеарни РНК од класа U- Група асоцирани со протеини мали (од 60 до 400 нуклеотиди) РНК молекули кои сочинуваат значителен дел од содржината на спликомот и се вклучени во процесот на ексцизија на интроните; во 4 од 5-те добро проучени Usn типови, U1, U2, U4 и U5 РНК се 5... ... Водич за технички преведувач
РНК биомаркери- * РНК биомаркери * РНК биомаркери огромен број човечки транскрипти кои не ја кодираат синтезата на протеини (nsbRNA или npcRNA). Во повеќето случаи, малите (miRNA, snoRNA) и долгите (антисенс РНК, dsRNA и други видови) молекули на РНК се... ... Генетика. енциклопедиски речник
Книги
- Купете за 1877 UAH (само во Украина)
- Клиничка генетика. Учебник (+ЦД), Бочков Николај Павлович, Пузирев Валери Павлович, Смирнихина Светлана Анатолиевна. Сите поглавја се ревидирани и дополнети во врска со развојот на медицинската наука и практика. Поглавјата за мултифакторни заболувања, превенција, третман на наследни болести,…