Амино киселините покажуваат својства и на киселини и на амини. Значи, тие формираат соли (поради киселинските својства на карбоксилната група):
NH 2 CH 2 COOH + NaOH (NH 2 CH 2 COO) Na + H 2 O
глицин натриум глицинат
и естри (како и другите органски киселини):
NH 2 CH 2 COOH + C 2 H 5 OHNH 2 CH 2 C(O)OC 2 H 5 + H 2 O
глицин етилглицинат
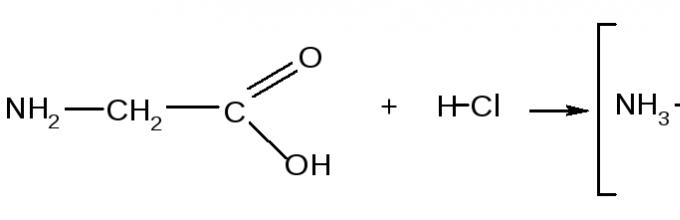
Со посилните киселини, амино киселините покажуваат својства на базите и формираат соли поради основните својства на амино групата:

глицин вистерија хлорид
Наједноставниот протеин е полипептид кој содржи најмалку 70 амино киселински остатоци во својата структура и има молекуларна тежина од над 10.000 Da (далтон). Далтон - мерна единица за масата на протеините, 1 далтон е еднаква на 1,66054·10 -27 kg (единица на јаглеродна маса). Слични соединенија кои се состојат од помалку амино киселински остатоци се класифицирани како пептиди. Пептидите по природа се некои хормони - инсулин, окситоцин, вазопресин. Некои пептиди се регулатори на имунитетот. Некои антибиотици (циклоспорин А, грамицидини А, Б, Ц и С), алкалоиди, токсини од пчели и оси, змии, отровни печурки (фалоидин и аманитин од жабарот), колера и ботулински токсини итн. имаат пептидна природа.
Нивоа на структурна организација на протеинските молекули.
Протеинската молекула има комплексна структура. Постојат неколку нивоа на структурна организација на протеинската молекула - примарни, секундарни, терцијарни и кватернарни структури.
Примарна структура е дефинирана како линеарна низа од протеиногени аминокиселински остатоци поврзани со пептидни врски (сл. 5):

Сл.5. Примарна структура на протеинска молекула
Примарната структура на протеинската молекула е генетски одредена за секој специфичен протеин во нуклеотидната секвенца на гласник РНК. Примарната структура, исто така, одредува повисоки нивоа на организација на протеинските молекули.
Секундарна структура - конформација (т.е. локација во вселената) на поединечни делови од протеинската молекула. Секундарната структура во протеините може да биде претставена со -спирала, -структура (структура на преклопен лист) (сл. 6).
Сл.6. Протеинска секундарна структура
Секундарната структура на протеинот се одржува со водородни врски помеѓу пептидните групи.
Терцијарна структура - конформација на целата протеинска молекула, т.е. просторно распоредување на целиот полипептиден синџир, вклучувајќи го распоредот на страничните радикали. За значителен број протеини, координатите на сите протеински атоми се добиени со анализа на дифракција на Х-зраци, со исклучок на координатите на атоми на водород. Во формирањето и стабилизирањето на терциерната структура учествуваат сите видови интеракции: хидрофобни, електростатски (јонски), дисулфидни ковалентни врски, водородни врски. Во овие интеракции учествуваат радикали на остатоци од аминокиселини. Меѓу врските што ја држат терциерната структура треба да се истакне: а) дисулфиден мост (- S - S -); б) естерски мост (помеѓу карбоксилната група и хидроксилната група); в) мост на сол (помеѓу карбоксилната група и амино групата); г) водородни врски.
Во согласност со обликот на протеинската молекула, определена со терциерната структура, се разликуваат следните групи на протеини:
1) Глобуларни протеини , кои имаат облик на топче (сфера). Таквите протеини вклучуваат, на пример, миоглобин, кој има 5 α-спирални сегменти и без β-набори, имуноглобулини, кои немаат α-спирала; главните елементи на секундарната структура се β-наборите
2) Фибриларни протеини . Овие протеини имаат издолжена форма на конец, тие вршат структурна функција во телото. Во примарната структура, тие имаат региони кои се повторуваат и формираат секундарна структура која е прилично униформа за целиот полипептиден синџир. Така, протеинот α - кератин (главната протеинска компонента на ноктите, косата, кожата) е изграден од продолжени α-спирали. Има поретки елементи секундарна структура, на пример, полипептидни синџири на колаген кои формираат левораки спирали со параметри кои остро се разликуваат од параметрите на α-спиралите. Во колагенските влакна, три спирални полипептидни синџири се извиткани во една десна суперхеликс (сл. 7):
Сл. 7 Терциерна структура на колагенот
Квартарна структура на протеинот. Кватернарната структура на протеините се однесува на начинот на кој поединечните полипептидни синџири (идентични или различни) со терциерна структура се распоредени во просторот, што доведува до формирање на структурно и функционално унифицирана макромолекуларна формација (мултимер). Не сите протеини имаат кватернарна структура. Пример за протеин со кватернарна структура е хемоглобинот, кој се состои од 4 подединици. Овој протеин е вклучен во транспортот на гасови во телото.
При кршење дисулфид ислаби видови врски во молекулите, сите протеински структури, освен примарната, се уништуваат (целосно или делумно), а протеинот ја губи својата мајчин имоти (својства на протеинската молекула својствени за неа во неговата природна, природна (мајчин) состојба). Овој процесповикани денатурација на протеини . Фактори кои предизвикуваат денатурација на протеините вклучуваат високи температури, ултравиолетово зрачење, концентрирани киселини и алкалии, соли тешки металии други.
Протеините се поделени на едноставно (протеини), кои се состојат само од амино киселини, и комплекс (протеини), кои содржат, покрај амино киселините, и други непротеински супстанции, на пример, јаглени хидрати, липиди, нуклеински киселини. Непротеинскиот дел од сложениот протеин се нарекува протетска група.
Едноставни протеини, кои се состојат само од остатоци од аминокиселини, се широко распространети во животинскиот и растителниот свет. Во моментов, не постои јасна класификација на овие соединенија.
Хистони
Тие имаат релативно мала молекуларна тежина (12-13 илјади), со доминација на алкални својства. Локализиран главно во клеточните јадра, растворлив во слаби киселини, преципитирани од амонијак и алкохол. Тие имаат само терцијарна структура. Во природни услови, тие се цврсто врзани за ДНК и се дел од нуклеопротеините. Главната функција е регулирање на трансферот на генетски информации од ДНК и РНК (преносот може да биде блокиран).
Протамини
Овие протеини имаат најниска молекуларна тежина (до 12 илјади). Покажува изразени основни својства. Добро растворлив во вода и слаби киселини. Содржани во герминативните клетки и го сочинуваат најголемиот дел од протеинот на хроматин. Како и хистоните, тие формираат комплекс со ДНК и даваат хемиска стабилност на ДНК, но за разлика од хистоните, тие не вршат регулаторна функција.
Глутелини
Растителни протеини содржани во глутен од семето на житарките и некои други култури, во зелените делови на растенијата. Нерастворлив во вода, солени раствори и етанол, но високо растворлив во слаби алкални раствори. Тие ги содржат сите есенцијални амино киселини и се комплетни прехранбени производи.
Проламини
Растителни протеини. Содржани во глутен од житни растенија. Тие се растворливи само во 70% алкохол (ова се објаснува со високата содржина на пролин и неполарни амино киселини во овие протеини).
Протеиноиди.
Протеиноидите вклучуваат протеини на потпорните ткива (коски, 'рскавица, лигаменти, тетиви, нокти, коса); тие се карактеризираат со висока содржина на сулфур. Овие протеини се нерастворливи или ретко растворливи во вода, сол и вода-алкохолни смеси.Протеиноидите вклучуваат кератин, колаген, фиброин.
Албумин
Ова се кисели протеини со мала молекуларна тежина (15-17 илјади), растворливи во вода и слаби солени раствори. Таложено од неутрални соли на 100% сатурација. Тие учествуваат во одржувањето на осмотскиот притисок на крвта и транспортираат разни материи со крвта. Содржани во крвниот серум, млеко, белка од јајце.
Глобулини
Молекуларна тежина до 100 илјади Нерастворлив во вода, но растворлив во слаби солени раствори и се таложи во помалку концентрирани раствори (веќе на 50% заситеност). Содржани во растителни семиња, особено мешунки и маслодајни семиња; во крвната плазма и некои други биолошки течности. Тие ја вршат функцијата на имунолошка одбрана и обезбедуваат отпорност на телото на вирусни заразни болести.
Амино киселини, протеини и пептидисе примери на соединенијата опишани подолу. Многу биолошки активни молекули содржат неколку хемиски различни функционални групи кои можат да комуницираат меѓу себе и меѓусебните функционални групи.
Амино киселини.
Амино киселини- органски бифункционални соединенија, кои вклучуваат карбоксилна група - УНС, а амино групата е Н.Х. 2 .
Одделно α И β - амино киселини:
Најчесто се наоѓа во природата α -киселини. Протеините содржат 19 амино киселини и една имино киселина ( C 5 H 9БР 2 ):


Наједноставниот амино киселина- глицин. Останатите амино киселини може да се поделат во следниве главни групи:
1) хомолози на глицин - аланин, валин, леуцин, изолеуцин.
Добивање на амино киселини.
Хемиски својства на амино киселините.
Амино киселини- Ова амфотерични соединенија, бидејќи содржат 2 спротивни функционални групи- амино група и хидроксилна група. Затоа, тие реагираат и со киселини и со алкалии:
Киселинско-базната трансформација може да се претстави како:
Амино киселините се структурни хемиски единици или „градежни блокови“ кои ги сочинуваат протеините. Амино киселините се состојат од 16% азот, ова е нивната главна хемиска разликаод другите две суштински елементиисхрана - јаглени хидрати и масти. Важноста на аминокиселините за организмот е одредена од огромната улога што ја играат протеините во сите животни процеси.
Секој жив организам, од најголемите животни до ситни микроби, се состои од протеини. Различни формипротеините учествуваат во сите процеси што се случуваат во живите организми. Во човечкото тело, мускулите, лигаментите, тетивите, сите органи и жлезди, косата и ноктите се формираат од протеини. Протеините се наоѓаат во течностите и коските. Ензимите и хормоните кои ги катализираат и регулираат сите процеси во телото се исто така протеини. Недостатокот на овие хранливи материи во телото може да доведе до нерамнотежа во рамнотежата на водата, што предизвикува оток.
Секој протеин во телото е уникатен и постои за одредени цели. Протеините не се заменливи. Тие се синтетизираат во телото од амино киселини, кои се формираат како резултат на разградувањето на протеините кои се наоѓаат во храната. Така, амино киселините, а не самите протеини се највредните нутритивни елементи. Покрај тоа што аминокиселините формираат протеини кои ги сочинуваат ткивата и органите на човечкото тело, некои од нив делуваат како невротрансмитери (невротрансмитери) или се нивни претходници.
Невротрансмитери се хемиски супстанции, пренесување на нервните импулси од една нервна клетка во друга. Така, некои амино киселини се неопходни за нормална функција на мозокот. Амино киселините обезбедуваат витамини и минерали соодветно да ги извршуваат своите функции. Некои амино киселини директно обезбедуваат енергија на мускулното ткиво.
Во човечкото тело, многу амино киселини се синтетизираат во црниот дроб. Сепак, некои од нив не можат да се синтетизираат во телото, па затоа човекот мора да ги добие од храна. Овие есенцијални амино киселини вклучуваат хистидин, изолеуцин, леуцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. Амино киселини кои се синтетизираат во црниот дроб: аланин, аргинин, аспарагин, аспарагинска киселина, цитрулин, цистеин, гама-аминобутерна киселина, глутамин и глутаминска киселина, глицин, орнитин, пролин, серин, таурин, тирозин.
Процесот на синтеза на протеини се случува постојано во телото. Во случај кога барем еден есенцијална амино киселинае отсутен, формирањето на протеини е суспендирано. Ова може да доведе до различни сериозни проблеми, од лошо варење до депресија и бавен раст.
Како настанува оваа ситуација? Полесно отколку што може да замислите. Многу фактори водат до тоа, дури и ако вашата исхрана е урамнотежена и консумирате доволно протеини. Малапсорпција во гастроинтестиналниот тракт, инфекции, повреди, стрес, одредени лекови, процесот на стареење и нерамнотежа на другите хранливи материи во телото, сето тоа може да доведе до недостаток на есенцијални аминокиселини.
Имајте на ум дека сето горенаведено не значи дека консумирањето многу протеини ќе реши какви било проблеми. Во реалноста, тоа не е погодно за одржување на здравјето.
Вишокот на протеини создава дополнителен стрес за бубрезите и црниот дроб, кои треба да ги обработат производите од метаболизмот на протеините, а главен е амонијакот. Тој е многу отровен за телото, па црниот дроб веднаш го преработува во уреа, која потоа преку крвотокот патува до бубрезите, каде што се филтрира и се излачува.
Сè додека количината на протеини не е превисока и црниот дроб добро функционира, амонијакот веднаш се неутрализира и не предизвикува никаква штета. Но, ако има премногу и црниот дроб не може да се справи со неговото неутрализирање (како резултат на лошата исхрана, дигестивни нарушувања и/или заболување на црниот дроб), во крвта се создаваат токсични нивоа на амонијак. Во овој случај, може да има маса сериозни проблемисо здравје, до хепатална енцефалопатија и кома.
Премногу висока концентрација на уреа предизвикува и оштетување на бубрезите и болки во грбот. Затоа, не е важно количеството, туку квалитетот на протеините што се консумираат во храната. Во моментов, можно е да се добијат есенцијални и несуштински амино киселини во форма на биолошки активни адитиви за храна.
Ова е особено важно за разни болести и при користење на диети за намалување. На вегетаријанците им се потребни додатоци кои содржат есенцијални амино киселини за да се осигураат дека телото добива се што е потребно за нормална синтеза на протеини.
 Достапно различни типовидодатоци кои содржат амино киселини. Амино киселините се дел од некои мултивитамини и протеински мешавини. Постојат комерцијално достапни формули кои содржат комплекси на амино киселини или кои содржат една или две амино киселини. Тие се претставени во различни форми: во капсули, таблети, течности и прашоци.
Достапно различни типовидодатоци кои содржат амино киселини. Амино киселините се дел од некои мултивитамини и протеински мешавини. Постојат комерцијално достапни формули кои содржат комплекси на амино киселини или кои содржат една или две амино киселини. Тие се претставени во различни форми: во капсули, таблети, течности и прашоци.
Повеќето амино киселини постојат во две форми, хемиската структура на едната е огледална слика на другата. Овие се нарекуваат D- и L-форми, на пример Д-цистин и L-цистин.
D значи декстра (десно на латински) и L значи лево (лево). Овие термини укажуваат на насоката на ротација на спиралата, што е хемиска структура на дадена молекула. Протеините во животинските и растителните организми се создаваат главно од L-форми на амино киселини (со исклучок на фенилаланин, кој е претставен со форми D, L).
Додатоци во исхраната кои содржат L-амино киселини се сметаат за посоодветни за биохемиските процеси на човечкото тело.
Слободните или неврзаните амино киселини се најчистата форма. Затоа, при изборот на додаток на аминокиселини, предност треба да се даде на производи кои содржат L-кристални амино киселини стандардизирани од Американската фармакопеја (USP). Тие не бараат варење и се апсорбираат директно во крвотокот. По орална администрација, тие се апсорбираат многу брзо и, по правило, не предизвикуваат алергиски реакции.
Поединечни амино киселини се земаат на празен стомак, по можност наутро или помеѓу оброци со мала количина на витамини Б6 и Ц. минути после или 30 минути пред оброците. Најдобро е да се земат и поединечни есенцијални амино киселини и комплекс од аминокиселини, но во различно време. Само амино киселините не треба да се земаат долго време, особено во високи дози. Се препорачува да се зема 2 месеци со 2 месеци пауза.
Аланин
Аланин помага во нормализирање на метаболизмот на гликозата. Воспоставена е врска помеѓу вишокот на аланин и инфекцијата со вирусот Епштајн-Бар, како и синдромот на хроничен замор. Една форма на аланин - бета-аланин е составен делпантотенска киселина и коензим А - еден од најважните катализатори во телото.
Аргинин
Аргининот го забавува растот на туморите, вклучувајќи го и ракот, преку стимулирање имунолошки системтело. Ја зголемува активноста и големината на тимусната жлезда, која произведува Т-лимфоцити. Во овој поглед, аргининот е корисен за луѓето кои страдаат од ХИВ инфекција и малигни неоплазми.
Се користи и за заболувања на црниот дроб (цироза и масна дегенерација), промовира процеси на детоксикација во црниот дроб (првенствено неутрализација на амонијакот). Семената течност содржи аргинин, па затоа понекогаш се користи во сложениот третман на неплодност кај мажите. Се наоѓа и во сврзното ткиво и кожата голем број нааргинин, па затоа земањето е ефикасно за разни повреди. Аргининот е важна компонента на метаболизмот во мускулното ткиво. Помага во одржување на оптималната рамнотежа на азот во телото, бидејќи учествува во транспортот и неутрализацијата на вишокот на азот во телото.
Аргининот помага при слабеење бидејќи предизвикува мало намалување на резервите на маснотии во телото.
 Аргининот е дел од многу ензими и хормони. Има стимулирачки ефект врз производството на инсулин од панкреасот како компонента на вазопресин (хормон на хипофизата) и помага во синтезата на хормонот за раст. Иако аргининот се синтетизира во телото, неговото производство може да се намали кај новороденчињата. Извори на аргинин вклучуваат чоколадо, кокос, млечни производи, желатин, месо, овес, кикирики, соја, ореви, бело брашно, пченица и пченични никулци.
Аргининот е дел од многу ензими и хормони. Има стимулирачки ефект врз производството на инсулин од панкреасот како компонента на вазопресин (хормон на хипофизата) и помага во синтезата на хормонот за раст. Иако аргининот се синтетизира во телото, неговото производство може да се намали кај новороденчињата. Извори на аргинин вклучуваат чоколадо, кокос, млечни производи, желатин, месо, овес, кикирики, соја, ореви, бело брашно, пченица и пченични никулци.
Луѓето кои имаат вирусни инфекции, вклучувајќи го и херпес симплекс, не треба да земаат додатоци на аргинин и треба да избегнуваат конзумирање на храна богата со аргинин. Бремените и доилките не треба да земаат додатоци на аргинин. Земање мали дози на аргинин се препорачува за болести на зглобовите и сврзното ткиво, нарушена толеранција на гликоза, заболувања на црниот дроб и повреди. Не се препорачува долготрајна употреба.
Аспарагин
Аспарагинот е неопходен за одржување на рамнотежа во процесите што се случуваат во централниот дел нервен систем: спречува и прекумерно возбудување и прекумерна инхибиција. Тој е вклучен во процесите на синтеза на аминокиселини во црниот дроб.
Со оглед на тоа што оваа аминокиселина ја зголемува виталноста, додатокот базиран на неа се користи за замор. Исто така, игра важна улога во метаболичките процеси. Аспарагинската киселина често се препишува за болести на нервниот систем. Тоа е корисно за спортистите, како и за дисфункција на црниот дроб. Покрај тоа, го стимулира имунолошкиот систем со зголемување на производството на имуноглобулини и антитела.
Аспарагинската киселина се наоѓа во големи количини во растителните протеини добиени од никнати семиња и во месните производи.
Карнитин
Строго кажано, карнитинот не е аминокиселина, но неговата хемиска структура е слична на онаа на амино киселините и затоа тие обично се разгледуваат заедно. Карнитинот не е вклучен во синтезата на протеините и не е невротрансмитер. Неговата главна функција во телото е транспорт на масни киселини со долг ланец, чија оксидација ослободува енергија. Ова е еден од главните извори на енергија за мускулното ткиво. Така, карнитинот ја зголемува конверзијата на мастите во енергија и го спречува таложењето на маснотии во телото, пред се во срцето, црниот дроб и скелетните мускули.
Карнитинот ја намалува веројатноста за развој на компликации од дијабетес поврзани со нарушувања на липидниот метаболизам, ја забавува дегенерацијата на масни црн дроб кај хроничен алкохолизам и ризикот од срцеви заболувања. Има способност да го намали нивото на триглицериди во крвта, промовира губење на тежината и ја зголемува мускулната сила кај пациенти со невромускулни заболувања и го подобрува антиоксидантниот ефект на витамините Ц и Е.
Се верува дека некои варијанти на мускулна дистрофија се поврзани со дефицит на карнитин. Со такви болести, луѓето треба да добијат повеќе од оваа супстанца отколку што се бара според нормите.
Може да се синтетизира во телото во присуство на железо, тиамин, пиридоксин и аминокиселините лизин и метионин. Синтезата на карнитин се јавува во присуство на доволни количини на витамин Ц. Недоволните количини на која било од овие хранливи материи во телото доведува до дефицит на карнитин. Карнитинот влегува во телото со храна, пред се месо и други производи од животинско потекло.
 Повеќето случаи на дефицит на карнитин се поврзани со генетски детерминиран дефект во процесот на неговата синтеза. Можни манифестации на дефицит на карнитин вклучуваат нарушена свест, болка во срцето, мускулна слабост и дебелина.
Повеќето случаи на дефицит на карнитин се поврзани со генетски детерминиран дефект во процесот на неговата синтеза. Можни манифестации на дефицит на карнитин вклучуваат нарушена свест, болка во срцето, мускулна слабост и дебелина.
Мажите, поради нивната поголема мускулна маса, бараат повеќе карнитин од жените. Вегетаријанците имаат поголема веројатност да имаат недостаток во ова хранлива состојкаод невегетаријанците, поради фактот што карнитинот не се наоѓа во растителните протеини.
Покрај тоа, метионин и лизин (амино киселини неопходни за синтеза на карнитин) исто така не се наоѓаат во доволни количини во растителната храна.
За да ја добијат потребната количина на карнитин, вегетаријанците треба да земаат додатоци или да јадат храна збогатена со лизин, како што се корнфлекс.
Карнитинот е претставен во додатоците во исхраната во различни форми: во форма на Д, Л-карнитин, Д-карнитин, Л-карнитин, ацетил-Л-карнитин.
Пожелно е да се зема Л-карнитин.
Цитрулин
Цитрулинот претежно се наоѓа во црниот дроб. Го зголемува снабдувањето со енергија, го стимулира имунолошкиот систем и се претвора во Л-аргинин за време на метаболизмот. Го неутрализира амонијакот, кој ги оштетува клетките на црниот дроб
Цистеин и цистин
Овие две амино киселини се тесно поврзани, секоја молекула на цистин се состои од две молекули на цистеин поврзани една со друга. Цистеинот е многу нестабилен и лесно се трансформира во L-цистин, а со тоа една аминокиселина лесно може да се промени во друга кога е потребно.
Двете амино киселини се амино киселини кои содржат сулфур и играат важна улога во формирањето на ткивото на кожата и се важни за процесите на детоксикација. Цистеинот е дел од алфа кератин - главниот протеин на ноктите, кожата и косата. Го промовира формирањето на колаген и ја подобрува еластичноста и текстурата на кожата. Цистеинот се наоѓа и во други протеини во телото, вклучително и некои дигестивни ензими.
Цистеинот помага во неутрализирање на одредени токсични материи и го штити телото од штетните ефекти на зрачењето. Тој е еден од најмоќните антиоксиданси, а неговото антиоксидантно дејство се засилува кога се зема истовремено со витамин Ц и селен.
Цистеинот е претходник на глутатион, супстанца која има заштитен ефект врз клетките на црниот дроб и мозокот од оштетување од алкохол, одредени лекови и токсични материи содржани во чадот од цигарите. Цистеинот подобро се раствора од цистинот и брзо се користи во организмот, па затоа често се користи во сложениот третман на разни болести. Оваа аминокиселина се формира во организмот од Л-метионин, со задолжително присуство на витамин Б6.
Дополнителен внес на цистеин е неопходен за ревматоиден артритис, артериски заболувања и рак. Го забрзува закрепнувањето по операции, изгореници, врзува тешки метали и растворливо железо. Оваа аминокиселина исто така го забрзува согорувањето на мастите и формирањето на мускулното ткиво.
Л-цистеинот има способност да ја уништува слузта во респираторниот тракт, поради што често се користи за бронхитис и емфизем. Ги забрзува процесите на заздравување кај респираторните заболувања и игра важна улога во активирањето на леукоцитите и лимфоцитите.
Бидејќи оваа супстанца ја зголемува количината на глутатион во белите дробови, бубрезите, црниот дроб и црвената коскена срцевина, го забавува процесот на стареење, на пример, намалувајќи го бројот на старечки дамки. Н-ацетилцистеинот е поефикасен во зголемувањето на нивото на глутатион во телото отколку цистинот или дури и самиот глутатион.
Луѓето со дијабетес треба да бидат внимателни кога земаат додатоци на цистеин бидејќи тој има способност да го инактивира инсулинот. Ако имате цистинурија, ретка генетска состојба што доведува до формирање на цистински камења, не треба да земате цистеин.
Диметилглицин
Диметилглицин е дериват на глицин, наједноставната амино киселина. Тој е составен дел на многу важни супстанции, како што се амино киселините метионин и холин, некои хормони, невротрансмитери и ДНК.
 Диметилглицин се наоѓа во мали количини во месните производи, семките и житарките. Иако нема симптоми поврзани со дефицит на диметилглицин, земањето додатоци на диметилглицин има голем број на придобивки, вклучително и подобрување на енергијата и менталните перформанси.
Диметилглицин се наоѓа во мали количини во месните производи, семките и житарките. Иако нема симптоми поврзани со дефицит на диметилглицин, земањето додатоци на диметилглицин има голем број на придобивки, вклучително и подобрување на енергијата и менталните перформанси.
Диметилглицинот исто така го стимулира имунолошкиот систем, го намалува холестеролот и триглицеридите во крвта, помага во нормализирање на крвниот притисок и нивото на гликоза, а исто така помага во нормализирање на функцијата на многу органи. Се користи и за епилептични напади.
Гама-аминобутерна киселина
Гама-аминобутерна киселина (ГАБА) функционира како невротрансмитер во централниот нервен систем во телото и е од суштинско значење за метаболизмот во мозокот. Се формира од друга аминокиселина - глутамин. Ја намалува активноста на невроните и спречува прекумерна ексцитација на нервните клетки.
Гама-аминобутерната киселина ја ублажува анксиозноста и има смирувачки ефект; може да се зема и како смирувачки, но без ризик од зависност. Оваа аминокиселина се користи во сложениот третман на епилепсија и артериска хипертензија. Бидејќи има релаксирачки ефект, се користи за лекување на сексуални дисфункции. Покрај тоа, ГАБА е пропишана за нарушување на дефицитот на внимание. Вишокот на гама-аминобутерна киселина, сепак, може да ја зголеми анксиозноста, предизвикувајќи отежнато дишење и треперење на екстремитетите.
Глутаминска киселина
Глутаминската киселина е невротрансмитер кој пренесува импулси во централниот нервен систем. Оваа амино киселина игра важна улога во метаболизмот на јаглени хидрати и промовира пенетрација на калциум преку крвно-мозочната бариера.
Оваа аминокиселина може да ја користат мозочните клетки како извор на енергија. Исто така, го неутрализира амонијакот со отстранување на атомите на азот во процесот на формирање на друга аминокиселина - глутамин. Овој процес е единствениот начин да се неутрализира амонијакот во мозокот.
Глутаминската киселина се користи во корекција на нарушувања во однесувањето кај децата, како и во третман на епилепсија, мускулна дистрофија, чиреви, хипогликемични состојби, компликации од инсулинска терапија за дијабетес мелитус и нарушувања на менталниот развој.
Глутамин
Глутаминот е аминокиселината која најчесто се наоѓа во слободна форма во мускулите. Многу лесно навлегува во крвно-мозочната бариера и во мозочните клетки преминува во глутаминска киселина и обратно, освен тоа, ја зголемува количината на гама-аминобутерна киселина, која е неопходна за одржување на нормалната функција на мозокот.
Оваа амино киселина, исто така, поддржува нормално киселинско-базната рамнотежаво организмот и здравата состојба на гастроинтестиналниот тракт, е неопходна за синтеза на ДНК и РНК.
Глутаминот е активен учесник во метаболизмот на азот. Нејзината молекула содржи два азотни атоми и се формира од глутаминска киселина со додавање на еден атом на азот. Така, синтезата на глутамин помага да се отстрани вишокот на амонијак од ткивата, првенствено од мозокот, и да се транспортира азот во телото.
Глутаминот се наоѓа во големи количини во мускулите и се користи за синтеза на протеини во клетките на скелетните мускули. Затоа, додатоците во исхраната со глутамин ги користат бодибилдерите и во различни диети, како и за спречување на губење на мускулната маса при болести како малигни неоплазми и СИДА, по операции и за време на долгорочен одмор во кревет.
Дополнително, глутаминот се користи и во третман на артритис, автоимуни болести, фиброза, гастроинтестинални заболувања, пептични улкуси и болести на сврзното ткиво.
 Оваа аминокиселина ја подобрува активноста на мозокот и затоа се користи за епилепсија, синдром на хроничен замор, импотенција, шизофренија и сенилна деменција. Л-глутаминот ја намалува патолошката желба за алкохол, затоа се користи во третманот на хроничен алкохолизам.
Оваа аминокиселина ја подобрува активноста на мозокот и затоа се користи за епилепсија, синдром на хроничен замор, импотенција, шизофренија и сенилна деменција. Л-глутаминот ја намалува патолошката желба за алкохол, затоа се користи во третманот на хроничен алкохолизам.
Глутаминот се наоѓа во многу намирници и од растително и од животинско потекло, но лесно се уништува со загревање. Спанаќот и магдоносот се добри извори на глутамин, доколку се консумираат сирови.
Додатоци во исхраната кои содржат глутамин треба да се чуваат само на суво место, во спротивно глутаминот ќе се претвори во амонијак и пироглутаминска киселина. Не земајте глутамин ако имате цироза на црниот дроб, бубрежна болест или Рејевиот синдром.
Глутатион
Глутатион, како и карнитинот, не е аминокиселина. Според својата хемиска структура, тоа е трипептид добиен во телото од цистеин, глутаминска киселина и глицин.
Глутатион е антиоксиданс. Повеќето глутатион се наоѓа во црниот дроб (дел од него се ослободува директно во крвотокот), како и во белите дробови и гастроинтестиналниот тракт.
Неопходен е за метаболизмот на јаглени хидрати, а исто така го забавува стареењето поради неговото влијание врз метаболизмот на липидите и спречува појава на атеросклероза. Недостатокот на глутатион првенствено влијае на нервниот систем, предизвикувајќи проблеми со координацијата, менталните процеси и тремор.
Количината на глутатион во телото се намалува со возраста. Во таа насока, повозрасните треба дополнително да го добијат. Сепак, пожелно е да се користат додатоци во исхраната кои содржат цистеин, глутаминска киселина и глицин - односно супстанции кои синтетизираат глутатион. Земањето N-ацетилцистеин се смета за најефикасно.
Глицин
Глицинот ја забавува дегенерацијата на мускулното ткиво, бидејќи е извор на креатин, супстанца содржана во мускулното ткиво и се користи во синтезата на ДНК и РНК. Глицинот е неопходен за синтеза нуклеински киселини, жолчни киселини и несуштински амино киселини во телото.
Тој е дел од многу антацидни лекови кои се користат за стомачни заболувања; корисен е за обновување на оштетеното ткиво, бидејќи го има во големи количини во кожата и сврзното ткиво.
Оваа аминокиселина е неопходна за нормално функционирање на централниот нервен систем и за одржување на доброто здравје на простатата. Функционира како инхибиторен невротрансмитер и на тој начин може да спречи епилептични напади.
Глицинот се користи за лекување на манично-депресивна психоза, а може да биде ефикасен и за хиперактивност. Вишокот глицин во телото предизвикува чувство на замор, но соодветната количина му дава енергија на телото. Доколку е потребно, глицинот може да се претвори во серин во телото.
Хистидин
Хистидин е есенцијална амино киселина која промовира раст и поправка на ткивото и е дел од миелинските обвивки кои штитат нервните клетки, а исто така е неопходен за формирање на црвени и бели крвни зрнца. Хистидин го штити телото од штетните ефекти на зрачењето, го промовира отстранувањето на тешките метали од телото и помага при СИДА.
Премногу висока содржина на хистидин може да доведе до стрес, па дури и до ментални нарушувања (агитација и психоза).
Несоодветното ниво на хистидин во телото ја влошува состојбата на ревматоидниот артритис и глувоста поврзана со оштетување на аудитивниот нерв. Метионинот помага да се намали нивото на хистидин во телото.
 Хистаминот, многу важна компонента на многу имунолошки реакции, се синтетизира од хистидин. Исто така, промовира сексуална возбуда. Во овој поглед, истовремената употреба на додатоци во исхраната кои содржат хистидин, ниацин и пиридоксин (неопходни за синтеза на хистамин) може да биде ефикасна за сексуални нарушувања.
Хистаминот, многу важна компонента на многу имунолошки реакции, се синтетизира од хистидин. Исто така, промовира сексуална возбуда. Во овој поглед, истовремената употреба на додатоци во исхраната кои содржат хистидин, ниацин и пиридоксин (неопходни за синтеза на хистамин) може да биде ефикасна за сексуални нарушувања.
Бидејќи хистаминот го стимулира лачењето на желудечниот сок, употребата на хистидин помага при дигестивни нарушувања поврзани со ниска киселост на желудечниот сок.
Луѓето кои страдаат од манична депресија не треба да земаат хистидин освен ако не е јасно утврден недостаток на оваа аминокиселина. Хистидин се наоѓа во оризот, пченицата и 'ржта.
Изолеуцин
Изолеуцинот е една од BCAA амино киселините и есенцијалните амино киселини неопходни за синтеза на хемоглобинот. Исто така го стабилизира и регулира нивото на шеќер во крвта и процесите на снабдување со енергија Метаболизмот на изолеуцин се јавува во мускулното ткиво.
Комбинираната употреба со изолеуцин и валин (BCAA) ја зголемува издржливоста и го промовира обновувањето на мускулното ткиво, што е особено важно за спортистите.
 Изолеуцинот е неопходен за многу ментални болести. Недостатокот на оваа амино киселина резултира со симптоми слични на хипогликемија.
Изолеуцинот е неопходен за многу ментални болести. Недостатокот на оваа амино киселина резултира со симптоми слични на хипогликемија.
Изворите на храна на изолеуцин вклучуваат бадеми, индиски ореви, пилешко, наут, јајца, риба, леќа, црн дроб, месо, 'рж, повеќето семиња и протеини од соја.
Постојат биолошки активни додатоци на храна кои содржат изолеуцин. Во овој случај, неопходно е да се одржи правилната рамнотежа помеѓу изолеуцин и две други разгранети BCAA амино киселини - леуцин и валин.
Леуцин
Леуцинот е есенцијална амино киселина, заедно со изолеуцин и валин, една од трите разгранети BCAA амино киселини. Дејствувајќи заедно, тие го штитат мускулното ткиво и се извори на енергија, а исто така промовираат реставрација на коските, кожата и мускулите, така што нивната употреба често се препорачува за време на периодот на опоравување по повредите и операциите.
Леуцинот, исто така, малку го намалува нивото на шеќер во крвта и го стимулира ослободувањето на хормонот за раст. Извори на храна на леуцин вклучуваат кафеав ориз, грав, месо, јаткасти плодови, брашно од соја и пченично брашно.
Додатоци во исхраната кои содржат леуцин се користат во комбинација со валин и изолеуцин. Тие треба да се земаат со претпазливост за да се избегне предизвикување хипогликемија. Вишокот на леуцин може да го зголеми количеството на амонијак во телото.
Лизин
Лизин е есенцијална амино киселина која е дел од речиси секој протеин. Неопходен е за нормално формирање и раст на коските кај децата, ја промовира апсорпцијата на калциум и го одржува нормалниот метаболизам на азот кај возрасните.
Оваа аминокиселина е вклучена во синтезата на антитела, хормони, ензими, формирање на колаген и поправка на ткивото. Лизин се користи за време на периодот на опоравување по операции и спортски повреди. Исто така, го намалува нивото на серумските триглицериди.
Лизинот има антивирусно дејство, особено против вирусите кои предизвикуваат херпес и акутни респираторни инфекции. При вирусни заболувања се препорачува земање суплементи кои содржат лизин во комбинација со витамин Ц и биофлавоноиди.
Недостатокот на оваа есенцијална амино киселина може да доведе до анемија, хеморагии во очното јаболко, ензимски нарушувања, раздразливост, замор и слабост, слаб апетит, бавен раст и губење на тежината, како и нарушувања на репродуктивниот систем.
Извори на храна на лизин вклучуваат сирење, јајца, риба, млеко, компири, црвено месо, соја и производи од квасец.
Метионин
 Метионинот е есенцијална аминокиселина која помага во преработката на мастите, спречувајќи нивно таложење во црниот дроб и на ѕидовите на артериите. Синтезата на таурин и цистеин зависи од количината на метионин во телото. Оваа аминокиселина го промовира варењето, обезбедува процеси на детоксикација (првенствено неутрализација на токсичните метали), ја намалува мускулната слабост, штити од изложување на зрачење и е корисна за остеопороза и хемиски алергии.
Метионинот е есенцијална аминокиселина која помага во преработката на мастите, спречувајќи нивно таложење во црниот дроб и на ѕидовите на артериите. Синтезата на таурин и цистеин зависи од количината на метионин во телото. Оваа аминокиселина го промовира варењето, обезбедува процеси на детоксикација (првенствено неутрализација на токсичните метали), ја намалува мускулната слабост, штити од изложување на зрачење и е корисна за остеопороза и хемиски алергии.
Оваа аминокиселина се користи во комплексна терапија на ревматоиден артритис и токсикоза на бременоста. Метионинот има изразено антиоксидативно дејство, бидејќи е добар извор на сулфур, кој ги инактивира слободните радикали. Се користи за Гилберт-ов синдром и дисфункција на црниот дроб. Метионинот е неопходен и за синтеза на нуклеински киселини, колаген и многу други протеини. Тоа е корисно за жени кои примаат орални хормонски контрацептиви. Метионинот го намалува нивото на хистамин во телото, што може да биде корисно при шизофренија кога количината на хистамин е покачена.
Метионинот во телото се претвора во цистеин, кој е претходник на глутатион. Ова е многу важно во случај на труење, кога се потребни големи количини на глутатион за да се неутрализираат токсините и да се заштити црниот дроб.
Извори на храна на метионин: мешунки, јајца, лук, леќа, месо, кромид, соја, семки и јогурт.
Орнитин
Орнитинот помага во ослободувањето на хормонот за раст, кој помага во согорувањето на мастите во телото. Овој ефект се засилува кога орнитин се користи во комбинација со аргинин и карнитин. Орнитинот е исто така суштински за имунолошкиот систем и функцијата на црниот дроб, учествувајќи во процесите на детоксикација и реставрацијата на клетките на црниот дроб.
Орнитинот во телото се синтетизира од аргинин и, пак, служи како претходник на цитрулин, пролин и глутаминска киселина. Високи концентрации на орнитин се наоѓаат во кожата и сврзното ткиво, така што оваа аминокиселина помага во поправка на оштетеното ткиво.
Додатоци во исхраната кои содржат орнитин не треба да се даваат на деца, бремени и доилки или на лица со историја на шизофренија.
Фенилаланин
Фенилаланин е есенцијална амино киселина. Во телото, може да се претвори во друга амино киселина - тирозин, која, пак, се користи во синтезата на два главни невротрансмитери: допамин и норепинефрин. Затоа, оваа аминокиселина влијае на расположението, ја намалува болката, ја подобрува меморијата и способноста за учење и го потиснува апетитот. Се користи во третман на артритис, депресија, менструални болки, мигрена, дебелина, Паркинсонова болест и шизофренија.
Фенилаланин се наоѓа во три форми: L-фенилаланин (природна форма и е компонента на повеќето протеини во човечкото тело), Д-фенилаланин (синтетичка форма на огледало, има аналгетски ефект), DL-фенилаланин (комбинира корисни карактеристикидве претходни форми, обично се користи за предменструален синдром.
Додатоци во исхраната кои содржат фенилаланин не треба да се даваат на бремени жени, лица со напади на анксиозност, дијабетес, висок крвен притисок, фенилкетонурија, пигментиран меланом.
Пролин
Пролинот ја подобрува состојбата на кожата со зголемување на производството на колаген и намалување на неговата загуба со возраста. Помага во обновувањето на 'рскавичните површини на зглобовите, ги зајакнува лигаментите и срцевиот мускул. За зајакнување на сврзното ткиво, пролинот најдобро се користи во комбинација со витамин Ц.
Пролинот влегува во телото главно од месни производи.
Серин
Серинот е неопходен за нормален метаболизам на масти и масни киселини, раст на мускулното ткиво и одржување на нормален имунолошки систем.
Серинот се синтетизира во телото од глицин. Како навлажнувачки агенс е вклучен во многу козметички производи и дерматолошки препарати.
Таурин
Тауринот се наоѓа во високи концентрации во срцевиот мускул, белите крвни зрнца, скелетните мускули и централниот нервен систем. Тој е вклучен во синтезата на многу други амино киселини, а исто така е главна компонента на жолчката, која е неопходна за варење на мастите, апсорпција на витамини растворливи во масти и за одржување на нормално ниво на холестерол во крвта.
Затоа, тауринот е корисен за атеросклероза, едем, срцеви заболувања, артериска хипертензија и хипогликемија. Тауринот е неопходен за нормален метаболизам на натриум, калиум, калциум и магнезиум. Го спречува отстранувањето на калиумот од срцевиот мускул и затоа помага да се спречат одредени нарушувања на срцевиот ритам. Тауринот има заштитен ефект врз мозокот, особено за време на дехидрација. Се користи во третман на анксиозност и агитација, епилепсија, хиперактивност и напади.
Додатоци во исхраната со таурин се даваат на деца со Даунов синдром и мускулна дистрофија. Во некои клиники, оваа аминокиселина е вклучена во комплексната терапија за рак на дојка. Прекумерното излачување на таурин од телото се јавува при различни состојби и метаболички нарушувања.
 Аритмии, нарушувања во формирањето на тромбоцити, кандидијаза, физички или емоционален стрес, цревни заболувања, недостаток на цинк и злоупотреба на алкохол доведуваат до недостаток на таурин во телото. Злоупотребата на алкохол, исто така, ја нарушува способноста на телото да апсорбира таурин.
Аритмии, нарушувања во формирањето на тромбоцити, кандидијаза, физички или емоционален стрес, цревни заболувања, недостаток на цинк и злоупотреба на алкохол доведуваат до недостаток на таурин во телото. Злоупотребата на алкохол, исто така, ја нарушува способноста на телото да апсорбира таурин.
Кај дијабетесот се зголемува потребата на организмот за таурин и обратно, земањето додатоци во исхраната кои содржат таурин и цистин ја намалува потребата за инсулин. Тауринот се наоѓа во јајцата, рибата, месото, млекото, но не се наоѓа во растителните протеини.
Се синтетизира во црниот дроб од цистеин и од метионин во другите органи и ткива на телото, под услов да има доволна количина на витамин Б6. Во случај на генетски или метаболички нарушувања кои ја попречуваат синтезата на таурин, неопходно е да се земе додаток во исхраната со оваа аминокиселина.
Треонин
Треонин е есенцијална амино киселина која помага во одржување на нормален метаболизам на протеините во телото. Тој е важен за синтезата на колаген и еластин, му помага на црниот дроб и е вклучен во метаболизмот на мастите во комбинација со аспарагинската киселина и метионин.
Треонинот се наоѓа во срцето, централниот нервен систем, скелетните мускули и го спречува таложењето на мастите во црниот дроб. Оваа аминокиселина го стимулира имунолошкиот систем бидејќи го промовира производството на антитела. Треонинот се наоѓа во многу мали количини во житарките, така што вегетаријанците имаат поголема веројатност да имаат недостаток на оваа аминокиселина.
Триптофан
Триптофанот е есенцијална аминокиселина потребна за производство на ниацин. Се користи за синтеза на серотонин, еден од најважните невротрансмитери, во мозокот. Триптофанот се користи за несоница, депресија и за стабилизирање на расположението.
Помага при нарушување на хиперактивноста кај децата, се користи за срцеви заболувања, за контрола на телесната тежина, намалување на апетитот, а исто така и за зголемување на ослободувањето на хормонот за раст. Помага при напади на мигрена, помага во намалување на штетните ефекти на никотинот. Недостатокот на триптофан и магнезиум може да ги зголеми спазмите на коронарните артерии.
Најбогатите извори на храна на триптофан вклучуваат кафеав ориз, селско сирење, месо, кикирики и протеин од соја.
Тирозин
Тирозин е претходник на невротрансмитерите норепинефрин и допамин. Оваа амино киселина е вклучена во регулирањето на расположението; недостатокот на тирозин доведува до недостаток на норепинефрин, што пак води до депресија. Тирозин го потиснува апетитот, помага да се намали складирањето на маснотии, го промовира производството на мелатонин и ја подобрува функцијата на надбубрежните жлезди, тироидната жлезда и хипофизата.
Тирозин е исто така вклучен во метаболизмот на фенилаланин. Тироидните хормони се формираат кога атоми на јод се додаваат на тирозин. Затоа, не е изненадувачки што нискиот плазматски тирозин е поврзан со хипотироидизам.
Симптомите на дефицит на тирозин, исто така, вклучуваат низок крвен притисок, ниска температурасиндром на тело и немирни нозе.
 Додатоци во исхраната со тирозин се користат за ублажување на стресот и се верува дека помагаат при синдром на хроничен замор и нарколепсија. Се користат за анксиозност, депресија, алергии и главоболки, како и за одвикнување од дрога. Тирозин може да биде корисен при Паркинсонова болест. Природни извори на тирозин вклучуваат бадеми, авокадо, банани, млечни производи, семки од тиква и сусам.
Додатоци во исхраната со тирозин се користат за ублажување на стресот и се верува дека помагаат при синдром на хроничен замор и нарколепсија. Се користат за анксиозност, депресија, алергии и главоболки, како и за одвикнување од дрога. Тирозин може да биде корисен при Паркинсонова болест. Природни извори на тирозин вклучуваат бадеми, авокадо, банани, млечни производи, семки од тиква и сусам.
Тирозин може да се синтетизира од фенилаланин во човечкото тело. Додатоци во исхраната со фенилаланин најдобро се земаат пред спиење или со храна која содржи големи количини на јаглени хидрати.
За време на третманот со инхибитори на моноамин оксидаза (обично препишани за депресија), треба речиси целосно да избегнувате храна што содржи тирозин и да не земате додатоци во исхраната со тирозин, бидејќи тоа може да доведе до неочекуван и нагло зголемување на крвниот притисок.
Валин
Валинот е есенцијална аминокиселина со стимулирачки ефект, една од BCAA амино киселините и затоа може да се користи од мускулите како извор на енергија. Валинот е неопходен за мускулен метаболизам, поправка на оштетените ткива и за одржување на нормален метаболизам на азот во телото.
Валин често се користи за да се коригираат сериозните недостатоци на аминокиселини кои произлегуваат од зависноста од дрога. Претерано е високо нивово телото може да доведе до симптоми како што се парестезија (сензација на иглички) па дури и халуцинации.
Валинот се наоѓа во следните намирници: житарици, месо, печурки, млечни производи, кикирики, протеин од соја.
Додатокот на валин треба да биде избалансиран со другите аминокиселини со разгранет ланец BCAA L-леуцин и L-изолеуцин.
1. Амино киселини изложба амфотерични својства и киселини и амини, како и специфични својства поради заедничкото присуство на овие групи. ВО водени раствориАМА постојат како внатрешни соли (биполарни јони). Водни раствори на моноаминомоно карбоксилни киселиниНеутрален до лакмусов тест, бидејќи нивните молекули содржат еднаков број на -NH 2 - и -COOH групи. Овие групи комуницираат едни со други за да формираат внатрешни соли:
Таквата молекула има спротивни полнежи на две места: позитивен NH 3 + и негативен на карбоксил –COO -. Во овој поглед, внатрешната сол на АМК се нарекува биполарен јон или Цвитер јон (Цвитер - хибрид).
Биполарен јон во кисела средина се однесува како катјон, бидејќи дисоцијацијата на карбоксилната група е потисната; во алкална средина - како анјон. Постојат pH вредности специфични за секоја амино киселина, во која бројот на анјонски форми во растворот е еднаков на бројот на катјонски форми. рН вредноста при која вкупниот полнеж на молекулата АМК е 0 се нарекува изоелектрична точка на АМК (pI AA).
Водните раствори на моноаминодикарбоксилни киселини имаат кисела реакција:
HOOC-CH 2 -CH-COOH « - OOC-CH 2 -CH–COO - + H +
Изоелектричната точка на моноаминодикарбоксилните киселини е во кисела средина и таквите АМА се нарекуваат кисели.
Диаминомонокарбоксилните киселини имаат основни својства во водени раствори (мора да се покаже учеството на водата во процесот на дисоцијација):
NH 2 -(CH 2) 4 -CH-COOH + H 2 O « NH 3 + -(CH 2) 4 -CH–COO - + OH -
Изоелектричната точка на диаминомонокарбоксилните киселини е на pH>7 и таквите АМА се нарекуваат базни.
Како биполарни јони, амино киселините покажуваат амфотерични својства: тие се способни да формираат соли и со киселини и со бази:
Интеракција хлороводородна киселина HCl произведува сол:
R-CH-COOH + HCl ® R-CH-COOH
NH 2 NH 3 + Cl -
Интеракцијата со база доведува до формирање на сол:
R-CH(NH2)-COOH + NaOH® R-CH(NH2)-COONa + H2O
2. Формирање на комплекси со метали– хелатен комплекс. Структурата на бакарната сол на гликол (глицин) може да се претстави со следнава формула:

Речиси целиот бакар достапен во човечкото тело (100 mg) се врзува за протеините (амино киселини) во форма на овие стабилни соединенија во облик на канџи.
3. Слично на другите киселини амино киселините формираат естри, халогени анхидриди, амиди.
4. Реакции на декарбоксилацијасе јавуваат во телото со учество на специјални ензими декарбоксилаза: добиените амини (триптамин, хистамин, серотинин) се нарекуваат биогени амини и се регулатори на голем број физиолошки функции на човечкото тело.
5. Интеракција со формалдехид(алдехиди)
R-CH-COOH + H 2 C=O ® R-CH-COOH
Формалдехидот ја врзува групата NH 2, групата -COOH останува слободна и може да се титрира со алкали. Затоа, оваа реакција се користи за квантитативно определување на амино киселините (метод Соренсен).
6. Интеракција азотна киселина доведува до формирање на хидрокси киселини и ослободување на азот. Врз основа на волуменот на ослободениот азот N2, се одредува неговата квантитативна содржина во предметот што се проучува. Оваа реакција се користи за квантитативно определување на амино киселините (метод Ван-Слајк):
R-CH-COOH + HNO 2 ® R-CH-COOH + N 2 + H 2 O
Ова е еден од начините за деаминирање на АМК надвор од телото
7. Ацилација на амино киселини.Амино групата на АМК може да се ацилира со киселински хлориди и анхидриди веќе на собна температура.
Производот на снимената реакција е ацетил-α-аминопропионска киселина.
Ацилните деривати на АМК се широко користени во проучувањето на нивната секвенца во протеините и во синтезата на пептидите (заштита на амино групата).
8.Специфични својствареакции поврзани со присуството и меѓусебно влијаниеамино и карбоксилни групи - формирање на пептиди. Заеднички имота-АМК е процес на поликондензација, што доведува до формирање на пептиди. Како резултат на оваа реакција, амидните врски се формираат на местото на интеракција помеѓу карбоксилната група на една АМК и амино групата на друга АМК. Со други зборови, пептидите се амиди формирани како резултат на интеракцијата на амино групи и карбоксили на амино киселини. Амидната врска во таквите соединенија се нарекува пептидна врска (објаснете ја структурата на пептидната група и пептидна врска: три-централен p,p-конјугат систем)
Во зависност од бројот на аминокиселински остатоци во молекулата, се разликуваат ди-, три-, тетрапептиди итн. до полипептиди (до 100 AMK остатоци). Олигопептидите содржат од 2 до 10 AMK остатоци, протеините содржат повеќе од 100 AMK остатоци Општо земено, полипептидниот синџир може да се претстави со дијаграмот:
H 2 N-CH-CO-NH-CH-CO-NH-CH-CO-... -NH-CH-COOH
Каде што R 1, R 2, ... R n се радикали на аминокиселини.
Концепт на протеини.
Најважните биополимери на амино киселините се протеините - протеините. Во човечкото тело има околу 5 милиони. разни протеини кои ја сочинуваат кожата, мускулите, крвта и другите ткива. Протеините (протеините) го добиле своето име од грчки збор„Протос“ - прво, најважно. Протеините извршуваат низа важни функции во организмот: 1. Градежна функција; 2. Транспортна функција; 3. Заштитна функција; 4. Каталитичка функција; 5. Хормонална функција; 6. Нутритивна функција.
Сите природни протеини се формираат од мономери на аминокиселини. Кога протеините се хидролизираат, се формира мешавина од АМК. Има 20 од овие АМК.
4. Илустративен материјал:презентација
5. Литература:
Главна литература:
1. Биоорганска хемија: учебник. Тјукавкина Н.А., Бауков Ју.И. 2014 година
- Сеитембетов Т.С. Хемија: учебник - Алмати: EVERO LLP, 2010. - 284 стр.
- Болисбекова С. М. Хемија на биогени елементи: упатство- Семи, 2012. - 219 стр. : тиња
- Веренцова Л.Г. Неорганска, физичка и колоидна хемија: учебник - Алмати: Еверо, 2009. - 214 стр. : болен.
- Физичка и колоидна хемија / Изменето од А.П. Бељаев. - М.: ГЕОТАР МЕДИА, 2008 година
- Веренцева Л.Г. Неорганска, физичка и колоидна хемија, (верификација тестови) 2009 г
Дополнителна литература:
- Равич-Шербо М.И., Новиков В.В. Физичка и колоидна хемија. M. 2003 година.
2. Слесарев В.И. Хемија. Основи на живата хемија. Санкт Петербург: Химиздат, 2001 година
3. Ершов Ју.А. општа хемија. Биофизичка хемија. Хемија на биогени елементи. М.: ВШ, 2003 година.
4. Асанбаева Р.Д., Илјасова М.И. Теоретска основазгради и реактивностбиолошки важна органски соединенија. Алмати, 2003 година.
- Водич за лабораториски часови по биоорганска хемија, ед. НА. Тјукавкина. М., Бустард, 2003 година.
- Глинка Н.Л. Општа хемија. М., 2003 година.
- Пономарев В.Д. Аналитичка хемијаДел 1.2 2003 година
6. Контролни прашања (Повратни информации):
1. Што ја одредува структурата на полипептидниот синџир како целина?
2. До што води денатурацијата на протеините?
3. Како се нарекува изоелектричната точка?
4. Кои амино киселини се нарекуваат есенцијални?
5. Како се формираат протеините во нашето тело?
Поврзани информации.
Хемиското однесување на амино киселините се одредува со две функционални групи - NH 2 и -COOH. Амино киселините се карактеризираат со реакции на амино групата, карбоксилната група и на радикалниот дел, а во зависност од реагенсот, интеракцијата на супстанциите може да се случи преку еден или повеќе реакциони центри.
Амфотерична природа на амино киселините.Имајќи и кисела и базна група во молекулата, амино киселините во водените раствори се однесуваат како типични амфотерични соединенија. Во киселите раствори тие покажуваат основни својства, реагирајќи како бази, во алкални раствори - како киселини, односно формирајќи две групи на соли:
Поради нивната амфотерна природа во живиот организам, аминокиселините играат улога на пуферски супстанции кои одржуваат одредена концентрација на водородни јони. Пуферните раствори добиени со интеракција на амино киселини со силни бази се широко користени во биоорганската и хемиската практика. Солите на амино киселините со минералните киселини се порастворливи во вода отколку слободните амино киселини. Солите со органски киселини се малку растворливи во вода и се користат за идентификување и одвојување на амино киселините.
Реакции предизвикани од амино групата.Со учество на амино групата, амино киселините формираат соли на амониум со киселини, се ацилираат, алкилираат , реагираат со азотна киселина и алдехиди според следната шема:

Алкилацијата се изведува со учество на R-Ha1 или Ar-Hal:

Во реакцијата на ацилација, се користат киселински хлориди или киселински анхидриди (ацетил хлорид, оцетен анхидрид, бензилоксикарбонил хлорид):

Реакциите на ацилација и алкилација се користат за заштита на NH 2 групата на амино киселини за време на синтезата на пептидите.
Реакции предизвикани од карбоксилна група.Со учество на карбоксилната група, амино киселините формираат соли, естри, амиди и киселински хлориди во согласност со шемата претставена подолу:

Ако кај -јаглеродниот атом во јаглеводородниот радикал постои супституент што повлекува електрони (NO 2, CC1 3, COOH, COR итн.), што ја поларизира врската CCOOH, тогаш карбоксилните киселини лесно се подложуваат реакции на декарбоксилација. Декарбоксилацијата на α-амино киселините кои содржат + NH 3 група како супституент доведува до формирање на биогени амини. Во жив организам, овој процес се јавува под дејство на ензимот декарбоксилаза и витамин пиридоксал фосфат.
Во лабораториски услови, реакцијата се изведува со загревање на α-амино киселината во присуство на апсорбери на CO 2, на пример, Ba(OH) 2.

Декарбоксилацијата на -фенил--аланин, лизин, серин и хистидин произведува фенамин, 1,5-диаминопентан (кадаверин), 2-аминоетанол-1 (коламин) и триптамин, соодветно.
Реакции на амино киселини кои вклучуваат странична група.Кога аминокиселината тирозин се нитрира со азотна киселина, се формира соединение со дериват на динитро, обоена во портокалова боја (тест за ксантопротеин):

Редокс транзициите се случуваат во системот цистеин-цистин:
2 НС CH 2 CH(NH 2)COOH HOOCCH(NH 2)CH 2 С-С CH2CH(NH2)COOH
HOOCCH(NH 2)CH 2 С– С CH 2 CH(NH 2)COOH 2 НС CH2CH(NH2)COOH
Во некои реакции, амино киселините реагираат на двете функционални групи истовремено.
Формирање на комплекси со метали.Речиси сите α-амино киселини формираат комплекси со двовалентни метални јони. Најстабилни се сложените внатрешни бакарни соли (хелатни соединенија), формирани како резултат на интеракција со бакар (II) хидроксид и обоени сино:

Дејство на азотна киселинана алифатични амино киселини води доформирање на хидрокси киселини и ароматични - диазо соединенија.
Формирање на хидрокси киселини:

Реакција на дијазотизација:

со ослободување на молекуларен азот N 2:

2. без ослободување на молекуларен азот N2:

Хромофорската група на азобензен -N=N во азо-соединенијата предизвикува жолта, жолта, портокалова или други бои на супстанции кога се апсорбираат во видливиот регион на светлината (400-800 nm). Аксохромна група
COOH ја менува и ја подобрува бојата поради π, π - конјугација со π - електронски системглавната група на хромофорот.
Односот на амино киселините со топлината.Кога се загреваат, амино киселините се распаѓаат за да формираат различни производи во зависност од нивниот тип. Кога се загрева -амино киселиникако резултат на интермолекуларна дехидрација, се формираат циклични амиди - дикетопиперазини :

дериват на валин (Val) диизопропил
дикетопиперазин
Кога се загрева -амино киселини Амонијакот се одвојува од нив за да формира α, β-незаситени киселини со конјугиран систем на двојни врски:
β-аминовалеринска киселина пентен-2-оична киселина
(3-аминопентаноична киселина)
Греење - И -амино киселини придружено со интрамолекуларна дехидрација и формирање на внатрешни циклични амиди – лактами:

γ-аминоизовалерична киселина γ-аминоизовалерична лактам
(4-амино-3-метилбутаноична киселина) киселини