Ι. Κατά αριθμό λειτουργικές ομάδες
Μονοαμινομονο καρβοξυλικά οξέα
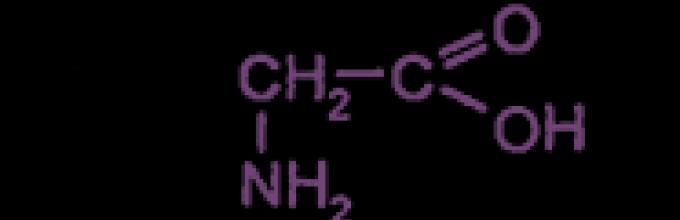
απλούστερος εκπρόσωπος:

Μονοαμινοδικαρβοξυλικά οξέα

Για παράδειγμα:

Διαμινομονοκαρβοξυλικά οξέα

Για παράδειγμα:

II. Σύμφωνα με τη σχετική θέση των καρβοξυλικών και αμινομάδων
-α-αμινοξέα

- β-αμινοξέα

- γ-αμινοξέα

Τύποι και ονόματα ορισμένων α-αμινοξέων, τα υπολείμματα των οποίων αποτελούν μέρος πρωτεϊνών

Οι πρωτεΐνες είναι φυσικά πολυμερή, τα μακρομόρια των οποίων είναι κατασκευασμένα από μεγάλος αριθμόςυπολείμματα 20 διαφορετικών α-αμινοξέων. Στη βιοχημεία, για τα αμινοξέα χρησιμοποιούνται συνήθως σύντομα, ασήμαντα ονόματα και ονομασίες με τρία γράμματα.
Μονοαμινομονοκαρβοξυλικά οξέα
|
Αμινοαιθανοϊκό ή αμινοξικό οξύ ή γλυκίνη (γλυκοκόλη) |
|
|
2-αμινοπροπανοϊκό ή α-αμινοπροπιονικό οξύ ή αλανίνη |
|
|
2-αμινο-3-υδροξυπροπανοϊκό ή α-αμινο-β-υδροξυπροπιονικό οξύ ή σερίνη |
|
|
2-αμινο-3-μερκαπτοπροπανοϊκό οξύ, ή β-μερκαπτοαλανίνη, ή κυστεΐνη |
|
|
2-αμινο-3-φαινυλπροπανοϊκό οξύ, ή β-φαινυλαλανίνη ή φαινυλαλανίνη |
|
|
2-αμινο-3-(4-υδροξυφαινυλ)-προπανοϊκό οξύ, ή β-(n-υδροξυφαινυλ)-απανίνη, ή τυροσίνη |
|
|
2-αμινο-3-μεθυλοβουτανοϊκό οξύ ή α-αμινοϊσοβαλερικό οξύ ή βαλίνη |
Μονοαμινοδικαρβοξυλικά οξέα
Διαμινομονοκαρβοξυλικό οξύ
Ταξινόμηση φυσικών αμινοξέων
I. Αντικαταστάσιμα αμινοξέα - μπορούν να συντεθούν στο ανθρώπινο σώμα. Αυτά περιλαμβάνουν μεταξύ των παραπάνω: γλυκίνη, αλανίνη, σερίνη, κυστεΐνη, τυροσίνη, ασπαρτικό και γλουταμικό οξύ.
II. Τα απαραίτητα αμινοξέα δεν μπορούν να συντεθούν στο ανθρώπινο σώμα και πρέπει να παρέχονται στον οργανισμό ως μέρος των πρωτεϊνών των τροφίμων. Η φαινυλαλανίνη, η βαλίνη, η λυσίνη δεν είναι αντιπροσωπευτικές μη απαραίτητα αμινοξέα.
Φυσικές ιδιότητες
Τα περισσότερα αμινοξέα είναι άχρωμα κρυσταλλικές ουσίες, πολύ διαλυτό στο νερό. Πολλά αμινοξέα έχουν γλυκιά γεύση. Τα σημεία τήξης διαφορετικών αμινοξέων κυμαίνονται από 230-300°C.
Χημικές ιδιότητες
Τα αμινοξέα είναι αμφοτερικές ενώσεις, το οποίο οφείλεται στην παρουσία στα μόριά τους λειτουργικών ομάδων όξινης (-COOH) και βασικής (-NH 2) φύσης.
1. Αλληλεπίδραση με βάσεις

2. Αλληλεπίδραση με οξέα

3. Σχηματισμός εσωτερικών αλάτων (διπολικά ιόντα)
Στα υδατικά διαλύματα, τα αμινοξέα υπάρχουν με τη μορφή μιγμάτων ισορροπίας μορίων και διπολικών ιόντων, τα οποία σε όξινο περιβάλλον μετατρέπονται σε κατιονική μορφή και σε αλκαλικό περιβάλλον σε ανιονική μορφή.
α) Μονοαμινομονοκαρβοξυλικά οξέα

Όταν σχηματίζονται εσωτερικά άλατα μονοαμινομονοκαρβοξυλικών οξέων, η φύση του μέσου δεν αλλάζει. Επομένως, αυτά τα αμινοξέα ονομάζονται ουδέτερα. Το συνολικό φορτίο των εσωτερικών αλάτων τέτοιων οξέων είναι μηδέν.
Όταν προστίθεται ένα οξύ (Η+), το καρβοξυλικό ιόν πρωτονιώνεται αφήνοντας μόνο ένα θετικό φορτίο στην ομάδα -ΝΗ
β) Μονοαμινοδικαρβοξυλικά οξέα

Όταν σχηματίζονται εσωτερικά άλατα μονοαμινοδικαρβοξυλικών οξέων, σχηματίζεται περίσσεια ιόντων υδρογόνου, επομένως υδατικά διαλύματααυτά τα οξέα έχουν pH
γ) Διαμινομονοκαρβοξυλικά οξέα

Όταν σχηματίζονται εσωτερικά άλατα διαμινομονοκαρβοξυλικών οξέων, σχηματίζεται περίσσεια ιόντων υδροξειδίου, άρα τα υδατικά διαλύματά τους έχουν pH > 7. Τέτοια αμινοξέα ονομάζονται βασικά. Το συνολικό φορτίο των εσωτερικών αλάτων των βασικών αμινοξέων είναι θετικό.
4. Σχηματισμός πεπτιδίων
Όταν η καρβοξυλική ομάδα ενός μορίου αμινοξέος αλληλεπιδρά με την αμινομάδα ενός άλλου μορίου αμινοξέος, σχηματίζονται διπεπτίδια:

Όταν δύο διαφορετικά αμινοξέα αλληλεπιδρούν, σχηματίζεται ένα μείγμα τεσσάρων διπεπτιδίων. Για παράδειγμα:

Ένα διπεπτίδιο, προσθέτοντας ένα άλλο μόριο αμινοξέος, μπορεί να σχηματίσει ένα τριπεπτίδιο. Ομοίως, ένα τετραπεπτίδιο μπορεί να ληφθεί από ένα τριπεπτίδιο, κ.λπ.
5. Σχηματισμός παραγώγων στην καρβοξυλομάδα
Όπως τα καρβοξυλικά οξέα, τα αμινοξέα μπορούν να σχηματίσουν εστέρες, χλωρίδια οξέων κ.λπ. Για παράδειγμα:

6. Πολυσυμπύκνωση ε-αμινοκαπροϊκού οξέος

Μέθοδοι απόκτησης
1. Αμμωνόλυση α-αλογονοκαρβοξυλικών οξέων
2. Υδρόλυση πρωτεϊνών
Τα αμινοξέα περιέχουν αμινο και καρβοξυλομάδες και παρουσιάζουν όλες τις ιδιότητες που είναι χαρακτηριστικές ενώσεων με τέτοιες λειτουργικές ομάδες. Όταν γράφετε αντιδράσεις αμινοξέων, χρησιμοποιούνται τύποι με μη ιονισμένες αμινο και καρβοξυ ομάδες.
1) αντιδράσεις στην αμινομάδα. Η αμινομάδα στα αμινοξέα εμφανίζει τις συνήθεις ιδιότητες των αμινών: οι αμίνες είναι βάσεις και δρουν ως πυρηνόφιλα στις αντιδράσεις.
1. Αντίδραση αμινοξέων ως βάσεων. Όταν τα αμινοξέα αλληλεπιδρούν με τα οξέα, σχηματίζονται άλατα αμμωνίου:
υδροχλωρική γλυκίνη, υδροχλωρικό άλας γλυκίνης
2. Δράση του νιτρώδους οξέος. Όταν δρα το νιτρώδες οξύ, σχηματίζονται υδροξυοξέα και απελευθερώνεται άζωτο και νερό:
Αυτή η αντίδραση χρησιμοποιείται για τον ποσοτικό προσδιορισμό ομάδων ελεύθερων αμινών σε αμινοξέα, καθώς και σε πρωτεΐνες.
3. Σχηματισμός παραγώγων Ν-ακυλίου, αντίδραση ακυλίωσης.
Τα αμινοξέα αντιδρούν με ανυδρίτες και αλογονίδια οξέων, σχηματίζοντας Ν-ακυλο παράγωγα αμινοξέων:
Βενζυλαιθέρα νατριούχο άλας Ν καρβοβενζοξυγλυκίνη - χλωροφορμική γλυκίνη
Η ακυλίωση είναι ένας από τους τρόπους προστασίας της αμινομάδας. Τα παράγωγα Ν-ακυλίου έχουν μεγάλης σημασίαςστη σύνθεση πεπτιδίων, αφού τα παράγωγα Ν-ακυλίου υδρολύονται εύκολα για να σχηματίσουν μια ελεύθερη αμινομάδα.
4. Σχηματισμός βάσεων Schiff. Όταν τα α-αμινοξέα αλληλεπιδρούν με αλδεΰδες, σχηματίζονται υποκατεστημένες ιμίνες (βάσεις Schiff) μέσω του σταδίου σχηματισμού των καρβινολαμινών:
παράγωγο αλανίνης φορμαλδεΰδης Ν-μεθυλόλης της αλανίνης
5. Αντίδραση αλκυλίωσης. Η αμινομάδα στο α-αμινοξύ αλκυλιώνεται για να σχηματίσει παράγωγα Ν-αλκυλίου:
Υψηλότερη τιμήέχει αντίδραση με 2,4 - δινιτροφθοροβενζόλιο. Τα προκύπτοντα παράγωγα δινιτροφαινυλίου (παράγωγα DNP) χρησιμοποιούνται για τον καθορισμό της αλληλουχίας αμινοξέων πεπτιδίων και πρωτεϊνών. Η αλληλεπίδραση α-αμινοξέων με 2,4-δινιτροφθοροβενζόλιο είναι ένα παράδειγμα αντίδρασης πυρηνόφιλης υποκατάστασης στον δακτύλιο βενζολίου. Λόγω της παρουσίας δύο ισχυρών ομάδων που αποσύρουν ηλεκτρόνια στον δακτύλιο βενζολίου, το αλογόνο γίνεται κινητό και υφίσταται μια αντίδραση υποκατάστασης:
 |
2.4 – δινιτρο –
φθοροβενζόλιο Ν - 2,4 - δινιτροφαινυλο - α - αμινοξύ
(DNPB) DNP - παράγωγα α - αμινοξέων
6.Αντίδραση με ισοθειοκυανικό φαινυλεστέρα. Αυτή η αντίδραση χρησιμοποιείται ευρέως για τον προσδιορισμό της δομής των πεπτιδίων. Ο ισοθειοκυανικός φαινυλεστέρας είναι ένα παράγωγο του ισοθειοκυανικού οξέος H-N=C=S. Η αλληλεπίδραση α-αμινοξέων με ισοθειοκυανικό φαινυλεστέρα προχωρά μέσω του μηχανισμού μιας πυρηνόφιλης αντίδρασης προσθήκης. Το προκύπτον προϊόν υφίσταται έπειτα μια αντίδραση ενδομοριακής υποκατάστασης, που οδηγεί στον σχηματισμό ενός κυκλικού υποκατεστημένου αμιδίου: φαινυλθειοϋδαντοΐνης.
Οι κυκλικές ενώσεις λαμβάνονται σε ποσοτική απόδοση και είναι φαινυλικά παράγωγα θειοϋδαντοΐνης (PTH - παράγωγα) - αμινοξέων. Τα παράγωγα PTG διαφέρουν ως προς τη δομή της ρίζας R.
Εκτός από τα συνηθισμένα άλατα, τα α-αμινοξέα μπορούν να σχηματίσουν, υπό ορισμένες συνθήκες, ενδοσύνθετα άλατα με κατιόντα βαριά μέταλλα. Όλα τα α-αμινοξέα χαρακτηρίζονται από όμορφα κρυσταλλοποιούμενα, έντονα μπλε χρώματος ενδοσύνθετα (χηλικά) άλατα χαλκού:
Αιθυλεστέρας αλανίνης
Ο σχηματισμός εστέρων είναι μία από τις μεθόδους για την προστασία της καρβοξυλικής ομάδας στη σύνθεση πεπτιδίων.
3. Σχηματισμός αλογονιδίων οξέος. Όταν δρουν σε α-αμινοξέα με προστατευμένη αμινομάδα με οξυδιχλωριούχο θείο (θειονυλοχλωρίδιο) ή τριχλωριούχο οξείδιο του φωσφόρου (οξυχλωριούχος φωσφόρος), σχηματίζονται χλωρίδια οξέος:
Η παραγωγή αλογονιδίων οξέος είναι ένας από τους τρόπους ενεργοποίησης της καρβοξυλικής ομάδας στη σύνθεση πεπτιδίων.
4.Λήψη ανυδριδίων α-αμινοξέων. Τα αλογονίδια οξέων έχουν πολύ υψηλή αντιδραστικότητα, γεγονός που μειώνει την επιλεκτικότητα της αντίδρασης κατά τη χρήση τους. Επομένως, μια πιο συχνά χρησιμοποιούμενη μέθοδος για την ενεργοποίηση μιας καρβοξυλικής ομάδας στη σύνθεση πεπτιδίων είναι η μετατροπή της σε μια ομάδα ανυδρίτη. Οι ανυδρίτες είναι λιγότερο δραστικοί από τα αλογονίδια οξέος. Όταν ένα α-αμινοξύ που έχει μια προστατευμένη αμινομάδα αλληλεπιδρά με το χλωρομυρμηκικό αιθυλεστέρα (χλωρομυρμηκικό αιθυλεστέρα), σχηματίζεται ένας δεσμός ανυδρίτη:
5. Αποκαρβοξυλίωση. α - Τα αμινοξέα που έχουν δύο ομάδες έλξης ηλεκτρονίων στο ίδιο άτομο άνθρακα αποκαρβοξυλιώνονται εύκολα. Σε εργαστηριακές συνθήκες, αυτό πραγματοποιείται με θέρμανση των αμινοξέων με υδροξείδιο του βαρίου. Αυτή η αντίδραση συμβαίνει στο σώμα με τη συμμετοχή ενζύμων αποκαρβοξυλάσης με το σχηματισμό βιογενών αμινών:
νινυδρίνη
Σχέση αμινοξέων με θερμότητα. Όταν τα α-αμινοξέα θερμαίνονται, σχηματίζονται κυκλικά αμίδια που ονομάζονται δικετοπιπεραζίνες:

Δικετοπιπεραζίνη
g - και d - Τα αμινοξέα διασπώνται εύκολα από το νερό και κυκλοποιούνται για να σχηματίσουν εσωτερικά αμίδια, λακτάμες:
g - λακτάμη (βουτυρολακτάμη)
Σε περιπτώσεις όπου οι αμινο και καρβοξυλομάδες διαχωρίζονται από πέντε ή περισσότερα άτομα άνθρακα, όταν θερμαίνονται, συμβαίνει πολυσυμπύκνωση με το σχηματισμό αλυσίδων πολυμερούς πολυαμιδίου με την εξάλειψη ενός μορίου νερού.
Τα αμινοξέα είναι οργανικά αμφοτερικές ενώσεις. Περιέχουν δύο λειτουργικές ομάδες αντίθετης φύσης στο μόριο: μια αμινομάδα με βασικές ιδιότητες και μια καρβοξυλομάδα με όξινες ιδιότητες. Τα αμινοξέα αντιδρούν τόσο με οξέα όσο και με βάσεις:
H 2 N -CH 2 -COOH + HCl → Cl [H 3 N-CH 2 -COOH],
H 2 N -CH 2 -COOH + NaOH → H 2 N-CH 2 -COONa + H 2 O.
Όταν τα αμινοξέα διαλύονται στο νερό, η καρβοξυλική ομάδα αφαιρεί ένα ιόν υδρογόνου, το οποίο μπορεί να προσκολληθεί στην αμινομάδα. Σε αυτή την περίπτωση, σχηματίζεται ένα εσωτερικό άλας, το μόριο του οποίου είναι ένα διπολικό ιόν:
H 2 N-CH 2 -COOH + H 3 N -CH 2 -COO - .
Οι μετασχηματισμοί οξέων-βάσης αμινοξέων σε διάφορα περιβάλλοντα μπορούν να παρασταθούν από το ακόλουθο γενικό διάγραμμα:

Τα υδατικά διαλύματα αμινοξέων έχουν ουδέτερο, αλκαλικό ή όξινο περιβάλλον ανάλογα με τον αριθμό των λειτουργικών ομάδων. Έτσι, το γλουταμικό οξύ σχηματίζει ένα όξινο διάλυμα (δύο ομάδες -COOH, μία -NH2), η λυσίνη σχηματίζει ένα αλκαλικό διάλυμα (μία -COOH ομάδα, δύο -NH2).
Αρέσει πρωτοταγείς αμίνες, τα αμινοξέα αντιδρούν με το νιτρώδες οξύ και η αμινομάδα μετατρέπεται σε υδροξοομάδα και το αμινοξύ σε υδροξυ οξύ:
H 2 N-CH(R)-COOH + HNO 2 → HO-CH(R)-COOH + N 2 + H 2 O
Η μέτρηση του όγκου του αζώτου που απελευθερώνεται μας επιτρέπει να προσδιορίσουμε την ποσότητα του αμινοξέος ( Μέθοδος Van Slyke).
Τα αμινοξέα μπορούν να αντιδράσουν με τις αλκοόλες παρουσία αερίου υδροχλωρίου, μετατρέποντάς τους σε αστήρ(ακριβέστερα, στο υδροχλωρικό άλας του αιθέρα):
H 2 N-CH(R)-COOH + R’OH H 2 N-CH(R)-COOR’ + H 2 O.
Οι εστέρες αμινοξέων δεν έχουν διπολική δομή και είναι πτητικές ενώσεις.
Η πιο σημαντική ιδιότητα των αμινοξέων είναι η ικανότητά τους να συμπυκνώνονται για να σχηματίσουν πεπτίδια.
Ποιοτικές αντιδράσεις.
1) Όλα τα αμινοξέα οξειδώνονται από τη νινυδρίνη

με το σχηματισμό προϊόντων χρωματισμένα μπλε-βιολετί. Το ιμινο οξύ προλίνη δίνει ένα κίτρινο χρώμα με τη νινυδρίνη. Αυτή η αντίδραση μπορεί να χρησιμοποιηθεί για τον ποσοτικό προσδιορισμό των αμινοξέων με φασματοφωτομετρία.
2) Όταν θερμαίνουμε αρωματικά αμινοξέα με συμπυκνωμένο νιτρικό οξύλαμβάνει χώρα νίτρωση του δακτυλίου βενζολίου και σχηματίζονται ενώσεις που χρωματίζονται κίτρινος. Αυτή η αντίδραση ονομάζεται ξανθοπρωτεΐνη(από το ελληνικό xanthos - κίτρινο).
Που αποδίδει σημαντικά βιολογικές λειτουργίεςσε ζωντανούς οργανισμούς, συμμετέχει στη βιοσύνθεση των πρωτεϊνών, είναι υπεύθυνο για τη φυσιολογική δραστηριότητα του νευρικού συστήματος και ρυθμίζει τις μεταβολικές διεργασίες. Το αμινοξικό οξύ, που προέρχεται τεχνητά, χρησιμοποιείται στη φαρμακευτική, την ιατρική και Βιομηχανία τροφίμων.
Το πρόσθετο τροφίμων E640 συνδυάζει κάτω από έναν αριθμό σήμανσης το αμινοοξικό οξύ (γλυκίνη) και το άλας του νατρίου - ενώσεις που χρησιμοποιούνται για τη βελτιστοποίηση της γεύσης και του αρώματος των προϊόντων. Το συμπλήρωμα είναι ασφαλές και επίσημα εγκεκριμένο στις περισσότερες χώρες του κόσμου.
Γλυκίνη και το άλας νατρίου της: γενικές πληροφορίες
Η γλυκίνη, επίσης γνωστή ως αμινοοξικό ή αμινοαιθανοϊκό οξύ, ανήκει σε μια σειρά από μη βασικά αμινοξέα - τις απλούστερες οργανικές δομές που αποτελούν μέρος των πρωτεϊνών και των ενώσεων τους. Η ουσία, που λαμβάνεται τεχνητά, είναι μια άχρωμη, άοσμη σκόνη και έχει γλυκιά γεύση.
Σε βιομηχανική κλίμακα, η γλυκίνη παράγεται με συνδυασμό χλωροοξικού οξέος και αμμωνίας. Το αμινοξικό οξύ, με τη σειρά του, έχει την ιδιότητα να σχηματίζει σύμπλοκα άλατα (γλυκινικά) με μεταλλικά ιόντα.
Το γλυκινικό νάτριο είναι ένα άλας νατρίου και αμινοοξικού οξέος, το οποίο είναι επίσης μια ουσία συνθετικής προέλευσης. Παρά το γεγονός ότι η γλυκίνη και το άλας της είναι διαφορετικές χημικές ενώσεις, στη βιομηχανία τροφίμων επιτελούν πανομοιότυπες λειτουργίες ως τροποποιητές γεύσης και αρώματος, συνδυάζονται κάτω από έναν αριθμό ετικέτας και θεωρούνται ως πρόσθετο Ε640.
| Ονομα | Γλυκίνη |
|---|---|
| Συνώνυμα | Αμινοοξικό (αμινοαιθανοϊκό) οξύ, γλυκόλη (απαρχαιωμένη) |
| Ομάδα | Μη απαραίτητα αμινοξέα |
| Χημική φόρμουλα | NH 2 – CH 2 – COOH |
| Δομή | Λεπτοί μονοκλινικοί κρύσταλλοι (κρυσταλλική σκόνη) |
| Χρώμα | Λευκό (άχρωμο) |
| Μυρωδιά | Απών |
| Γεύση | Γλυκός |
| Διαλυτότητα | Πλήρως διαλυτό σε, μερικώς διαλυτό σε. Δεν διαλύεται σε αιθέρα |
| Προσθετικός κωδικός | E640 (συμπεριλαμβανομένου του αλατιού νατρίου) |
| Προέλευση | Συνθετικός |
| Τοξικότητα | Ασφαλές όταν καταναλώνεται εντός κανονικών ορίων |
| Τομείς χρήσης | Βιομηχανία τροφίμων, φαρμακευτικά προϊόντα, ιατρική, κοσμετολογία |
Βιολογικός ρόλος της γλυκίνης και οι πηγές της
Η γλυκίνη βρίσκεται στα πρωτεϊνικά μόρια πολύ πιο συχνά από άλλα αμινοξέα και εκτελεί σημαντικές βιολογικές λειτουργίες. Στο ανθρώπινο σώμα, αυτό το αμινοξύ συντίθεται με τρανσαμίνωση (αναστρέψιμη μεταφορά της αμινομάδας) γλυοξυλικού ή ενζυματική διάσπαση χολίνης και σερίνης.
Το αμινοξικό οξύ είναι πρόδρομος των πορφυρινών και των πουρινών, η βιοσύνθεση των οποίων συμβαίνει σε ζωντανά κύτταρα, ωστόσο βιολογικό ρόλοΑυτή η σύνδεση δεν περιορίζεται σε αυτές τις λειτουργίες. Η γλυκίνη είναι επίσης ένας νευροδιαβιβαστής που εμπλέκεται στη μετάδοση των νευρικών ερεθισμάτων, ρυθμίζει την παραγωγή άλλων αμινοξέων και έχει «ανασταλτική» επίδραση στους νευρώνες και τους κινητικούς νευρώνες.
Το σώμα ενός υγιούς ατόμου συνθέτει ανεξάρτητα αμινοξέα στις απαιτούμενες ποσότητες, επομένως δεν υπάρχει, κατά κανόνα, ανάγκη χρήσης τους σε φάρμακα και συμπληρώματα διατροφής. Οι πηγές τροφίμων αμινοοξικού οξέος περιλαμβάνουν ζωικά προϊόντα (βοδινό συκώτι), ξηρούς καρπούς και ορισμένα φρούτα.
Η επίδραση της γλυκίνης και του άλατος νατρίου της στον ανθρώπινο οργανισμό
Το αμινοοξικό οξύ ως νευροδιαβιβαστής εκτελεί ρυθμιστικές λειτουργίες και επηρεάζει κυρίως το κεντρικό και το περιφερικό νευρικό σύστημα. Η γλυκίνη έχει νοοτροπικές ιδιότητες, ομαλοποιεί το μεταβολισμό, ενεργοποιεί τις προστατευτικές λειτουργίες του κεντρικού νευρικού συστήματος και έχει μια ήπια ηρεμιστική δράση.
Θετικές επιδράσεις της γλυκίνης στον ανθρώπινο οργανισμό:
- μείωση συναισθηματικής έντασης, άγχους, στρες, επιθετικότητας.
- βελτιωμένη διάθεση και ομαλοποίηση του ύπνου.
- χαλάρωση των μυών και ανακούφιση από κράμπες.
- αυξημένη απόδοση?
- αποδυνάμωση παρενέργειεςλήψη ψυχοφαρμάκων?
- μείωση της σοβαρότητας των φυτοαγγειακών διαταραχών.
- μείωση της λαχτάρας για αλκοόλ και γλυκά.
Ως μέρος του συμπληρώματος E640, η γλυκίνη και το άλας της δεν έχουν τις παραπάνω ιδιότητες και δεν έχουν ούτε θετικές ούτε αρνητικές επιπτώσεις στον ανθρώπινο οργανισμό όταν καταναλώνονται εντός των φυσιολογικών ορίων. Το πρόσθετο τροφίμων δεν αποτελεί απειλή για την υγεία, αλλά σε περίπτωση ατομικής δυσανεξίας μπορεί να προκαλέσει αλλεργική αντίδραση.
Πιθανοί κίνδυνοι μπορεί να προέρχονται από ακαθαρσίες στο πρόσθετο και προϊόντα διατροφής χαμηλής ποιότητας, για την παρασκευή των οποίων χρησιμοποιούνται βελτιστοποιητές γεύσης και αρώματος.
Εφαρμογή της γλυκίνης και του άλατος νατρίου της
Οι εφαρμογές της γλυκίνης και του γλυκινικού νατρίου περιορίζονται κυρίως στη βιομηχανία τροφίμων, την ιατρική και τα φαρμακευτικά προϊόντα. Ωστόσο, το αμινοοξικό οξύ έχει βρει εφαρμογή και στη βιομηχανία καλλυντικών λόγω της υποαλλεργικότητας και της αντιοξειδωτικής του δράσης.
Καλλυντικά που περιέχουν το πρόσθετο E640:
- φαρμακευτικά σαμπουάν για εξασθενημένα μαλλιά και προϊόντα κατά της φαλάκρας.
- αντιγηραντικά καλλυντικά, ενυδατικές κρέμες και μάσκες για όλους τους τύπους δέρματος.
- οροί καθαρισμού και τόνερ.
- κραγιόν και βάλσαμα.
Τα θρυμματισμένα δισκία γλυκίνης μπορούν να χρησιμοποιηθούν για την παρασκευή σπιτικών προϊόντων περιποίησης δέρματος και να προστεθούν σε ενυδατικές μάσκες και κρέμες. Το αμινοοξικό οξύ προάγει τη διείσδυση πολύτιμων θρεπτικών συστατικών στα βαθιά στρώματα του χορίου και ενισχύει την επίδραση των φαρμακευτικών καλλυντικών.
Πρόσθετο E640 στη βιομηχανία τροφίμων
 Η γλυκίνη και το γλυκινικό νάτριο χρησιμοποιούνται ενεργά σε τεχνολογικές διαδικασίεςπαραγωγή αλκοολούχων ποτών. Το πρόσθετο E640, συγκεκριμένα, περιλαμβάνεται στην ελίτ βότκα, η οποία βοηθά στην εξουδετέρωση της δυσάρεστης οσμής και στην απαλότητα της τραχιάς γεύσης. Υπάρχει επίσης η άποψη ότι η παρουσία γλυκίνης στα αλκοολούχα ποτά συμβάλλει στη μείωση της τοξικής επίδρασης του αλκοόλ στο νευρικό σύστημα και αποτρέπει το hangover.
Η γλυκίνη και το γλυκινικό νάτριο χρησιμοποιούνται ενεργά σε τεχνολογικές διαδικασίεςπαραγωγή αλκοολούχων ποτών. Το πρόσθετο E640, συγκεκριμένα, περιλαμβάνεται στην ελίτ βότκα, η οποία βοηθά στην εξουδετέρωση της δυσάρεστης οσμής και στην απαλότητα της τραχιάς γεύσης. Υπάρχει επίσης η άποψη ότι η παρουσία γλυκίνης στα αλκοολούχα ποτά συμβάλλει στη μείωση της τοξικής επίδρασης του αλκοόλ στο νευρικό σύστημα και αποτρέπει το hangover.
Προϊόντα διατροφής που περιέχουν το πρόσθετο Ε640:
- ισχυρά αλκοολούχα ποτά?
- μαρμελάδες, κονσέρβες, ζελέ, ?
- συσκευασμένοι χυμοί με πολτό?
- εμπλουτισμένη μαγειρική?
- αθλητικά ενισχυμένα ποτά?
- σάλτσες, καρυκεύματα και μπαχαρικά.
Το αμινοξικό οξύ χρησιμοποιείται όχι μόνο για τη βελτιστοποίηση της γεύσης και της βιολογικής μεταφοράς δραστικές ουσίες, αλλά και ως αντιβακτηριδιακός παράγοντας. Συγκεκριμένα, χρησιμοποιείται για την επεξεργασία κρέατος, ψαριών και θαλασσινών για την εξουδετέρωση του επικίνδυνου E. coli.
Ιατρική χρήση
Η γλυκίνη χρησιμοποιείται ενεργά για τη θεραπεία και την πρόληψη ασθενειών που σχετίζονται με κεντρικές και περιφερικές νευρικό σύστημα. Αυτή η ουσία αποτελεί μέρος φαρμακευτικών σκευασμάτων με νοοτροπική, ηρεμιστική, αντισπασμωδική και υπνωτική δράση και έχει ήπια αντικαταθλιπτική και ηρεμιστική δράση.
Ιατρικές ενδείξεις για τη χρήση του αμινοξικού οξέος ως φάρμακο:
- μειωμένη πνευματική απόδοση, διαταραχές ύπνου και μνήμης.
- συναισθηματική ένταση, αγχωτικές καταστάσεις, νευρώσεις.
- συναισθηματική αστάθεια και αυξημένη διεγερσιμότητα.
- συνέπειες ισχαιμικού εγκεφαλικού, τραυματικού εγκεφαλικού τραυματισμού και νευρολοιμώξεων.
- βλαστική-αγγειακή δυστονία, ισχαιμία.
- αυξημένος μυϊκός τόνος, μυϊκές κράμπες.
- εθισμός στο αλκοόλ και στα ναρκωτικά, τοξικές επιδράσεις φαρμάκων που καταστέλλουν το κεντρικό νευρικό σύστημα.
Έχει αποδειχθεί ότι η κατανάλωση 3 g γλυκίνης την ημέρα έχει θετική επίδραση στις νοητικές ικανότητες και τη γενική συναισθηματική κατάσταση ενός ατόμου, ανακουφίζει από την υπνηλία κατά τη διάρκεια της ημέρας και ομαλοποιεί τον νυχτερινό ύπνο. Το φάρμακο συνταγογραφείται επίσης σε έγκυες γυναίκες για τη μείωση του άγχους, σε παιδιά και εφήβους που αντιμετωπίζουν δυσκολίες με την κοινωνική προσαρμογή και τη συγκέντρωση.
Πρόσθετο Ε640 και νομοθεσία
Ο βελτιστοποιητής γεύσης και οσμής E640 χρησιμοποιείται στην παραγωγή τροφίμων στις περισσότερες χώρες του κόσμου, αλλά δεν υπάρχουν πληροφορίες για το πρόσθετο στον Codex Alimentarius. Δεν έχουν υπάρξει περιπτώσεις δηλητηρίασης από γλυκίνη και γλυκινικό νάτριο όταν καταναλώνονται ως τροφή, επομένως ο τροποποιητής E640 θεωρείται ασφαλής.
Το πρόσθετο περιλαμβάνεται στη λίστα των επίσημα εγκεκριμένων προϊόντων για χρήση στη βιομηχανία τροφίμων στην Ευρωπαϊκή Ένωση, τις ΗΠΑ και τον Καναδά. Νομοθεσία Ρωσική Ομοσπονδίακαι η Λευκορωσία επιτρέπει επίσης την παρουσία του E640 σε προϊόντα εντός των επιτρεπόμενων προτύπων που ορίζει η SanPiN. Δεν υπάρχουν δεδομένα για τη χρήση του E640 ως ενισχυτικού γεύσης και αρωματικού παράγοντα στην Ουκρανία.
Παρά το γεγονός ότι η γλυκίνη και το άλας της δεν έχουν τοξική επίδραση στο ανθρώπινο σώμα και είναι εγκεκριμένα για χρήση, τα προϊόντα που περιέχουν E640 δύσκολα μπορούν να χαρακτηριστούν χρήσιμα. Τα περισσότερα αρώματα και αρώματα χρησιμοποιούνται για να προσελκύσουν την προσοχή του αγοραστή σε προϊόντα χαμηλής ποιότητας, η χρήση των οποίων θα πρέπει να ελαχιστοποιηθεί.
Γλυκίνη (αμινοοξικό οξύ, γλυκόλη, Gly, G)
H2NCH2COOH
Μοριακή μάζα 75,07; άχρωμοι κρύσταλλοι? t λιώσει 232-236°C (με αποσύνθεση). εξαιρετικά διαλυτό στο νερό, αδιάλυτο στους περισσότερους οργανικούς διαλύτες. Στους 25°C p Κ α 2,34 (COOH) και 9,6 (ΝΗ2); R Εγώ 5,97.
Όσον αφορά τις χημικές ιδιότητες, η γλυκίνη είναι ένα τυπικό αλειφατικό α-αμινοξύ. Ο ποσοτικός προσδιορισμός βασίζεται στον σχηματισμό έγχρωμων προϊόντων με ο-φθαλαλδεΰδη (αντίδραση Zimmermann). Βρίσκεται πιο συχνά σε πρωτεΐνες από άλλα αμινοξέα. Χρησιμεύει ως πρόδρομος στη βιοσύνθεση ενώσεων πορφυρίνης και βάσεων πουρινών. Η γλυκίνη είναι ένα κωδικοποιημένο αμινοξύ, μη απαραίτητο. Η βιοσύνθεσή του πραγματοποιείται με τρανσαμίνωση γλυοξυλικού οξέος, ενζυματική διάσπαση σερίνης και θρεονίνης. Η λυκίνη συντίθεται από χλωροοξικό οξύ και NH3. Στο φάσμα NMR στο D 2 O, η χημική μετατόπιση των πρωτονίων της ομάδας CH 2 είναι 3,55 ppm. Το εσωτερικό άλας της γλυκίνης (CH 3) 3 + NCH 2 COO ονομάζεται βεταΐνη.
Η γλυκίνη χρησιμοποιείται για τη σύνθεση πεπτιδίων ως συστατικό ρυθμιστικά διαλύματα, αναμεμειγμένο με άλλα αμινοξέα - για παρεντερική διατροφή.