Κατά τη διάρκεια της ζωής του, ο Σκωτσέζος βοτανολόγος Ρόμπερτ Μπράουν, ως ο καλύτερος ειδικός στα φυτά, έλαβε τον τίτλο «Πρίγκιπας των Βοτανολόγων». Έκανε πολλές υπέροχες ανακαλύψεις. Το 1805, μετά από μια τετραετή αποστολή στην Αυστραλία, έφερε στην Αγγλία περίπου 4.000 είδη αυστραλιανών φυτών άγνωστα στους επιστήμονες και πέρασε πολλά χρόνια μελετώντας τα. Περιγράφονται φυτά που φέρθηκαν από την Ινδονησία και Κεντρική Αφρική. Μελέτησε τη φυσιολογία των φυτών, περιέγραψε λεπτομερώς τον πυρήνα για πρώτη φορά φυτικό κύτταρο. Αλλά το όνομα του επιστήμονα είναι πλέον ευρέως γνωστό όχι λόγω αυτών των εργασιών.
Το 1827 ο Μπράουν διεξήγαγε έρευνα για τη γύρη των φυτών. Ενδιαφερόταν ιδιαίτερα για το πώς η γύρη συμμετέχει στη διαδικασία της γονιμοποίησης. Κάποτε, κάτω από ένα μικροσκόπιο, εξέτασε επιμήκεις κυτταροπλασματικούς κόκκους αιωρούμενους στο νερό από κύτταρα γύρης του βορειοαμερικανικού φυτού Clarkia pulchella. Ξαφνικά ο Μπράουν είδε ότι οι μικρότεροι στερεοί κόκκοι, που μετά βίας φαινόταν σε μια σταγόνα νερού, έτρεμαν συνεχώς και κινούνταν από μέρος σε μέρος. Διαπίστωσε ότι αυτές οι κινήσεις, σύμφωνα με τα λόγια του, «δεν συνδέονται ούτε με ροές στο υγρό ούτε με τη σταδιακή εξάτμισή του, αλλά είναι εγγενείς στα ίδια τα σωματίδια».
Η παρατήρηση του Μπράουν επιβεβαιώθηκε από άλλους επιστήμονες. Τα μικρότερα σωματίδια συμπεριφέρονταν σαν να ήταν ζωντανά και ο «χορός» των σωματιδίων επιταχύνθηκε με την αύξηση της θερμοκρασίας και τη μείωση του μεγέθους των σωματιδίων και σαφώς επιβραδύνθηκε όταν αντικαθιστούσε το νερό με ένα πιο παχύρρευστο μέσο. Αυτό το εκπληκτικό φαινόμενο δεν σταμάτησε ποτέ: μπορούσε να παρατηρηθεί για όσο χρονικό διάστημα επιθυμείτε. Στην αρχή, ο Μπράουν πίστευε ακόμη ότι τα ζωντανά όντα έπεσαν στο πεδίο του μικροσκοπίου, ειδικά επειδή η γύρη είναι τα αρσενικά αναπαραγωγικά κύτταρα των φυτών, αλλά υπήρχαν και σωματίδια από νεκρά φυτά, ακόμη και από αυτά που είχαν αποξηρανθεί εκατό χρόνια νωρίτερα σε φυτά. Τότε ο Μπράουν αναρωτήθηκε αν αυτά ήταν τα «στοιχειώδη μόρια των ζωντανών όντων» για τα οποία μίλησε ο διάσημος Γάλλος φυσιοδίφης Ζορζ Μπουφόν (1707-1788), συγγραφέας του 36 τόμου Φυσικής Ιστορίας. Αυτή η υπόθεση χάθηκε όταν ο Μπράουν άρχισε να εξετάζει προφανώς άψυχα αντικείμενα. στην αρχή ήταν πολύ μικρά σωματίδια άνθρακα, καθώς και αιθάλη και σκόνη από τον αέρα του Λονδίνου, και στη συνέχεια αλεσμένα ανόργανες ουσίες: γυαλί, πολλά διαφορετικά ορυκτά. «Ενεργά μόρια» υπήρχαν παντού: «Σε κάθε ορυκτό», έγραψε ο Μπράουν, «το οποίο κατάφερα να το αλέθω σε σκόνη σε τέτοιο βαθμό που θα μπορούσε να αιωρηθεί για κάποιο χρονικό διάστημα στο νερό, βρήκα, σε μεγαλύτερες ή μικρότερες ποσότητες, αυτά τα μόρια».
Για περίπου 30 χρόνια, η ανακάλυψη του Μπράουν δεν τράβηξε το ενδιαφέρον των φυσικών. Το νέο φαινόμενο δεν δόθηκε μεγάλης σημασίας, πιστεύοντας ότι εξηγείται από το τρέμουλο του παρασκευάσματος ή παρόμοια με την κίνηση των σωματιδίων σκόνης, που παρατηρείται στην ατμόσφαιρα όταν πέφτει πάνω τους μια ακτίνα φωτός και που, όπως ήταν γνωστό, προκαλείται από την κίνηση του αέρας. Αλλά αν οι κινήσεις των σωματιδίων Brown προκλήθηκαν από οποιεσδήποτε ροές στο υγρό, τότε τέτοια γειτονικά σωματίδια θα κινούνταν συντονισμένα, κάτι που έρχεται σε αντίθεση με τα δεδομένα παρατήρησης.
Μια εξήγηση της κίνησης Brown (όπως ονομάστηκε αυτό το φαινόμενο) από την κίνηση των αόρατων μορίων δόθηκε μόνο στο τελευταίο τέταρτο του 19ου αιώνα, αλλά δεν έγινε αμέσως αποδεκτή από όλους τους επιστήμονες. Το 1863, ένας δάσκαλος της περιγραφικής γεωμετρίας από την Καρλσρούη (Γερμανία), ο Ludwig Christian Wiener (1826-1896), πρότεινε ότι το φαινόμενο σχετίζεται με ταλαντευτικές κινήσειςαόρατα άτομα. Είναι σημαντικό ότι ο Wiener είδε την ευκαιρία να χρησιμοποιήσει αυτό το φαινόμενο για να διεισδύσει στα μυστικά της δομής της ύλης. Ήταν ο πρώτος που προσπάθησε να μετρήσει την ταχύτητα κίνησης των σωματιδίων Brown και την εξάρτησή της από το μέγεθός τους. Όμως τα συμπεράσματα του Wiener περιπλέκονταν από την εισαγωγή της έννοιας των «ατόμων του αιθέρα» εκτός από τα άτομα της ύλης. Το 1876, ο William Ramsay και το 1877, οι Βέλγοι Ιησουίτες ιερείς Carbonel, Delso και Thirion, και τελικά, το 1888, ο Guy, έδειξαν ξεκάθαρα τη θερμική φύση της κίνησης Brown [5].
«Σε μια μεγάλη περιοχή», έγραψαν οι Delso και Carbonelle, «οι κρούσεις των μορίων, που είναι η αιτία της πίεσης, δεν προκαλούν κανένα τίναγμα του αιωρούμενου σώματος, επειδή μαζί δημιουργούν μια ομοιόμορφη πίεση στο σώμα προς όλες τις κατευθύνσεις. . Εάν όμως η περιοχή δεν επαρκεί για να αντισταθμίσει την ανομοιομορφία, είναι απαραίτητο να ληφθεί υπόψη η ανισότητα των πιέσεων και η συνεχής μεταβολή τους από σημείο σε σημείο. Νόμος μεγάλοι αριθμοίδεν μειώνει τώρα την επίδραση των συγκρούσεων σε μια μέση ομοιόμορφη πίεση, το αποτέλεσμα τους δεν θα είναι πλέον ίσο με το μηδέν, αλλά θα αλλάζει συνεχώς την κατεύθυνση και το μέγεθός τους».
Αν δεχτούμε αυτή την εξήγηση, τότε το φαινόμενο της θερμικής κίνησης των υγρών, που υποτίθεται από την κινητική θεωρία, μπορεί να ειπωθεί ότι αποδεικνύεται ad oculos (οπτικά). Όπως είναι δυνατόν, χωρίς να διακρίνουμε τα κύματα στην απόσταση στη θάλασσα, να εξηγήσουμε το λίκνισμα ενός σκάφους στον ορίζοντα από τα κύματα, με τον ίδιο τρόπο, χωρίς να δούμε την κίνηση των μορίων, μπορεί κανείς να το κρίνει από την κίνηση των αιωρούμενων σωματιδίων. σε υγρό.
Αυτή η εξήγηση της κίνησης Brown είναι σημαντική όχι μόνο ως επιβεβαίωση της κινητικής θεωρίας, αλλά συνεπάγεται επίσης σημαντικές θεωρητικές συνέπειες. Σύμφωνα με το νόμο της διατήρησης της ενέργειας, μια αλλαγή στην ταχύτητα ενός αιωρούμενου σωματιδίου πρέπει να συνοδεύεται από μια αλλαγή της θερμοκρασίας σε άμεση γειτνίαση με αυτό το σωματίδιο: αυτή η θερμοκρασία αυξάνεται εάν η ταχύτητα του σωματιδίου μειωθεί και μειώνεται εάν η ταχύτητα του σωματιδίου αυξάνεται. Έτσι, η θερμική ισορροπία ενός υγρού είναι μια στατιστική ισορροπία.
Μια ακόμη πιο σημαντική παρατήρηση έγινε το 1888 από τον Γκάι: η κίνηση Brown, αυστηρά μιλώντας, δεν υπακούει στον δεύτερο νόμο της θερμοδυναμικής. Στην πραγματικότητα, όταν ένα αιωρούμενο σωματίδιο ανεβαίνει αυθόρμητα σε ένα υγρό, μέρος της θερμότητας του περιβάλλοντός του μετατρέπεται αυθόρμητα σε μηχανική εργασία, το οποίο απαγορεύεται από τον δεύτερο νόμο της θερμοδυναμικής. Οι παρατηρήσεις, ωστόσο, έχουν δείξει ότι η ανύψωση ενός σωματιδίου συμβαίνει λιγότερο συχνά, όσο πιο βαρύ είναι το σωματίδιο. Για σωματίδια ύλης κανονικού μεγέθους, αυτή η πιθανότητα μιας τέτοιας αύξησης είναι πρακτικά μηδενική.
Έτσι, ο δεύτερος νόμος της θερμοδυναμικής γίνεται νόμος των πιθανοτήτων και όχι νόμος της ανάγκης. Καμία προηγούμενη εμπειρία δεν έχει υποστηρίξει αυτή τη στατιστική ερμηνεία. Αρκούσε να αρνηθούμε την ύπαρξη μορίων, όπως έγινε, για παράδειγμα, από τη σχολή της ενέργειας, που άκμασε υπό την ηγεσία του Mach και του Ostwald, για να γίνει ο δεύτερος νόμος της θερμοδυναμικής νόμος της ανάγκης. Αλλά μετά την ανακάλυψη της κίνησης Brown, μια αυστηρή ερμηνεία του δεύτερου νόμου έγινε αδύνατη: υπήρχε πραγματική εμπειρία που έδειξε ότι ο δεύτερος νόμος της θερμοδυναμικής παραβιάζεται συνεχώς στη φύση, ότι μηχανή αέναης κίνησηςΤο δεύτερο είδος όχι μόνο δεν αποκλείεται, αλλά συμβαίνει συνεχώς μπροστά στα μάτια μας.
Ως εκ τούτου, στα τέλη του περασμένου αιώνα, η μελέτη της κίνησης Brown απέκτησε τεράστια θεωρητική σημασία και τράβηξε την προσοχή πολλών θεωρητικών φυσικών, και ιδιαίτερα του Αϊνστάιν.
Τι είναι η κίνηση Brown;
Τώρα θα εξοικειωθείτε με τα πιο προφανή στοιχεία της θερμικής κίνησης των μορίων (η δεύτερη κύρια θέση της μοριακής κινητικής θεωρίας). Φροντίστε να προσπαθήσετε να κοιτάξετε μέσα από ένα μικροσκόπιο και να δείτε πώς κινούνται τα λεγόμενα σωματίδια Brownian.
Προηγουμένως, μάθατε τι είναι διάχυση, δηλαδή ανάμειξη αερίων, υγρών και στερεάκατά την άμεση επαφή τους. Αυτό το φαινόμενο μπορεί να εξηγηθεί από την τυχαία κίνηση των μορίων και τη διείσδυση μορίων μιας ουσίας στο χώρο μεταξύ των μορίων μιας άλλης ουσίας. Αυτό μπορεί να εξηγήσει, για παράδειγμα, το γεγονός ότι ο όγκος ενός μείγματος νερού και αλκοόλης είναι μικρότερος από τον όγκο των συστατικών του. Αλλά η πιο προφανής απόδειξη της κίνησης των μορίων μπορεί να ληφθεί παρατηρώντας μέσω μικροσκοπίου τα μικρότερα σωματίδια οποιασδήποτε ουσίας που αιωρείται στο νερό. στερεός. Αυτά τα σωματίδια υφίστανται τυχαία κίνηση, η οποία ονομάζεται Brownian.
Αυτή είναι η θερμική κίνηση των σωματιδίων που αιωρούνται σε ένα υγρό (ή αέριο).
Παρατήρηση της κίνησης Brown
Ο Άγγλος βοτανολόγος R. Brown (1773-1858) παρατήρησε για πρώτη φορά αυτό το φαινόμενο το 1827, εξετάζοντας τα σπόρια βρύου που αιωρούνται στο νερό μέσω μικροσκοπίου. Αργότερα κοίταξε άλλα μικρά σωματίδια, συμπεριλαμβανομένων κομματιών πέτρας από τις αιγυπτιακές πυραμίδες. Σήμερα, για να παρατηρήσουν την κίνηση Brown, χρησιμοποιούν σωματίδια τσίχλας, η οποία είναι αδιάλυτη στο νερό. Αυτά τα σωματίδια κινούνται τυχαία. Το πιο εκπληκτικό και ασυνήθιστο για εμάς είναι ότι αυτή η κίνηση δεν σταματά ποτέ. Έχουμε συνηθίσει στο γεγονός ότι κάθε κινούμενο σώμα σταματά αργά ή γρήγορα. Ο Μπράουν αρχικά πίστευε ότι τα σπόρια βρύου έδειχναν σημάδια ζωής.
θερμική κίνηση και δεν μπορεί να σταματήσει. Όσο αυξάνεται η θερμοκρασία, αυξάνεται και η έντασή της. Το σχήμα 8.3 δείχνει ένα διάγραμμα της κίνησης των σωματιδίων Brown. Οι θέσεις των σωματιδίων, σημειωμένες με τελείες, προσδιορίζονται σε τακτά χρονικά διαστήματα των 30 δευτερολέπτων. Αυτά τα σημεία συνδέονται με ευθείες γραμμές. Στην πραγματικότητα, η τροχιά των σωματιδίων είναι πολύ πιο περίπλοκη.Brownian κίνησημπορεί επίσης να παρατηρηθεί στο αέριο. Προκαλείται από σωματίδια σκόνης ή καπνού που αιωρούνται στον αέρα.
Ο Γερμανός φυσικός R. Pohl (1884-1976) περιγράφει πολύχρωμα την κίνηση Brown: «Λίγα φαινόμενα είναι ικανά να αιχμαλωτίσουν έναν παρατηρητή όσο η κίνηση Brown. Εδώ ο παρατηρητής επιτρέπεται να κοιτάξει στα παρασκήνια του τι συμβαίνει στη φύση. Ανοίγει μπροστά του νέο κόσμο- ασταμάτητη φασαρία ενός τεράστιου αριθμού σωματιδίων. Τα μικρότερα σωματίδια πετούν γρήγορα μέσα από το οπτικό πεδίο του μικροσκοπίου, αλλάζοντας σχεδόν αμέσως την κατεύθυνση της κίνησης. Τα μεγαλύτερα σωματίδια κινούνται πιο αργά, αλλά επίσης αλλάζουν συνεχώς την κατεύθυνση της κίνησης. Τα μεγάλα σωματίδια πρακτικά συνθλίβονται στη θέση τους. Οι προεξοχές τους δείχνουν ξεκάθαρα την περιστροφή των σωματιδίων γύρω από τον άξονά τους, η οποία αλλάζει συνεχώς κατεύθυνση στο διάστημα. Δεν υπάρχει πουθενά ίχνος συστήματος ή τάξης. Η κυριαρχία της τυφλής ευκαιρίας - αυτή είναι η ισχυρή, συντριπτική εντύπωση που κάνει αυτή η εικόνα στον παρατηρητή».
Επί του παρόντος η έννοια Brownian κίνησηχρησιμοποιείται σε περισσότερα με ευρεία έννοια. Για παράδειγμα, η κίνηση Brown είναι η δόνηση των βελονών των ευαίσθητων οργάνων μέτρησης, η οποία συμβαίνει λόγω της θερμικής κίνησης των ατόμων των μερών του οργάνου και του περιβάλλοντος.
Επεξήγηση της κίνησης Brown
Η κίνηση Brown μπορεί να εξηγηθεί μόνο με βάση τη μοριακή κινητική θεωρία. Ο λόγος για την κίνηση Brown ενός σωματιδίου είναι ότι οι επιπτώσεις των υγρών μορίων στο σωματίδιο δεν αλληλοεξουδετερώνονται. Το σχήμα 8.4 δείχνει σχηματικά τη θέση ενός σωματιδίου Brown και τα μόρια που βρίσκονται πιο κοντά σε αυτό. Όταν τα μόρια κινούνται τυχαία, οι ώσεις που μεταδίδουν στο σωματίδιο Brown, για παράδειγμα, προς τα αριστερά και προς τα δεξιά, δεν είναι ίδιες. Επομένως, η προκύπτουσα δύναμη πίεσης των μορίων υγρού σε ένα σωματίδιο Brown είναι μη μηδενική. Αυτή η δύναμη προκαλεί αλλαγή στην κίνηση του σωματιδίου.

Η μέση πίεση έχει μια ορισμένη τιμή τόσο στο αέριο όσο και στο υγρό. Αλλά υπάρχουν πάντα μικρές τυχαίες αποκλίσεις από αυτόν τον μέσο όρο. Όσο μικρότερη είναι η επιφάνεια του σώματος, τόσο πιο αισθητές είναι οι σχετικές αλλαγές στη δύναμη πίεσης που ασκεί δεδομένης περιοχής. Έτσι, για παράδειγμα, εάν η περιοχή έχει μέγεθος της τάξης πολλών διαμέτρων του μορίου, τότε η δύναμη πίεσης που ασκείται σε αυτήν αλλάζει απότομα από το μηδέν σε μια ορισμένη τιμή όταν το μόριο χτυπά αυτήν την περιοχή.
Η μοριακή κινητική θεωρία της κίνησης Brown δημιουργήθηκε το 1905 από τον A. Einstein (1879-1955).
Η κατασκευή της θεωρίας της κίνησης Brown και η πειραματική επιβεβαίωσή της από τον Γάλλο φυσικό J. Perrin ολοκλήρωσε τελικά τη νίκη της μοριακής κινητικής θεωρίας.
Τα πειράματα του Perrin
Η ιδέα των πειραμάτων του Perrin είναι η εξής. Είναι γνωστό ότι η συγκέντρωση των μορίων αερίου στην ατμόσφαιρα μειώνεται με το υψόμετρο. Αν δεν υπήρχε θερμική κίνηση, τότε όλα τα μόρια θα έπεφταν στη Γη και η ατμόσφαιρα θα εξαφανιζόταν. Ωστόσο, αν δεν υπήρχε έλξη προς τη Γη, τότε λόγω θερμικής κίνησης τα μόρια θα έφευγαν από τη Γη, αφού το αέριο είναι ικανό για απεριόριστη διαστολή. Ως αποτέλεσμα της δράσης αυτών των αντίθετων παραγόντων, δημιουργείται μια ορισμένη κατανομή των μορίων σε ύψος, όπως προαναφέρθηκε, δηλ. η συγκέντρωση των μορίων μειώνεται αρκετά γρήγορα με το ύψος. Επιπλέον, παρά περισσότερη μάζαμόρια, τόσο πιο γρήγορα μειώνεται η συγκέντρωσή τους με το ύψος.
Τα σωματίδια Brown συμμετέχουν στη θερμική κίνηση. Δεδομένου ότι η αλληλεπίδρασή τους είναι αμελητέα μικρή, η συλλογή αυτών των σωματιδίων σε ένα αέριο ή υγρό μπορεί να θεωρηθεί ως ιδανικό αέριο πολύ βαρέων μορίων. Κατά συνέπεια, η συγκέντρωση των σωματιδίων Brownian σε ένα αέριο ή υγρό στο βαρυτικό πεδίο της Γης θα πρέπει να μειωθεί σύμφωνα με τον ίδιο νόμο με τη συγκέντρωση των μορίων αερίου. Αυτός ο νόμος είναι γνωστός.
Ο Perrin, χρησιμοποιώντας ένα μικροσκόπιο υψηλής μεγέθυνσης με μικρό βάθος πεδίου (ρηχό βάθος πεδίου), παρατήρησε σωματίδια Brownian σε πολύ λεπτά στρώματα υγρού. Υπολογίζοντας τη συγκέντρωση των σωματιδίων σε διαφορετικά ύψη, βρήκε ότι αυτή η συγκέντρωση μειώνεται με το ύψος σύμφωνα με τον ίδιο νόμο με τη συγκέντρωση των μορίων αερίου. Η διαφορά είναι ότι λόγω της μεγάλης μάζας των σωματιδίων Brownian, η μείωση συμβαίνει πολύ γρήγορα.
Επιπλέον, η μέτρηση των σωματιδίων Brownian σε διαφορετικά ύψη επέτρεψε στον Perrin να προσδιορίσει τη σταθερά του Avogadro χρησιμοποιώντας μια εντελώς νέα μέθοδο. Η τιμή αυτής της σταθεράς συνέπεσε με τη γνωστή.
Όλα αυτά τα γεγονότα δείχνουν την ορθότητα της θεωρίας της κίνησης Brown και, κατά συνέπεια, ότι τα σωματίδια Brown συμμετέχουν στη θερμική κίνηση των μορίων.
Έχετε δει ξεκάθαρα την ύπαρξη θερμικής κίνησης. είδε μια χαοτική κίνηση να γίνεται. Τα μόρια κινούνται ακόμη πιο τυχαία από τα σωματίδια Brown.
Η ουσία του φαινομένου
Τώρα ας προσπαθήσουμε να κατανοήσουμε την ουσία του φαινομένου της κίνησης Brown. Και συμβαίνει επειδή όλα τα απολύτως υγρά και αέρια αποτελούνται από άτομα ή μόρια. Αλλά γνωρίζουμε επίσης ότι αυτά τα μικροσκοπικά σωματίδια, όντας σε συνεχή χαοτική κίνηση, ωθούν συνεχώς το σωματίδιο Brown από διαφορετικές κατευθύνσεις.
Αλλά αυτό που είναι ενδιαφέρον είναι ότι οι επιστήμονες έχουν αποδείξει ότι τα σωματίδια είναι περισσότερα μεγάλα μεγέθη, που ξεπερνούν τα 5 μικρά παραμένουν ακίνητα και σχεδόν δεν συμμετέχουν στην κίνηση Brown, κάτι που δεν μπορεί να ειπωθεί για μικρότερα σωματίδια. Τα σωματίδια με μέγεθος μικρότερο από 3 μικρά είναι ικανά να κινούνται μεταφραστικά, να εκτελούν περιστροφές ή να γράφουν πολύπλοκες τροχιές.
Όταν ένα μεγάλο σώμα βυθίζεται στο περιβάλλον, οι κραδασμοί που συμβαίνουν σε τεράστιο αριθμό φαίνεται να φτάνουν μέσο επίπεδοκαι διατηρεί σταθερή πίεση. Σε αυτή την περίπτωση, η θεωρία του Αρχιμήδη μπαίνει στο παιχνίδι, καθώς ένα μεγάλο σώμα που περιβάλλεται από το περιβάλλον από όλες τις πλευρές εξισορροπεί την πίεση και η εναπομένουσα δύναμη ανύψωσης επιτρέπει σε αυτό το σώμα να επιπλέει ή να βυθίζεται.
Αν όμως το σώμα έχει διαστάσεις όπως ένα σωματίδιο Brown, δηλαδή εντελώς ανεπαίσθητες, τότε γίνονται αισθητές οι αποκλίσεις της πίεσης, οι οποίες συμβάλλουν στη δημιουργία μιας τυχαίας δύναμης που οδηγεί σε δονήσεις αυτών των σωματιδίων. Μπορεί να συναχθεί το συμπέρασμα ότι τα σωματίδια Brown στο μέσο βρίσκονται σε εναιώρηση, σε αντίθεση με τα μεγάλα σωματίδια που βυθίζονται ή επιπλέουν.
Έννοια της κίνησης Brown
Ας προσπαθήσουμε να καταλάβουμε εάν η κίνηση Brown έχει κάποια σημασία στο φυσικό περιβάλλον:
Πρώτον, η κίνηση Brown διαδραματίζει σημαντικό ρόλο στη διατροφή των φυτών από το έδαφος.
Δεύτερον, στους ανθρώπινους και ζωικούς οργανισμούς, η απορρόφηση των θρεπτικών συστατικών γίνεται μέσω των τοιχωμάτων των πεπτικών οργάνων λόγω της κίνησης Brown.
Τρίτον, στην εφαρμογή της αναπνοής του δέρματος.
Και τέλος, η κίνηση Brown είναι επίσης σημαντική στη διάδοση βλαβερές ουσίεςστον αέρα και στο νερό.
Εργασία για το σπίτι
Διαβάστε προσεκτικά τις ερωτήσεις και δώστε γραπτές απαντήσεις σε αυτές:
1. Θυμάστε τι ονομάζεται διάχυση;
2. Ποια είναι η σχέση μεταξύ της διάχυσης και της θερμικής κίνησης των μορίων;
3. Ορίστε την κίνηση Brown.
4. Πιστεύετε ότι η κίνηση Brown είναι θερμική και δικαιολογείτε την απάντησή σας;
5. Θα αλλάξει η φύση της κίνησης Brown όταν θερμανθεί; Αν αλλάξει, πώς ακριβώς;
6. Ποια συσκευή χρησιμοποιείται για τη μελέτη της κίνησης Brown;
7. Αλλάζει το μοτίβο της κίνησης Brown με την αύξηση της θερμοκρασίας και πώς ακριβώς;
8. Θα υπάρξουν αλλαγές στην κίνηση Brown εάν το γαλάκτωμα νερού αντικατασταθεί με γλυκερίνη;
G.Ya.Myakishev, B.B.Bukhovtsev, N.N.Sotsky, Φυσική 10η τάξη
Η ανακάλυψη του Μπράουν.
Ο Σκωτσέζος βοτανολόγος Ρόμπερτ Μπράουν (μερικές φορές το επώνυμό του μεταγράφεται ως Μπράουν) κατά τη διάρκεια της ζωής του, ως ο καλύτερος ειδικός στα φυτά, έλαβε τον τίτλο «Πρίγκιπας των Βοτανολόγων». Έκανε πολλές υπέροχες ανακαλύψεις. Το 1805, μετά από μια τετραετή αποστολή στην Αυστραλία, έφερε στην Αγγλία περίπου 4.000 είδη αυστραλιανών φυτών άγνωστα στους επιστήμονες και πέρασε πολλά χρόνια μελετώντας τα. Περιγράφονται φυτά που έφεραν από την Ινδονησία και την Κεντρική Αφρική. Σπούδασε φυσιολογία φυτών και για πρώτη φορά περιέγραψε λεπτομερώς τον πυρήνα ενός φυτικού κυττάρου. Η Ακαδημία Επιστημών της Αγίας Πετρούπολης τον έκανε επίτιμο μέλος. Αλλά το όνομα του επιστήμονα είναι πλέον ευρέως γνωστό όχι λόγω αυτών των εργασιών.
Το 1827 ο Μπράουν διεξήγαγε έρευνα για τη γύρη των φυτών. Ενδιαφερόταν ιδιαίτερα για το πώς η γύρη συμμετέχει στη διαδικασία της γονιμοποίησης. Κάποτε, κάτω από ένα μικροσκόπιο, εξέτασε επιμήκεις κυτταροπλασματικούς κόκκους αιωρούμενους στο νερό από κύτταρα γύρης του βορειοαμερικανικού φυτού Clarkia pulchella. Ξαφνικά ο Μπράουν είδε ότι οι μικρότεροι στερεοί κόκκοι, που μετά βίας φαινόταν σε μια σταγόνα νερού, έτρεμαν συνεχώς και κινούνταν από μέρος σε μέρος. Διαπίστωσε ότι αυτές οι κινήσεις, σύμφωνα με τα λόγια του, «δεν συνδέονται ούτε με ροές στο υγρό ούτε με τη σταδιακή εξάτμισή του, αλλά είναι εγγενείς στα ίδια τα σωματίδια».
Η παρατήρηση του Μπράουν επιβεβαιώθηκε από άλλους επιστήμονες. Τα μικρότερα σωματίδια συμπεριφέρονταν σαν να ήταν ζωντανά και ο «χορός» των σωματιδίων επιταχύνθηκε με την αύξηση της θερμοκρασίας και τη μείωση του μεγέθους των σωματιδίων και σαφώς επιβραδύνθηκε όταν αντικαθιστούσε το νερό με ένα πιο παχύρρευστο μέσο. Αυτό το εκπληκτικό φαινόμενο δεν σταμάτησε ποτέ: μπορούσε να παρατηρηθεί για όσο χρονικό διάστημα επιθυμείτε. Στην αρχή, ο Μπράουν πίστευε ακόμη ότι τα ζωντανά όντα έπεσαν στο πεδίο του μικροσκοπίου, ειδικά επειδή η γύρη είναι τα αρσενικά αναπαραγωγικά κύτταρα των φυτών, αλλά υπήρχαν και σωματίδια από νεκρά φυτά, ακόμη και από αυτά που είχαν αποξηρανθεί εκατό χρόνια νωρίτερα σε φυτά. Τότε ο Μπράουν αναρωτήθηκε αν αυτά ήταν τα «στοιχειώδη μόρια των ζωντανών όντων» για τα οποία μίλησε ο διάσημος Γάλλος φυσιοδίφης Ζωρζ Μπουφόν (1707–1788), συγγραφέας του 36 τόμου Φυσικής Ιστορίας. Αυτή η υπόθεση χάθηκε όταν ο Μπράουν άρχισε να εξετάζει προφανώς άψυχα αντικείμενα. Στην αρχή ήταν πολύ μικρά σωματίδια άνθρακα, καθώς και αιθάλη και σκόνη από τον αέρα του Λονδίνου, στη συνέχεια λεπτοαλεσμένες ανόργανες ουσίες: γυαλί, πολλά διαφορετικά ορυκτά. «Ενεργά μόρια» υπήρχαν παντού: «Σε κάθε ορυκτό», έγραψε ο Μπράουν, «το οποίο κατάφερα να κονιοποιήσω σε τέτοιο βαθμό ώστε να μπορεί να αιωρηθεί στο νερό για κάποιο χρονικό διάστημα, βρήκα, σε μεγαλύτερες ή μικρότερες ποσότητες, αυτά τα μόρια ."
Πρέπει να πούμε ότι ο Μπράουν δεν διέθετε κανένα από τα πιο πρόσφατα μικροσκόπια. Στο άρθρο του τονίζει συγκεκριμένα ότι είχε συνηθισμένους αμφίκυρτους φακούς, τους οποίους χρησιμοποιούσε για αρκετά χρόνια. Και συνεχίζει λέγοντας: «Σε όλη τη διάρκεια της μελέτης συνέχισα να χρησιμοποιώ τους ίδιους φακούς με τους οποίους ξεκίνησα τη δουλειά, προκειμένου να δώσω μεγαλύτερη αξιοπιστία στις δηλώσεις μου και να τις κάνω όσο το δυνατόν πιο προσιτές στις συνηθισμένες παρατηρήσεις».
Τώρα, για να επαναλάβουμε την παρατήρηση του Μπράουν, αρκεί να έχουμε ένα όχι πολύ δυνατό μικροσκόπιο και να το χρησιμοποιήσουμε για να εξετάσουμε τον καπνό σε ένα μαυρισμένο κουτί, που φωτίζεται μέσα από μια πλευρική οπή με μια δέσμη έντονου φωτός. Σε ένα αέριο, το φαινόμενο εκδηλώνεται πολύ πιο καθαρά από ό,τι σε ένα υγρό: μικρά κομμάτια στάχτης ή αιθάλης (ανάλογα με την πηγή του καπνού) είναι ορατά, διασκορπίζουν το φως και πηδούν συνεχώς μπρος-πίσω.
Όπως συμβαίνει συχνά στην επιστήμη, πολλά χρόνια αργότερα οι ιστορικοί ανακάλυψαν ότι το 1670, ο εφευρέτης του μικροσκοπίου, ο Ολλανδός Antonie Leeuwenhoek, παρατήρησε προφανώς ένα παρόμοιο φαινόμενο, αλλά τη σπανιότητα και την ατέλεια των μικροσκοπίων, την εμβρυϊκή κατάσταση της μοριακής επιστήμης εκείνη την εποχή δεν τράβηξε την προσοχή στην παρατήρηση του Leeuwenhoek, επομένως η ανακάλυψη αποδίδεται δικαίως στον Brown, ο οποίος ήταν ο πρώτος που τη μελέτησε και την περιέγραψε λεπτομερώς.
Κίνηση Brown και ατομική-μοριακή θεωρία.
Το φαινόμενο που παρατήρησε ο Μπράουν έγινε γρήγορα ευρέως γνωστό. Ο ίδιος έδειξε τα πειράματά του σε πολλούς συναδέλφους (ο Μπράουν απαριθμεί δύο δωδεκάδες ονόματα). Εξήγησέ το όμως μυστηριώδες φαινόμενο, το οποίο ονομάστηκε «Κίνημα Μπράουν», δεν ήταν δυνατό ούτε από τον ίδιο τον Μπράουν ούτε από πολλούς άλλους επιστήμονες για πολλά χρόνια. Οι κινήσεις των σωματιδίων ήταν εντελώς τυχαίες: σκίτσα των θέσεων τους έγιναν μέσα διαφορετικές στιγμέςο χρόνος (για παράδειγμα, κάθε λεπτό) δεν έδινε με την πρώτη ματιά καμία δυνατότητα εύρεσης κάποιου σχεδίου σε αυτές τις κινήσεις.
Μια εξήγηση της κίνησης Brown (όπως ονομάστηκε αυτό το φαινόμενο) από την κίνηση των αόρατων μορίων δόθηκε μόνο στο τελευταίο τέταρτο του 19ου αιώνα, αλλά δεν έγινε αμέσως αποδεκτή από όλους τους επιστήμονες. Το 1863, ένας δάσκαλος της περιγραφικής γεωμετρίας από την Καρλσρούη (Γερμανία), ο Ludwig Christian Wiener (1826–1896), πρότεινε ότι το φαινόμενο συνδέθηκε με τις ταλαντωτικές κινήσεις αόρατων ατόμων. Αυτή ήταν η πρώτη, αν και πολύ μακριά από τη σύγχρονη, εξήγηση της κίνησης Brown από τις ιδιότητες των ίδιων των ατόμων και των μορίων. Είναι σημαντικό ότι ο Wiener είδε την ευκαιρία να χρησιμοποιήσει αυτό το φαινόμενο για να διεισδύσει στα μυστικά της δομής της ύλης. Ήταν ο πρώτος που προσπάθησε να μετρήσει την ταχύτητα κίνησης των σωματιδίων Brown και την εξάρτησή της από το μέγεθός τους. Είναι αξιοπερίεργο το γεγονός ότι το 1921, στα Πρακτικά της Εθνικής Ακαδημίας Επιστημών των ΗΠΑ, δημοσιεύτηκε μια εργασία για την κίνηση Brown ενός άλλου Wiener, του Norbert, του διάσημου ιδρυτή της κυβερνητικής.
Οι ιδέες του L.K. Wiener έγιναν αποδεκτές και αναπτύχθηκαν από πολλούς επιστήμονες - Sigmund Exner στην Αυστρία (και 33 χρόνια αργότερα - ο γιος του Felix), Giovanni Cantoni στην Ιταλία, Karl Wilhelm Negeli στη Γερμανία, Louis Georges Gouy στη Γαλλία, τρεις Βέλγοι ιερείς - Ιησουίτες Carbonelli, Delso και Tirion και άλλοι. Μεταξύ αυτών των επιστημόνων ήταν και ο μετέπειτα διάσημος Άγγλος φυσικός και χημικός William Ramsay. Σταδιακά έγινε σαφές ότι οι μικρότεροι κόκκοι ύλης χτυπιούνταν από όλες τις πλευρές από ακόμη μικρότερα σωματίδια, τα οποία δεν ήταν πλέον ορατά με μικροσκόπιο - όπως τα κύματα που λικνίζουν ένα μακρινό σκάφος δεν είναι ορατά από την ακτή, ενώ οι κινήσεις του σκάφους είναι ορατά αρκετά καθαρά. Όπως έγραψαν σε ένα από τα άρθρα το 1877, «...ο νόμος των μεγάλων αριθμών δεν μειώνει πλέον την επίδραση των συγκρούσεων στη μέση ομοιόμορφη πίεση· το αποτέλεσμά τους δεν θα είναι πλέον ίσο με μηδέν, αλλά θα αλλάζει συνεχώς την κατεύθυνση και μέγεθος."
Ποιοτικά, η εικόνα ήταν αρκετά εύλογη και ακόμη και οπτική. Περίπου με τον ίδιο τρόπο που ένα μικρό κλαδάκι ή ζωύφιο πρέπει να κινείται όταν σπρώχνεται (ή τραβιέται) μέσα διαφορετικές πλευρέςπολλά μυρμήγκια. Αυτά τα μικρότερα σωματίδια ήταν στην πραγματικότητα στο λεξιλόγιο των επιστημόνων, αλλά κανείς δεν τα είχε δει ποτέ. Ονομάζονταν μόρια. Μετάφραση από τα λατινικά, αυτή η λέξη σημαίνει «μικρή μάζα». Παραδόξως, αυτή ακριβώς είναι η εξήγηση που δίνει σε ένα παρόμοιο φαινόμενο ο Ρωμαίος φιλόσοφος Τίτος Λουκρήτιος Κάρος (περίπου 99–55 π.Χ.) στο περίφημο ποίημά του Περί της φύσης των πραγμάτων. Σε αυτό, αποκαλεί τα μικρότερα σωματίδια αόρατα στο μάτι «πρωταρχικές αρχές» των πραγμάτων.
Οι αρχές των πραγμάτων κινούνται πρώτα μόνες τους,
Ακολουθούν σώματα από τον μικρότερο συνδυασμό τους,
Κοντά, σαν να λέγαμε, σε ισχύ στις πρωταρχικές αρχές,
Κρυμμένοι από αυτούς, δεχόμενοι σοκ, αρχίζουν να αγωνίζονται,
Οι ίδιοι να κινούνται, ενθαρρύνοντας στη συνέχεια μεγαλύτερα σώματα.
Ξεκινώντας λοιπόν από την αρχή η κίνηση σιγά σιγά
Αγγίζει τα συναισθήματά μας και γίνεται επίσης ορατό
Σε εμάς και στους κόκκους της σκόνης που κινούνται στο φως του ήλιου,
Αν και οι δονήσεις από τις οποίες εμφανίζεται είναι ανεπαίσθητες...
Στη συνέχεια, αποδείχθηκε ότι ο Λουκρήτιος έκανε λάθος: είναι αδύνατο να παρατηρήσουμε την κίνηση Brown με γυμνό μάτι και τα σωματίδια σκόνης σε μια ηλιακή ακτίνα που διείσδυσε σε σκοτεινό δωμάτιο, «χορός» λόγω των στροβιλιστικών κινήσεων του αέρα. Αλλά εξωτερικά και τα δύο φαινόμενα έχουν κάποιες ομοιότητες. Και μόνο τον 19ο αιώνα. Έγινε προφανές σε πολλούς επιστήμονες ότι η κίνηση των σωματιδίων Brown προκαλείται από τυχαίες κρούσεις των μορίων του μέσου. Τα κινούμενα μόρια συγκρούονται με σωματίδια σκόνης και άλλα στερεά σωματίδια που βρίσκονται στο νερό. Όσο υψηλότερη είναι η θερμοκρασία, τόσο πιο γρήγορη είναι η κίνηση. Εάν ένα κομμάτι σκόνης είναι μεγάλο, για παράδειγμα, έχει μέγεθος 0,1 mm (η διάμετρος είναι ένα εκατομμύριο φορές μεγαλύτερη από αυτή ενός μορίου νερού), τότε πολλές ταυτόχρονες κρούσεις σε αυτό από όλες τις πλευρές είναι αμοιβαία ισορροπημένες και πρακτικά δεν το κάνει. «Νιώσε» τα - περίπου το ίδιο με ένα κομμάτι ξύλου στο μέγεθος ενός πιάτου δεν θα «νιώσει» τις προσπάθειες πολλών μυρμηγκιών που θα το τραβήξουν ή θα το σπρώξουν σε διαφορετικές κατευθύνσεις. Εάν το σωματίδιο της σκόνης είναι σχετικά μικρό, θα κινηθεί προς τη μία ή την άλλη κατεύθυνση υπό την επίδραση κρούσεων από τα γύρω μόρια.
Τα σωματίδια Brownian έχουν μέγεθος της τάξης των 0,1–1 μm, δηλ. από το ένα χιλιοστό έως το ένα δέκατο χιλιοστό του χιλιοστού, γι' αυτό ο Μπράουν μπόρεσε να διακρίνει την κίνησή τους επειδή κοίταζε μικροσκοπικούς κυτταροπλασματικούς κόκκους και όχι την ίδια τη γύρη (για την οποία συχνά γράφεται λανθασμένα). Το πρόβλημα είναι ότι τα κύτταρα γύρης είναι πολύ μεγάλα. Έτσι, στη γύρη του λιβαδιού, που μεταφέρεται από τον άνεμο και προκαλεί αλλεργικές ασθένειες στον άνθρωπο (πυρετός εκ χόρτου), το μέγεθος των κυττάρων είναι συνήθως της τάξης των 20 - 50 microns, δηλ. είναι πολύ μεγάλα για να παρατηρήσουν την κίνηση Brown. Είναι επίσης σημαντικό να σημειωθεί ότι μεμονωμένες κινήσεις ενός σωματιδίου Brown συμβαίνουν πολύ συχνά και σε πολύ μικρές αποστάσεις, έτσι ώστε να είναι αδύνατο να τις δούμε, αλλά κάτω από ένα μικροσκόπιο, κινήσεις που έχουν συμβεί σε μια συγκεκριμένη χρονική περίοδο είναι ορατές.
Φαίνεται ότι το ίδιο το γεγονός της ύπαρξης της κίνησης Brown αποδεικνύεται ξεκάθαρα μοριακή δομήσημασία, ωστόσο, ακόμη και στις αρχές του 20ού αιώνα. Υπήρχαν επιστήμονες, συμπεριλαμβανομένων φυσικών και χημικών, που δεν πίστευαν στην ύπαρξη μορίων. Η ατομική-μοριακή θεωρία μόνο αργά και με δυσκολία κέρδισε την αναγνώριση. Έτσι, ο κορυφαίος Γάλλος οργανικός χημικός Marcelin Berthelot (1827–1907) έγραψε: «Η έννοια ενός μορίου, από τη σκοπιά της γνώσης μας, είναι αβέβαιη, ενώ μια άλλη έννοια - ένα άτομο - είναι καθαρά υποθετική». Ο διάσημος Γάλλος χημικός A. Saint-Clair Deville (1818–1881) μίλησε ακόμη πιο ξεκάθαρα: «Δεν αποδέχομαι το νόμο του Avogadro, ούτε το άτομο, ούτε το μόριο, γιατί αρνούμαι να πιστέψω σε αυτό που ούτε μπορώ να δω ούτε να παρατηρήσω. ” Και ο Γερμανός φυσικοχημικός Wilhelm Ostwald (1853–1932), βραβευμένος βραβείο Νόμπελ, ένας από τους ιδρυτές φυσική χημεία, στις αρχές του 20ου αιώνα. αρνήθηκε κατηγορηματικά την ύπαρξη ατόμων. Κατάφερε να γράψει ένα τρίτομο εγχειρίδιο χημείας στο οποίο η λέξη «άτομο» δεν αναφέρεται ποτέ καν. Μιλώντας στις 19 Απριλίου 1904 με μια μεγάλη έκθεση στο Βασιλικό Ίδρυμα σε μέλη των Άγγλων Χημική Εταιρεία, ο Ostwald προσπάθησε να αποδείξει ότι τα άτομα δεν υπάρχουν και «αυτό που ονομάζουμε ύλη είναι μόνο μια συλλογή ενεργειών που συλλέγονται μαζί σε ένα δεδομένο μέρος».
Αλλά ακόμη και εκείνοι οι φυσικοί που αποδέχονταν τη μοριακή θεωρία δεν μπορούσαν να πιστέψουν ότι κάτι τέτοιο με απλό τρόποΗ εγκυρότητα της ατομικής-μοριακής θεωρίας αποδείχθηκε και έτσι προβλήθηκαν ποικίλοι εναλλακτικοί λόγοι για να εξηγηθεί το φαινόμενο. Και αυτό είναι απολύτως σύμφωνα με το πνεύμα της επιστήμης: μέχρι να εντοπιστεί με σαφήνεια η αιτία ενός φαινομένου, είναι δυνατό (και ακόμη και απαραίτητο) να υποθέσουμε διάφορες υποθέσεις, οι οποίες θα πρέπει, αν είναι δυνατόν, να ελεγχθούν πειραματικά ή θεωρητικά. Έτσι, πίσω στο 1905 Εγκυκλοπαιδικό ΛεξικόΟι Brockhaus and Efron δημοσίευσαν ένα σύντομο άρθρο από τον καθηγητή φυσικής της Αγίας Πετρούπολης N.A. Gezehus, δάσκαλο του διάσημου ακαδημαϊκού A.F. Ioffe. Ο Gesehus έγραψε ότι, σύμφωνα με ορισμένους επιστήμονες, η κίνηση Brown προκαλείται από «ακτίνες φωτός ή θερμότητας που περνούν μέσα από ένα υγρό» και καταλήγει σε «απλές ροές μέσα σε ένα υγρό που δεν έχουν καμία σχέση με τις κινήσεις των μορίων» και αυτές οι ροές μπορεί να προκληθεί από «εξάτμιση, διάχυση και άλλους λόγους». Άλλωστε, ήταν ήδη γνωστό ότι μια πολύ παρόμοια κίνηση σωματιδίων σκόνης στον αέρα προκαλείται ακριβώς από ροές δίνης. Αλλά η εξήγηση που έδωσε ο Gesehus θα μπορούσε εύκολα να διαψευσθεί πειραματικά: αν κοιτάξετε δύο σωματίδια Brownian που βρίσκονται πολύ κοντά το ένα στο άλλο μέσω ενός ισχυρού μικροσκοπίου, οι κινήσεις τους θα αποδειχθούν εντελώς ανεξάρτητες. Εάν αυτές οι κινήσεις προκλήθηκαν από οποιεσδήποτε ροές στο υγρό, τότε τέτοια γειτονικά σωματίδια θα κινούνταν συντονισμένα.
Θεωρία της κίνησης Brown.
Στις αρχές του 20ου αιώνα. Οι περισσότεροι επιστήμονες κατανόησαν τη μοριακή φύση της κίνησης Brown. Αλλά όλες οι εξηγήσεις παρέμειναν καθαρά ποιοτικές· καμία ποσοτική θεωρία δεν μπορούσε να σταθεί πειραματική επαλήθευση. Επιπλέον, εσύ ο ίδιος πειραματικά αποτελέσματαήταν ασαφή: το φανταστικό θέαμα των ασταμάτητα ορμητικών σωματιδίων υπνώτισε τους πειραματιστές και δεν γνώριζαν ακριβώς ποια χαρακτηριστικά του φαινομένου έπρεπε να μετρηθούν.
Παρά τη φαινομενική πλήρη διαταραχή, ήταν ακόμα δυνατό να περιγραφούν οι τυχαίες κινήσεις των σωματιδίων Brown με μια μαθηματική σχέση. Για πρώτη φορά, μια αυστηρή εξήγηση της κίνησης Brown δόθηκε το 1904 από τον Πολωνό φυσικό Marian Smoluchowski (1872–1917), ο οποίος εκείνα τα χρόνια εργαζόταν στο Πανεπιστήμιο του Lviv. Ταυτόχρονα, η θεωρία αυτού του φαινομένου αναπτύχθηκε από τον Albert Einstein (1879–1955), έναν ελάχιστα γνωστό τότε εμπειρογνώμονα 2ης κατηγορίας στο Γραφείο Διπλωμάτων Ευρεσιτεχνίας της ελβετικής πόλης της Βέρνης. Το άρθρο του, που δημοσιεύτηκε τον Μάιο του 1905 στο γερμανικό περιοδικό Annalen der Physik, είχε τον τίτλο «Στην κίνηση των σωματιδίων που αιωρούνται σε ένα ρευστό σε ηρεμία, που απαιτείται από τη μοριακή κινητική θεωρία της θερμότητας». Με αυτό το όνομα, ο Αϊνστάιν ήθελε να δείξει ότι η μοριακή κινητική θεωρία της δομής της ύλης υπονοεί απαραίτητα την ύπαρξη τυχαίας κίνησης των μικρότερων στερεών σωματιδίων στα υγρά.
Είναι περίεργο ότι στην αρχή αυτού του άρθρου, ο Αϊνστάιν γράφει ότι είναι εξοικειωμένος με το ίδιο το φαινόμενο, αν και επιφανειακά: «Είναι πιθανό οι εν λόγω κινήσεις να είναι ταυτόσημες με τη λεγόμενη μοριακή κίνηση Brown, αλλά τα διαθέσιμα δεδομένα Για μένα σχετικά με τα τελευταία είναι τόσο ανακριβή που δεν μπορούσα να διατυπώσω μια συγκεκριμένη άποψη». Και δεκαετίες αργότερα, ήδη στα τέλη της ζωής του, ο Αϊνστάιν έγραψε κάτι διαφορετικό στα απομνημονεύματά του - ότι δεν ήξερε καθόλου για την κίνηση Brown και στην πραγματικότητα την «ανακάλυψε ξανά» καθαρά θεωρητικά: «Μη γνωρίζοντας ότι οι παρατηρήσεις της «κίνησης Brown» ήταν από καιρό γνωστό, ανακάλυψα ότι η ατομική θεωρία οδηγεί στην ύπαρξη παρατηρήσιμης κίνησης μικροσκοπικών αιωρούμενων σωματιδίων." Όπως και να έχει, το θεωρητικό άρθρο του Αϊνστάιν τελείωσε με μια άμεση κλήση στους πειραματιστές να δοκιμάσουν τα συμπεράσματά του πειραματικά: "Αν κάποιος ερευνητής μπορούσε σύντομα να απαντήσει τα ερωτήματα που τίθενται εδώ ρωτούν!" – τελειώνει το άρθρο του με ένα τόσο ασυνήθιστο επιφώνημα.
Η απάντηση στην παθιασμένη έκκληση του Αϊνστάιν δεν άργησε να έρθει.
Σύμφωνα με τη θεωρία Smoluchowski-Einstein, η μέση τιμή της τετραγωνικής μετατόπισης ενός σωματιδίου Brown (s2) κατά τη διάρκεια του χρόνου t είναι ευθέως ανάλογη με τη θερμοκρασία T και αντιστρόφως ανάλογη με το ιξώδες του υγρού h, το μέγεθος σωματιδίου r και τη σταθερά του Avogadro
NA: s2 = 2RTt/6phrNA,
Όπου R είναι η σταθερά του αερίου. Έτσι, εάν σε 1 λεπτό ένα σωματίδιο με διάμετρο 1 μm κινείται κατά 10 μm, τότε σε 9 λεπτά - κατά 10 = 30 μm, σε 25 λεπτά - κατά 10 = 50 μm, κ.λπ. Κάτω από παρόμοιες συνθήκες, ένα σωματίδιο με διάμετρο 0,25 μm για τις ίδιες χρονικές περιόδους (1, 9 και 25 λεπτά) θα κινηθεί κατά 20, 60 και 100 μm, αντίστοιχα, αφού = 2. Είναι σημαντικό ο παραπάνω τύπος να περιλαμβάνει Η σταθερά του Avogadro, η οποία επομένως, μπορεί να προσδιοριστεί με ποσοτικές μετρήσεις της κίνησης ενός σωματιδίου Brown, που έγινε από τον Γάλλο φυσικό Jean Baptiste Perrin (1870–1942).
Το 1908, ο Perrin άρχισε ποσοτικές παρατηρήσεις της κίνησης των σωματιδίων Brown στο μικροσκόπιο. Χρησιμοποίησε ένα υπερμικροσκόπιο, που εφευρέθηκε το 1902, το οποίο επέτρεψε την ανίχνευση των μικρότερων σωματιδίων διαχέοντας φως πάνω τους από έναν ισχυρό πλευρικό φωτιστή. Ο Perrin έλαβε μικροσκοπικές μπάλες σχεδόν σφαιρικού σχήματος και περίπου ίδιου μεγέθους από κόμμι, τον συμπυκνωμένο χυμό ορισμένων τροπικών δέντρων (χρησιμοποιείται επίσης ως κίτρινη ακουαρέλα). Αυτά τα μικροσκοπικά σφαιρίδια εναιωρήθηκαν σε γλυκερίνη που περιείχε 12% νερό. το παχύρρευστο υγρό εμπόδιζε την εμφάνιση εσωτερικών ροών σε αυτό που θα θόλωναν την εικόνα. Οπλισμένος με ένα χρονόμετρο, ο Perrin σημείωσε και στη συνέχεια σκιαγράφησε (φυσικά, σε πολύ μεγεθυμένη κλίμακα) σε ένα γραφικό φύλλο χαρτιού τη θέση των σωματιδίων σε τακτά χρονικά διαστήματα, για παράδειγμα, κάθε μισό λεπτό. Συνδέοντας τα σημεία που προέκυψαν με ευθείες γραμμές, απέκτησε περίπλοκες τροχιές, μερικές από τις οποίες φαίνονται στο σχήμα (προέρχονται από το βιβλίο του Perrin Atomy, που δημοσιεύτηκε το 1920 στο Παρίσι). Μια τέτοια χαοτική, άτακτη κίνηση των σωματιδίων οδηγεί στο γεγονός ότι κινούνται στο χώρο αρκετά αργά: το άθροισμα των τμημάτων είναι πολύ μεγαλύτερο από τη μετατόπιση του σωματιδίου από το πρώτο σημείο στο τελευταίο. 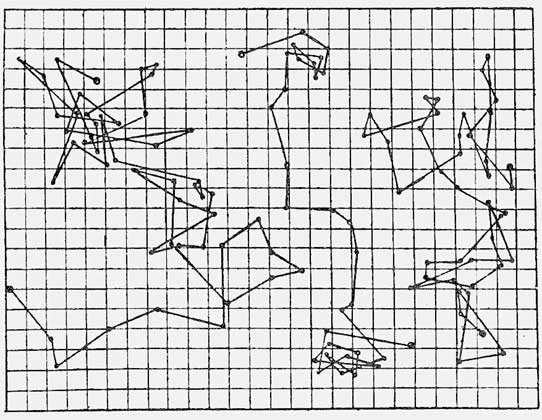
Διαδοχικές θέσεις κάθε 30 δευτερόλεπτα τριών σωματιδίων Brownian - μπάλες τσίχλας με μέγεθος περίπου 1 micron. Ένα κελί αντιστοιχεί σε απόσταση 3 μm.
Διαδοχικές θέσεις κάθε 30 δευτερόλεπτα τριών σωματιδίων Brownian - μπάλες τσίχλας με μέγεθος περίπου 1 micron. Ένα κελί αντιστοιχεί σε απόσταση 3 μm. Εάν ο Perrin μπορούσε να καθορίσει τη θέση των σωματιδίων Brownian όχι μετά από 30, αλλά μετά από 3 δευτερόλεπτα, τότε οι ευθείες γραμμές μεταξύ κάθε γειτονικού σημείου θα μετατρέπονταν στην ίδια πολύπλοκη διακεκομμένη γραμμή ζιγκ-ζαγκ, μόνο σε μικρότερη κλίμακα.
Χρησιμοποιώντας τον θεωρητικό τύπο και τα αποτελέσματά του, ο Perrin έλαβε μια αρκετά ακριβή τιμή για τον αριθμό του Avogadro για εκείνη την εποχή: 6.8.1023. Ο Perrin χρησιμοποίησε επίσης ένα μικροσκόπιο για να μελετήσει την κατακόρυφη κατανομή των σωματιδίων Brown (βλ. ΝΟΜΟ ΤΟΥ AVOGADRO) και έδειξε ότι, παρά τη δράση της βαρύτητας, παραμένουν αιωρούμενα σε διάλυμα. Ο Perrin έχει και άλλους σημαντικό έργο. Το 1895 απέδειξε ότι οι καθοδικές ακτίνες είναι αρνητικές ηλεκτρικά φορτία(ηλεκτρόνια), το 1901 πρότεινε για πρώτη φορά ένα πλανητικό μοντέλο του ατόμου. Το 1926 τιμήθηκε με το Νόμπελ Φυσικής.
Τα αποτελέσματα που έλαβε ο Perrin επιβεβαίωσαν τα θεωρητικά συμπεράσματα του Αϊνστάιν. Έκανε έντονη εντύπωση. Όπως έγραψε ο Αμερικανός φυσικός A. Pais πολλά χρόνια αργότερα, «δεν παύεις ποτέ να εκπλήσσεσαι με αυτό το αποτέλεσμα, που προκύπτει με έναν τόσο απλό τρόπο: αρκεί να ετοιμάσεις ένα εναιώρημα από μπάλες, το μέγεθος των οποίων είναι μεγάλο σε σύγκριση με το μέγεθος. από απλά μόρια, πάρτε ένα χρονόμετρο και ένα μικροσκόπιο και μπορείτε να προσδιορίσετε τη σταθερά του Avogadro!». Θα μπορούσε επίσης να εκπλαγεί κανείς: περιγραφές νέων πειραμάτων για την κίνηση Brown εξακολουθούν να εμφανίζονται σε επιστημονικά περιοδικά (Nature, Science, Journal of Chemical Education) κατά καιρούς! Μετά τη δημοσίευση των αποτελεσμάτων του Perrin, ο Ostwald, πρώην αντίπαλος του ατομισμού, παραδέχτηκε ότι «η σύμπτωση της κίνησης Brown με τις απαιτήσεις της κινητικής υπόθεσης... δίνει τώρα στον πιο προσεκτικό επιστήμονα το δικαίωμα να μιλήσει για πειραματική απόδειξη της ατομικής θεωρίας της ύλης. Έτσι, η ατομική θεωρία έχει ανυψωθεί στην τάξη μιας επιστημονικής, καλά θεμελιωμένης θεωρίας». Τον απηχεί ο Γάλλος μαθηματικός και φυσικός Ανρί Πουανκαρέ: «Ο λαμπρός προσδιορισμός του αριθμού των ατόμων από τον Περέν ολοκλήρωσε τον θρίαμβο του ατομισμού... Το άτομο των χημικών έχει πλέον γίνει πραγματικότητα».
Brownian κίνηση και διάχυση.
Η κίνηση των σωματιδίων Brown μοιάζει πολύ στην εμφάνιση με την κίνηση μεμονωμένων μορίων ως αποτέλεσμα της θερμικής τους κίνησης. Αυτή η κίνηση ονομάζεται διάχυση. Ακόμη και πριν από το έργο του Smoluchowski και του Einstein, οι νόμοι της μοριακής κίνησης καθιερώθηκαν στην απλούστερη περίπτωση της αέριας κατάστασης της ύλης. Αποδείχθηκε ότι τα μόρια στα αέρια κινούνται πολύ γρήγορα - με την ταχύτητα μιας σφαίρας, αλλά δεν μπορούν να πετάξουν μακριά, καθώς πολύ συχνά συγκρούονται με άλλα μόρια. Για παράδειγμα, τα μόρια οξυγόνου και αζώτου στον αέρα, που κινούνται με μέση ταχύτητα περίπου 500 m/s, αντιμετωπίζουν περισσότερες από ένα δισεκατομμύριο συγκρούσεις κάθε δευτερόλεπτο. Επομένως, η διαδρομή του μορίου, αν μπορούσε να ακολουθηθεί, θα ήταν μια πολύπλοκη διακεκομμένη γραμμή. Τα σωματίδια Brown περιγράφουν επίσης μια παρόμοια τροχιά εάν η θέση τους καταγράφεται σε συγκεκριμένα χρονικά διαστήματα. Τόσο η διάχυση όσο και η κίνηση Brown είναι συνέπεια της χαοτικής θερμικής κίνησης των μορίων και επομένως περιγράφονται από παρόμοια μαθηματικές εξαρτήσεις. Η διαφορά είναι ότι τα μόρια στα αέρια κινούνται σε ευθεία γραμμή μέχρι να συγκρουστούν με άλλα μόρια, μετά από την οποία αλλάζουν κατεύθυνση. Ένα σωματίδιο Brown, σε αντίθεση με ένα μόριο, δεν εκτελεί «ελεύθερες πτήσεις», αλλά βιώνει πολύ συχνά μικρές και ακανόνιστες «τρεμούλες», με αποτέλεσμα να μετατοπίζεται χαοτικά προς τη μία ή την άλλη κατεύθυνση. Οι υπολογισμοί έχουν δείξει ότι για ένα σωματίδιο μεγέθους 0,1 μm, μια κίνηση συμβαίνει σε τρία δισεκατομμυριοστά του δευτερολέπτου σε απόσταση μόνο 0,5 nm (1 nm = 0,001 μm). Όπως εύστοχα το θέτει ένας συγγραφέας, αυτό θυμίζει τη μετακίνηση ενός άδειου κουτιού μπύρας σε μια πλατεία όπου έχει συγκεντρωθεί πλήθος κόσμου.
Η διάχυση είναι πολύ πιο εύκολο να παρατηρηθεί από την κίνηση Brown, καθώς δεν απαιτεί μικροσκόπιο: οι κινήσεις δεν παρατηρούνται μεμονωμένων σωματιδίων, αλλά των τεράστιων μαζών τους, απλά πρέπει να διασφαλίσετε ότι η διάχυση δεν υπερτίθεται από τη μεταφορά - ανάμειξη της ύλης ως αποτέλεσμα των ροών στροβιλισμού (τέτοιες ροές είναι εύκολο να παρατηρηθούν, τοποθετώντας μια σταγόνα έγχρωμου διαλύματος, όπως μελάνι, σε ένα ποτήρι ζεστό νερό).
Η διάχυση είναι βολικό να παρατηρείται σε παχιά πηκτώματα. Ένα τέτοιο τζελ μπορεί να παρασκευαστεί, για παράδειγμα, σε ένα βάζο πενικιλίνης παρασκευάζοντας ένα διάλυμα ζελατίνης 4-5% σε αυτό. Η ζελατίνη πρέπει πρώτα να φουσκώσει για αρκετές ώρες και στη συνέχεια διαλύεται πλήρως με ανάδευση κατεβάζοντας το βάζο σε ζεστό νερό. Μετά την ψύξη, λαμβάνεται ένα μη ρέον πήκτωμα με τη μορφή μιας διαφανούς, ελαφρώς θολής μάζας. Εάν, χρησιμοποιώντας αιχμηρά τσιμπιδάκια, εισάγετε προσεκτικά έναν μικρό κρύσταλλο υπερμαγγανικού καλίου («υπερμαγγανικό κάλιο») στο κέντρο αυτής της μάζας, ο κρύσταλλος θα παραμείνει κρεμασμένος στο σημείο που έμεινε, καθώς το τζελ εμποδίζει την πτώση του. Μέσα σε λίγα λεπτά, μια βιολετί σφαίρα θα αρχίσει να μεγαλώνει γύρω από τον κρύσταλλο· με την πάροδο του χρόνου, γίνεται όλο και μεγαλύτερη έως ότου τα τοιχώματα του βάζου παραμορφώσουν το σχήμα του. Το ίδιο αποτέλεσμα μπορεί να επιτευχθεί χρησιμοποιώντας έναν κρύσταλλο θειικού χαλκού, μόνο σε αυτή την περίπτωση η μπάλα δεν θα αποδειχθεί μοβ, αλλά μπλε.
Είναι σαφές γιατί η μπάλα βγήκε: τα ιόντα MnO4– που σχηματίζονται κατά τη διάλυση του κρυστάλλου μεταφέρονται σε διάλυμα (η γέλη είναι κυρίως νερό) και, ως αποτέλεσμα της διάχυσης, κινούνται ομοιόμορφα προς όλες τις κατευθύνσεις, ενώ η βαρύτητα δεν έχει πρακτικά καμία επίδραση στον ρυθμό διάχυσης. Η διάχυση στο υγρό είναι πολύ αργή: θα χρειαστούν πολλές ώρες για να μεγαλώσει η μπάλα αρκετά εκατοστά. Στα αέρια, η διάχυση είναι πολύ πιο γρήγορη, αλλά παρόλα αυτά, αν ο αέρας δεν αναμειγνυόταν, η μυρωδιά του αρώματος ή της αμμωνίας θα εξαπλωνόταν στο δωμάτιο για ώρες.
Θεωρία κίνησης Brown: τυχαίοι περίπατοι.
Η θεωρία Smoluchowski-Einstein εξηγεί τους νόμους τόσο της διάχυσης όσο και της κίνησης Brown. Μπορούμε να εξετάσουμε αυτά τα μοτίβα χρησιμοποιώντας το παράδειγμα της διάχυσης. Αν η ταχύτητα ενός μορίου είναι u, τότε, κινούμενο σε ευθεία γραμμή, σε χρόνο t θα πάει την απόσταση L = ut, αλλά λόγω συγκρούσεων με άλλα μόρια, αυτό το μόριο δεν κινείται ευθύγραμμα, αλλά αλλάζει συνεχώς την κατεύθυνση της κίνησής του. Εάν ήταν δυνατό να σκιαγραφηθεί η διαδρομή ενός μορίου, δεν θα διέφερε ουσιαστικά από τα σχέδια που έλαβε ο Perrin. Από τέτοια σχήματα είναι σαφές ότι, λόγω χαοτικής κίνησης, το μόριο μετατοπίζεται κατά μια απόσταση s, σημαντικά μικρότερη από το L. Αυτές οι ποσότητες σχετίζονται με τη σχέση s =, όπου l είναι η απόσταση που το μόριο πετά από μια σύγκρουση σε ένα άλλο, η μέση ελεύθερη διαδρομή. Οι μετρήσεις έδειξαν ότι για μόρια αέρα σε κανονική ατμοσφαιρική πίεση l ~ 0,1 μm, που σημαίνει ότι με ταχύτητα 500 m/s ένα μόριο αζώτου ή οξυγόνου θα πετάξει σε 10.000 δευτερόλεπτα (λιγότερο από τρεις ώρες) απόσταση L = 5000 km και θα Η μετατόπιση από την αρχική θέση είναι μόνο s = 0,7 m (70 cm), γι' αυτό οι ουσίες κινούνται τόσο αργά λόγω της διάχυσης, ακόμη και στα αέρια.
Η διαδρομή ενός μορίου ως αποτέλεσμα της διάχυσης (ή η διαδρομή ενός σωματιδίου Brown) ονομάζεται τυχαίος περίπατος. Οι πνευματώδεις φυσικοί επανερμήνευσαν αυτή την έκφραση ως το περπάτημα του μεθυσμένου - «το μονοπάτι ενός μεθυσμένου». Αυτή η αναλογία επιτρέπει επίσης να συμπεράνει κανείς πολύ απλά ότι η βασική εξίσωση μιας τέτοιας διαδικασίας βασίζεται στο παράδειγμα της μονοδιάστατης κίνησης, η οποία είναι εύκολο να γενικευτεί σε τρισδιάστατη.
Ας υποθέσουμε ότι ένας αγενής ναύτης βγήκε από μια ταβέρνα αργά το βράδυ και κατευθύνθηκε στο δρόμο. Έχοντας περπατήσει το μονοπάτι l μέχρι το πλησιέστερο φανάρι, ξεκουράστηκε και πήγε... είτε πιο μακριά, στο διπλανό φανάρι, είτε πίσω, στην ταβέρνα - άλλωστε δεν θυμάται από πού ήρθε. Το ερώτημα είναι, θα αφήσει ποτέ το κολοκυθάκι, ή απλά θα περιπλανηθεί γύρω του, τώρα απομακρυνόμενος, τώρα πλησιάζοντας το; (Μια άλλη εκδοχή του προβλήματος αναφέρει ότι υπάρχουν βρώμικα χαντάκια και στις δύο άκρες του δρόμου, όπου τελειώνουν τα φώτα του δρόμου, και ρωτά αν ο ναύτης θα μπορέσει να αποφύγει να πέσει σε ένα από αυτά.) Διαισθητικά, φαίνεται ότι η δεύτερη απάντηση είναι σωστή. Αλλά είναι λάθος: αποδεικνύεται ότι ο ναύτης σταδιακά θα απομακρύνεται όλο και περισσότερο από το σημείο μηδέν, αν και πολύ πιο αργά από ό,τι αν περπατούσε μόνο προς μία κατεύθυνση. Δείτε πώς να το αποδείξετε.
Έχοντας περπατήσει για πρώτη φορά στο πλησιέστερο φανάρι (δεξιά ή αριστερά), ο ναύτης θα βρεθεί σε απόσταση s1 = ± l από το σημείο εκκίνησης. Εφόσον μας ενδιαφέρει μόνο η απόστασή του από αυτό το σημείο, αλλά όχι η κατεύθυνσή του, θα απαλλαγούμε από τα σημάδια τετραγωνίζοντας αυτήν την έκφραση: s12 = l2. Μετά από κάποιο χρονικό διάστημα, ο ναύτης, έχοντας ήδη ολοκληρώσει Ν «περιπλανήσεις», θα βρίσκεται σε απόσταση
SN = από την αρχή. Και έχοντας περάσει ξανά (προς μία κατεύθυνση) στον πλησιέστερο λαμπτήρα, σε απόσταση sN+1 = sN ± l, ή, χρησιμοποιώντας το τετράγωνο της μετατόπισης, s2N+1 = s2N ±2sN l + l2. Εάν ο ναύτης επαναλάβει αυτή την κίνηση πολλές φορές (από Ν σε Ν + 1), τότε ως αποτέλεσμα του μέσου όρου (κάνει το Νο βήμα προς τα δεξιά ή προς τα αριστερά με ίση πιθανότητα), ο όρος ±2sNl θα μειωθεί, οπότε αυτό (οι γωνιακές αγκύλες υποδεικνύουν τη μέση τιμή).
Αφού s12 = l2, λοιπόν
S22 = s12 + l2 = 2l2, s32 = s22 + l2 = 3ll2, κ.λπ., δηλ. s2N = Nl2 ή sN =l. Η συνολική απόσταση που διανύθηκε L μπορεί να γραφτεί τόσο ως το γινόμενο της ταχύτητας του ναύτη και του χρόνου ταξιδιού (L = ut), όσο και ως το γινόμενο του αριθμού των περιπλανήσεων και της απόστασης μεταξύ των φαναριών (L = Nl), επομένως, ut = Nl, από όπου N = ut/l και τέλος sN = . Έτσι, λαμβάνουμε την εξάρτηση της μετατόπισης του ναύτη (καθώς και του μορίου ή του σωματιδίου Brown) από το χρόνο. Για παράδειγμα, αν υπάρχουν 10 μέτρα μεταξύ των λαμπτήρων και ένας ναύτης περπατά με ταχύτητα 1 m/s, τότε σε μια ώρα κοινή διαδρομήθα είναι L = 3600 m = 3,6 km, ενώ η μετατόπιση από το σημείο μηδέν στον ίδιο χρόνο θα είναι ίση μόνο με s = 190 m. Σε τρεις ώρες θα καλύψει L = 10,8 km, και θα μετατοπιστεί κατά s = 330 m. και τα λοιπά.
Το γινόμενο ul στον τύπο που προκύπτει μπορεί να συγκριθεί με τον συντελεστή διάχυσης, ο οποίος, όπως έδειξε ο Ιρλανδός φυσικός και μαθηματικός George Gabriel Stokes (1819–1903), εξαρτάται από το μέγεθος των σωματιδίων και το ιξώδες του μέσου. Με βάση παρόμοιες εκτιμήσεις, ο Αϊνστάιν εξήγαγε την εξίσωσή του.
Η θεωρία της κίνησης Brown στην πραγματική ζωή.
Η θεωρία των τυχαίων περιπάτων έχει σημαντικές πρακτικές εφαρμογές. Λένε ότι ελλείψει ορόσημων (ο ήλιος, τα αστέρια, ο θόρυβος του αυτοκινητόδρομου ή ΣΙΔΗΡΟΔΡΟΜΙΚΗ ΓΡΑΜΜΗκ.λπ.) ένα άτομο περιπλανιέται στο δάσος, σε ένα χωράφι σε μια χιονοθύελλα ή σε πυκνή ομίχλη σε κύκλους, επιστρέφοντας όλη την ώρα στην αρχική του θέση. Στην πραγματικότητα, δεν περπατά σε κύκλους, αλλά περίπου με τον ίδιο τρόπο κινούνται τα μόρια ή τα σωματίδια Brown. Μπορεί να επιστρέψει στην αρχική του θέση, αλλά μόνο τυχαία. Όμως διασχίζει το δρόμο του πολλές φορές. Λένε επίσης ότι άνθρωποι παγωμένοι σε μια χιονοθύελλα βρέθηκαν «κάποια χιλιόμετρα» από την πλησιέστερη κατοικία ή δρόμο, αλλά στην πραγματικότητα το άτομο δεν είχε καμία πιθανότητα να περπατήσει αυτό το χιλιόμετρο, και να γιατί.
Για να υπολογίσετε πόσο θα μετατοπιστεί ένα άτομο ως αποτέλεσμα τυχαίων περιπάτων, πρέπει να γνωρίζετε την τιμή του l, δηλ. την απόσταση που μπορεί να περπατήσει ένα άτομο σε ευθεία γραμμή χωρίς ορόσημα. Αυτή η τιμή μετρήθηκε από τον Διδάκτωρ Γεωλογικών και Ορυκτολογικών Επιστημών B.S. Gorobets με τη βοήθεια εθελοντών φοιτητών. Αυτός, φυσικά, δεν τους άφησε σε ένα πυκνό δάσος ή σε ένα χιονισμένο γήπεδο, όλα ήταν πιο απλά - ο μαθητής τοποθετήθηκε στο κέντρο ενός άδειου σταδίου, με δεμένα μάτια και του ζητήθηκε να περπατήσει μέχρι το τέλος του γηπέδου ποδοσφαίρου στο πλήρης σιωπή (για να αποκλειστεί ο προσανατολισμός από ήχους). Αποδείχθηκε ότι κατά μέσο όρο ο μαθητής περπάτησε σε ευθεία γραμμή μόνο για περίπου 20 μέτρα (η απόκλιση από την ιδανική ευθεία δεν ξεπερνούσε τις 5°) και στη συνέχεια άρχισε να αποκλίνει όλο και περισσότερο από την αρχική κατεύθυνση. Στο τέλος, σταμάτησε, μακριά από το να φτάσει στην άκρη.
Αφήστε το τώρα άνθρωπος που περπατά(ή μάλλον, περιπλανιέται) στο δάσος με ταχύτητα 2 χιλιομέτρων την ώρα (για έναν δρόμο αυτό είναι πολύ αργό, αλλά για ένα πυκνό δάσος είναι πολύ γρήγορο), τότε αν η τιμή του l είναι 20 μέτρα, τότε σε ώρα θα καλύψει 2 km, αλλά θα μετατοπιστεί μόνο κατά 200 m, σε δύο ώρες - περίπου 280 m, σε τρεις ώρες - 350 m, σε 4 ώρες - 400 m, κλπ. Και κινούμενος σε ευθεία γραμμή με τέτοια ταχύτητα, ένα άτομο θα περπατούσε 8 χιλιόμετρα σε 4 ώρες, έτσι στις οδηγίες Σύμφωνα με τις προφυλάξεις ασφαλείας για την εργασία πεδίου, υπάρχει ο ακόλουθος κανόνας: εάν χαθούν ορόσημα, πρέπει να μείνετε στη θέση τους, να δημιουργήσετε ένα καταφύγιο και να περιμένετε το τέλος του κακοκαιρία (μπορεί να βγει ο ήλιος) ή για βοήθεια. Στο δάσος, τα ορόσημα - δέντρα ή θάμνοι - θα σας βοηθήσουν να κινηθείτε σε ευθεία γραμμή και κάθε φορά που χρειάζεται να μένετε σε δύο τέτοια ορόσημα - το ένα μπροστά, το άλλο πίσω. Αλλά, φυσικά, είναι καλύτερο να έχετε μαζί σας μια πυξίδα...
Ο Σκωτσέζος βοτανολόγος Ρόμπερτ Μπράουν (μερικές φορές το επώνυμό του μεταγράφεται ως Μπράουν) κατά τη διάρκεια της ζωής του, ως ο καλύτερος ειδικός στα φυτά, έλαβε τον τίτλο «Πρίγκιπας των Βοτανολόγων». Έκανε πολλές υπέροχες ανακαλύψεις. Το 1805, μετά από μια τετραετή αποστολή στην Αυστραλία, έφερε στην Αγγλία περίπου 4.000 είδη αυστραλιανών φυτών άγνωστα στους επιστήμονες και πέρασε πολλά χρόνια μελετώντας τα. Περιγράφονται φυτά που έφεραν από την Ινδονησία και την Κεντρική Αφρική. Σπούδασε φυσιολογία φυτών και για πρώτη φορά περιέγραψε λεπτομερώς τον πυρήνα ενός φυτικού κυττάρου. Η Ακαδημία Επιστημών της Αγίας Πετρούπολης τον έκανε επίτιμο μέλος. Αλλά το όνομα του επιστήμονα είναι πλέον ευρέως γνωστό όχι λόγω αυτών των εργασιών.
Το 1827 ο Μπράουν διεξήγαγε έρευνα για τη γύρη των φυτών. Ενδιαφερόταν ιδιαίτερα για το πώς η γύρη συμμετέχει στη διαδικασία της γονιμοποίησης. Κάποτε κοίταξε κάτω από ένα μικροσκόπιο κύτταρα γύρης από φυτό της Βόρειας Αμερικής. Clarkia pulchella(όμορφα clarkia) επιμήκεις κυτταροπλασματικοί κόκκοι αιωρούμενοι στο νερό. Ξαφνικά ο Μπράουν είδε ότι οι μικρότεροι στερεοί κόκκοι, που μετά βίας φαινόταν σε μια σταγόνα νερού, έτρεμαν συνεχώς και κινούνταν από μέρος σε μέρος. Διαπίστωσε ότι αυτές οι κινήσεις, σύμφωνα με τα λόγια του, «δεν συνδέονται ούτε με ροές στο υγρό ούτε με τη σταδιακή εξάτμισή του, αλλά είναι εγγενείς στα ίδια τα σωματίδια».
Η παρατήρηση του Μπράουν επιβεβαιώθηκε από άλλους επιστήμονες. Τα μικρότερα σωματίδια συμπεριφέρονταν σαν να ήταν ζωντανά και ο «χορός» των σωματιδίων επιταχύνθηκε με την αύξηση της θερμοκρασίας και τη μείωση του μεγέθους των σωματιδίων και σαφώς επιβραδύνθηκε όταν αντικαθιστούσε το νερό με ένα πιο παχύρρευστο μέσο. Αυτό το εκπληκτικό φαινόμενο δεν σταμάτησε ποτέ: μπορούσε να παρατηρηθεί για όσο χρονικό διάστημα επιθυμείτε. Στην αρχή, ο Μπράουν πίστευε ακόμη ότι τα ζωντανά όντα έπεσαν στο πεδίο του μικροσκοπίου, ειδικά επειδή η γύρη είναι τα αρσενικά αναπαραγωγικά κύτταρα των φυτών, αλλά υπήρχαν και σωματίδια από νεκρά φυτά, ακόμη και από αυτά που είχαν αποξηρανθεί εκατό χρόνια νωρίτερα σε φυτά. Τότε ο Μπράουν σκέφτηκε αν αυτά ήταν «στοιχειώδη μόρια ζωντανών όντων», για τα οποία μίλησε ο διάσημος Γάλλος φυσιοδίφης Ζορζ Μπουφόν (1707–1788), συγγραφέας ενός βιβλίου 36 τόμων. Φυσική ιστορία. Αυτή η υπόθεση χάθηκε όταν ο Μπράουν άρχισε να εξετάζει προφανώς άψυχα αντικείμενα. Στην αρχή ήταν πολύ μικρά σωματίδια άνθρακα, καθώς και αιθάλη και σκόνη από τον αέρα του Λονδίνου, στη συνέχεια λεπτοαλεσμένες ανόργανες ουσίες: γυαλί, πολλά διαφορετικά ορυκτά. «Ενεργά μόρια» υπήρχαν παντού: «Σε κάθε ορυκτό», έγραψε ο Μπράουν, «το οποίο κατάφερα να κονιοποιήσω σε τέτοιο βαθμό ώστε να μπορεί να αιωρηθεί στο νερό για κάποιο χρονικό διάστημα, βρήκα, σε μεγαλύτερες ή μικρότερες ποσότητες, αυτά τα μόρια ."
Πρέπει να πούμε ότι ο Μπράουν δεν διέθετε κανένα από τα πιο πρόσφατα μικροσκόπια. Στο άρθρο του τονίζει συγκεκριμένα ότι είχε συνηθισμένους αμφίκυρτους φακούς, τους οποίους χρησιμοποιούσε για αρκετά χρόνια. Και συνεχίζει λέγοντας: «Σε όλη τη διάρκεια της μελέτης συνέχισα να χρησιμοποιώ τους ίδιους φακούς με τους οποίους ξεκίνησα τη δουλειά, προκειμένου να δώσω μεγαλύτερη αξιοπιστία στις δηλώσεις μου και να τις κάνω όσο το δυνατόν πιο προσιτές στις συνηθισμένες παρατηρήσεις».
Τώρα, για να επαναλάβουμε την παρατήρηση του Μπράουν, αρκεί να έχουμε ένα όχι πολύ δυνατό μικροσκόπιο και να το χρησιμοποιήσουμε για να εξετάσουμε τον καπνό σε ένα μαυρισμένο κουτί, που φωτίζεται μέσα από μια πλευρική οπή με μια δέσμη έντονου φωτός. Σε ένα αέριο, το φαινόμενο εκδηλώνεται πολύ πιο καθαρά από ό,τι σε ένα υγρό: μικρά κομμάτια στάχτης ή αιθάλης (ανάλογα με την πηγή του καπνού) είναι ορατά, διασκορπίζουν το φως και πηδούν συνεχώς μπρος-πίσω.
Όπως συμβαίνει συχνά στην επιστήμη, πολλά χρόνια αργότερα οι ιστορικοί ανακάλυψαν ότι το 1670, ο εφευρέτης του μικροσκοπίου, ο Ολλανδός Antonie Leeuwenhoek, παρατήρησε προφανώς ένα παρόμοιο φαινόμενο, αλλά τη σπανιότητα και την ατέλεια των μικροσκοπίων, την εμβρυϊκή κατάσταση της μοριακής επιστήμης εκείνη την εποχή δεν τράβηξε την προσοχή στην παρατήρηση του Leeuwenhoek, επομένως η ανακάλυψη αποδίδεται δικαίως στον Brown, ο οποίος ήταν ο πρώτος που τη μελέτησε και την περιέγραψε λεπτομερώς.
Κίνηση Brown και ατομική-μοριακή θεωρία.
Το φαινόμενο που παρατήρησε ο Μπράουν έγινε γρήγορα ευρέως γνωστό. Ο ίδιος έδειξε τα πειράματά του σε πολλούς συναδέλφους (ο Μπράουν απαριθμεί δύο δωδεκάδες ονόματα). Αλλά ούτε ο ίδιος ο Μπράουν ούτε πολλοί άλλοι επιστήμονες για πολλά χρόνια μπορούσαν να εξηγήσουν αυτό το μυστηριώδες φαινόμενο, το οποίο ονομάστηκε «κίνημα Μπράουν». Οι κινήσεις των σωματιδίων ήταν εντελώς τυχαίες: σκίτσα των θέσεων τους που έγιναν σε διαφορετικά χρονικά σημεία (για παράδειγμα, κάθε λεπτό) δεν επέτρεψαν με την πρώτη ματιά να βρεθεί οποιοδήποτε σχέδιο σε αυτές τις κινήσεις.
Μια εξήγηση της κίνησης Brown (όπως ονομάστηκε αυτό το φαινόμενο) από την κίνηση των αόρατων μορίων δόθηκε μόνο στο τελευταίο τέταρτο του 19ου αιώνα, αλλά δεν έγινε αμέσως αποδεκτή από όλους τους επιστήμονες. Το 1863, ένας δάσκαλος της περιγραφικής γεωμετρίας από την Καρλσρούη (Γερμανία), ο Ludwig Christian Wiener (1826–1896), πρότεινε ότι το φαινόμενο συνδέθηκε με τις ταλαντωτικές κινήσεις αόρατων ατόμων. Αυτή ήταν η πρώτη, αν και πολύ μακριά από τη σύγχρονη, εξήγηση της κίνησης Brown από τις ιδιότητες των ίδιων των ατόμων και των μορίων. Είναι σημαντικό ότι ο Wiener είδε την ευκαιρία να χρησιμοποιήσει αυτό το φαινόμενο για να διεισδύσει στα μυστικά της δομής της ύλης. Ήταν ο πρώτος που προσπάθησε να μετρήσει την ταχύτητα κίνησης των σωματιδίων Brown και την εξάρτησή της από το μέγεθός τους. Είναι περίεργο ότι το 1921 Εκθέσεις της Εθνικής Ακαδημίας Επιστημών των ΗΠΑΔημοσιεύτηκε ένα έργο σχετικά με την κίνηση Brown ενός άλλου Wiener - του Norbert, του διάσημου ιδρυτή της κυβερνητικής.
Οι ιδέες του L.K. Wiener έγιναν αποδεκτές και αναπτύχθηκαν από πολλούς επιστήμονες - Sigmund Exner στην Αυστρία (και 33 χρόνια αργότερα - ο γιος του Felix), Giovanni Cantoni στην Ιταλία, Karl Wilhelm Negeli στη Γερμανία, Louis Georges Gouy στη Γαλλία, τρεις Βέλγοι ιερείς - Ιησουίτες Carbonelli, Delso και Tirion και άλλοι. Μεταξύ αυτών των επιστημόνων ήταν και ο μετέπειτα διάσημος Άγγλος φυσικός και χημικός William Ramsay. Σταδιακά έγινε σαφές ότι οι μικρότεροι κόκκοι ύλης χτυπιούνταν από όλες τις πλευρές από ακόμη μικρότερα σωματίδια, τα οποία δεν ήταν πλέον ορατά με μικροσκόπιο - όπως τα κύματα που λικνίζουν ένα μακρινό σκάφος δεν είναι ορατά από την ακτή, ενώ οι κινήσεις του σκάφους είναι ορατά αρκετά καθαρά. Όπως έγραψαν σε ένα από τα άρθρα το 1877, «...ο νόμος των μεγάλων αριθμών δεν μειώνει πλέον την επίδραση των συγκρούσεων στη μέση ομοιόμορφη πίεση· το αποτέλεσμά τους δεν θα είναι πλέον ίσο με μηδέν, αλλά θα αλλάζει συνεχώς την κατεύθυνση και μέγεθος."
Ποιοτικά, η εικόνα ήταν αρκετά εύλογη και ακόμη και οπτική. Ένα μικρό κλαδάκι ή ένα ζωύφιο πρέπει να κινείται με τον ίδιο περίπου τρόπο, να σπρώχνεται (ή να τραβιέται) σε διαφορετικές κατευθύνσεις από πολλά μυρμήγκια. Αυτά τα μικρότερα σωματίδια ήταν στην πραγματικότητα στο λεξιλόγιο των επιστημόνων, αλλά κανείς δεν τα είχε δει ποτέ. Ονομάζονταν μόρια. Μετάφραση από τα λατινικά, αυτή η λέξη σημαίνει «μικρή μάζα». Παραδόξως, αυτή ακριβώς είναι η εξήγηση που δίνει σε ένα παρόμοιο φαινόμενο ο Ρωμαίος φιλόσοφος Titus Lucretius Carus (περίπου 99–55 π.Χ.) στο διάσημο ποίημά του Σχετικά με τη φύση των πραγμάτων. Σε αυτό, αποκαλεί τα μικρότερα σωματίδια αόρατα στο μάτι «πρωταρχικές αρχές» των πραγμάτων.
Οι αρχές των πραγμάτων κινούνται πρώτα μόνες τους,
Ακολουθούν σώματα από τον μικρότερο συνδυασμό τους,
Κοντά, σαν να λέγαμε, σε ισχύ στις πρωταρχικές αρχές,
Κρυμμένοι από αυτούς, δεχόμενοι σοκ, αρχίζουν να αγωνίζονται,
Οι ίδιοι να κινούνται, ενθαρρύνοντας στη συνέχεια μεγαλύτερα σώματα.
Ξεκινώντας λοιπόν από την αρχή η κίνηση σιγά σιγά
Αγγίζει τα συναισθήματά μας και γίνεται επίσης ορατό
Σε εμάς και στους κόκκους της σκόνης που κινούνται στο φως του ήλιου,
Αν και οι δονήσεις από τις οποίες εμφανίζεται είναι ανεπαίσθητες...
Στη συνέχεια, αποδείχθηκε ότι ο Λουκρήτιος έκανε λάθος: είναι αδύνατο να παρατηρήσει κανείς την κίνηση του Brown με γυμνό μάτι και τα σωματίδια σκόνης σε μια ηλιαχτίδα που εισχώρησε σε ένα σκοτεινό δωμάτιο «χορεύουν» λόγω των κινήσεων στροβιλισμού του αέρα. Αλλά εξωτερικά και τα δύο φαινόμενα έχουν κάποιες ομοιότητες. Και μόνο τον 19ο αιώνα. Έγινε προφανές σε πολλούς επιστήμονες ότι η κίνηση των σωματιδίων Brown προκαλείται από τυχαίες κρούσεις των μορίων του μέσου. Τα κινούμενα μόρια συγκρούονται με σωματίδια σκόνης και άλλα στερεά σωματίδια που βρίσκονται στο νερό. Όσο υψηλότερη είναι η θερμοκρασία, τόσο πιο γρήγορη είναι η κίνηση. Εάν ένα κομμάτι σκόνης είναι μεγάλο, για παράδειγμα, έχει μέγεθος 0,1 mm (η διάμετρος είναι ένα εκατομμύριο φορές μεγαλύτερη από αυτή ενός μορίου νερού), τότε πολλές ταυτόχρονες κρούσεις σε αυτό από όλες τις πλευρές είναι αμοιβαία ισορροπημένες και πρακτικά δεν το κάνει. «Νιώσε» τα - περίπου το ίδιο με ένα κομμάτι ξύλου στο μέγεθος ενός πιάτου δεν θα «νιώσει» τις προσπάθειες πολλών μυρμηγκιών που θα το τραβήξουν ή θα το σπρώξουν σε διαφορετικές κατευθύνσεις. Εάν το σωματίδιο της σκόνης είναι σχετικά μικρό, θα κινηθεί προς τη μία ή την άλλη κατεύθυνση υπό την επίδραση κρούσεων από τα γύρω μόρια.
Τα σωματίδια Brownian έχουν μέγεθος της τάξης των 0,1–1 μm, δηλ. από το ένα χιλιοστό έως το ένα δέκατο χιλιοστό του χιλιοστού, γι' αυτό ο Μπράουν μπόρεσε να διακρίνει την κίνησή τους επειδή κοίταζε μικροσκοπικούς κυτταροπλασματικούς κόκκους και όχι την ίδια τη γύρη (για την οποία συχνά γράφεται λανθασμένα). Το πρόβλημα είναι ότι τα κύτταρα γύρης είναι πολύ μεγάλα. Έτσι, στη γύρη του λιβαδιού, που μεταφέρεται από τον άνεμο και προκαλεί αλλεργικές ασθένειες στον άνθρωπο (πυρετός εκ χόρτου), το μέγεθος των κυττάρων είναι συνήθως της τάξης των 20 - 50 microns, δηλ. είναι πολύ μεγάλα για να παρατηρήσουν την κίνηση Brown. Είναι επίσης σημαντικό να σημειωθεί ότι μεμονωμένες κινήσεις ενός σωματιδίου Brown συμβαίνουν πολύ συχνά και σε πολύ μικρές αποστάσεις, έτσι ώστε να είναι αδύνατο να τις δούμε, αλλά κάτω από ένα μικροσκόπιο, κινήσεις που έχουν συμβεί σε μια συγκεκριμένη χρονική περίοδο είναι ορατές.
Φαίνεται ότι το ίδιο το γεγονός της ύπαρξης της κίνησης Brown απέδειξε ξεκάθαρα τη μοριακή δομή της ύλης, αλλά ακόμη και στις αρχές του 20ου αιώνα. Υπήρχαν επιστήμονες, συμπεριλαμβανομένων φυσικών και χημικών, που δεν πίστευαν στην ύπαρξη μορίων. Η ατομική-μοριακή θεωρία μόνο αργά και με δυσκολία κέρδισε την αναγνώριση. Έτσι, ο κορυφαίος Γάλλος οργανικός χημικός Marcelin Berthelot (1827–1907) έγραψε: «Η έννοια ενός μορίου, από τη σκοπιά της γνώσης μας, είναι αβέβαιη, ενώ μια άλλη έννοια - ένα άτομο - είναι καθαρά υποθετική». Ο διάσημος Γάλλος χημικός A. Saint-Clair Deville (1818–1881) μίλησε ακόμη πιο ξεκάθαρα: «Δεν αποδέχομαι το νόμο του Avogadro, ούτε το άτομο, ούτε το μόριο, γιατί αρνούμαι να πιστέψω σε αυτό που ούτε μπορώ να δω ούτε να παρατηρήσω. ” Και ο Γερμανός φυσικοχημικός Wilhelm Ostwald (1853–1932), βραβευμένος με Νόμπελ, ένας από τους ιδρυτές της φυσικής χημείας, στις αρχές του 20ού αιώνα. αρνήθηκε κατηγορηματικά την ύπαρξη ατόμων. Κατάφερε να γράψει ένα τρίτομο εγχειρίδιο χημείας στο οποίο η λέξη «άτομο» δεν αναφέρεται ποτέ καν. Μιλώντας στις 19 Απριλίου 1904, με μια μεγάλη έκθεση στο Βασιλικό Ίδρυμα στα μέλη της Αγγλικής Χημικής Εταιρείας, ο Ostwald προσπάθησε να αποδείξει ότι τα άτομα δεν υπάρχουν και «αυτό που ονομάζουμε ύλη είναι μόνο μια συλλογή ενεργειών που συλλέγονται μαζί σε ένα δεδομένο θέση."
Αλλά ακόμη και εκείνοι οι φυσικοί που αποδέχονταν τη μοριακή θεωρία δεν μπορούσαν να πιστέψουν ότι η εγκυρότητα της ατομικής-μοριακής θεωρίας αποδείχθηκε με τόσο απλό τρόπο, έτσι προβλήθηκαν ποικίλοι εναλλακτικοί λόγοι για να εξηγηθεί το φαινόμενο. Και αυτό είναι απολύτως σύμφωνα με το πνεύμα της επιστήμης: μέχρι να εντοπιστεί με σαφήνεια η αιτία ενός φαινομένου, είναι δυνατό (και ακόμη και απαραίτητο) να υποθέσουμε διάφορες υποθέσεις, οι οποίες θα πρέπει, αν είναι δυνατόν, να ελεγχθούν πειραματικά ή θεωρητικά. Έτσι, το 1905, ένα σύντομο άρθρο του καθηγητή φυσικής της Αγίας Πετρούπολης N.A. Gezehus, δασκάλου του διάσημου ακαδημαϊκού A.F. Ioffe, δημοσιεύτηκε στο Εγκυκλοπαιδικό Λεξικό Brockhaus and Efron. Ο Gesehus έγραψε ότι, σύμφωνα με ορισμένους επιστήμονες, η κίνηση Brown προκαλείται από «ακτίνες φωτός ή θερμότητας που περνούν μέσα από ένα υγρό» και καταλήγει σε «απλές ροές μέσα σε ένα υγρό που δεν έχουν καμία σχέση με τις κινήσεις των μορίων» και αυτές οι ροές μπορεί να προκληθεί από «εξάτμιση, διάχυση και άλλους λόγους». Άλλωστε, ήταν ήδη γνωστό ότι μια πολύ παρόμοια κίνηση σωματιδίων σκόνης στον αέρα προκαλείται ακριβώς από ροές δίνης. Αλλά η εξήγηση που έδωσε ο Gesehus θα μπορούσε εύκολα να διαψευσθεί πειραματικά: αν κοιτάξετε δύο σωματίδια Brownian που βρίσκονται πολύ κοντά το ένα στο άλλο μέσω ενός ισχυρού μικροσκοπίου, οι κινήσεις τους θα αποδειχθούν εντελώς ανεξάρτητες. Εάν αυτές οι κινήσεις προκλήθηκαν από οποιεσδήποτε ροές στο υγρό, τότε τέτοια γειτονικά σωματίδια θα κινούνταν συντονισμένα.
Θεωρία της κίνησης Brown.
Στις αρχές του 20ου αιώνα. Οι περισσότεροι επιστήμονες κατανόησαν τη μοριακή φύση της κίνησης Brown. Αλλά όλες οι εξηγήσεις παρέμειναν καθαρά ποιοτικές· καμία ποσοτική θεωρία δεν μπορούσε να αντέξει πειραματικές δοκιμές. Επιπλέον, τα ίδια τα πειραματικά αποτελέσματα ήταν ασαφή: το φανταστικό θέαμα των ασταμάτητα ορμητικών σωματιδίων υπνώτισε τους πειραματιστές και δεν γνώριζαν ακριβώς ποια χαρακτηριστικά του φαινομένου έπρεπε να μετρηθούν.
Παρά τη φαινομενική πλήρη διαταραχή, ήταν ακόμα δυνατό να περιγραφούν οι τυχαίες κινήσεις των σωματιδίων Brown με μια μαθηματική σχέση. Για πρώτη φορά, μια αυστηρή εξήγηση της κίνησης Brown δόθηκε το 1904 από τον Πολωνό φυσικό Marian Smoluchowski (1872–1917), ο οποίος εκείνα τα χρόνια εργαζόταν στο Πανεπιστήμιο του Lviv. Ταυτόχρονα, η θεωρία αυτού του φαινομένου αναπτύχθηκε από τον Albert Einstein (1879–1955), έναν ελάχιστα γνωστό τότε εμπειρογνώμονα 2ης κατηγορίας στο Γραφείο Διπλωμάτων Ευρεσιτεχνίας της ελβετικής πόλης της Βέρνης. Το άρθρο του, που δημοσιεύτηκε τον Μάιο του 1905 στο γερμανικό περιοδικό Annalen der Physik, είχε τον τίτλο Σχετικά με την κίνηση των σωματιδίων που αιωρούνται σε ένα ρευστό σε ηρεμία, που απαιτείται από τη μοριακή κινητική θεωρία της θερμότητας. Με αυτό το όνομα, ο Αϊνστάιν ήθελε να δείξει ότι η μοριακή κινητική θεωρία της δομής της ύλης υπονοεί απαραίτητα την ύπαρξη τυχαίας κίνησης των μικρότερων στερεών σωματιδίων στα υγρά.
Είναι περίεργο ότι στην αρχή αυτού του άρθρου, ο Αϊνστάιν γράφει ότι είναι εξοικειωμένος με το ίδιο το φαινόμενο, αν και επιφανειακά: «Είναι πιθανό οι εν λόγω κινήσεις να είναι ταυτόσημες με τη λεγόμενη μοριακή κίνηση Brown, αλλά τα διαθέσιμα δεδομένα Για μένα σχετικά με τα τελευταία είναι τόσο ανακριβή που δεν μπορούσα να διατυπώσω μια συγκεκριμένη άποψη». Και δεκαετίες αργότερα, ήδη στα τέλη της ζωής του, ο Αϊνστάιν έγραψε κάτι διαφορετικό στα απομνημονεύματά του - ότι δεν ήξερε καθόλου για την κίνηση Brown και στην πραγματικότητα την «ανακάλυψε ξανά» καθαρά θεωρητικά: «Μη γνωρίζοντας ότι οι παρατηρήσεις της «κίνησης Brown» ήταν από καιρό γνωστό, ανακάλυψα ότι η ατομική θεωρία οδηγεί στην ύπαρξη παρατηρήσιμης κίνησης μικροσκοπικών αιωρούμενων σωματιδίων." Όπως και να έχει, το θεωρητικό άρθρο του Αϊνστάιν τελείωσε με μια άμεση κλήση στους πειραματιστές να δοκιμάσουν τα συμπεράσματά του πειραματικά: "Αν κάποιος ερευνητής μπορούσε σύντομα να απαντήσει τα ερωτήματα που τίθενται εδώ ρωτούν!" – τελειώνει το άρθρο του με ένα τόσο ασυνήθιστο επιφώνημα.
Η απάντηση στην παθιασμένη έκκληση του Αϊνστάιν δεν άργησε να έρθει.
Σύμφωνα με τη θεωρία Smoluchowski-Einstein, η μέση τιμή της τετραγωνικής μετατόπισης ενός σωματιδίου Brown ( μικρό 2) για το χρόνο tευθέως ανάλογη της θερμοκρασίας Τκαι αντιστρόφως ανάλογο με το ιξώδες του υγρού h, μέγεθος σωματιδίων rκαι η σταθερά του Avogadro
ΝΕΝΑ: μικρό 2 = 2RTt/6ph rNΕΝΑ,
Οπου R– σταθερά αερίου. Έτσι, εάν σε 1 λεπτό ένα σωματίδιο με διάμετρο 1 μm κινείται κατά 10 μm, τότε σε 9 λεπτά - κατά 10 = 30 μm, σε 25 λεπτά - κατά 10 = 50 μm, κ.λπ. Κάτω από παρόμοιες συνθήκες, ένα σωματίδιο με διάμετρο 0,25 μm για τις ίδιες χρονικές περιόδους (1, 9 και 25 λεπτά) θα κινηθεί κατά 20, 60 και 100 μm, αντίστοιχα, αφού = 2. Είναι σημαντικό ο παραπάνω τύπος να περιλαμβάνει Η σταθερά του Avogadro, η οποία επομένως, μπορεί να προσδιοριστεί με ποσοτικές μετρήσεις της κίνησης ενός σωματιδίου Brown, που έγινε από τον Γάλλο φυσικό Jean Baptiste Perrin (1870–1942).
Το 1908, ο Perrin άρχισε ποσοτικές παρατηρήσεις της κίνησης των σωματιδίων Brown στο μικροσκόπιο. Χρησιμοποίησε ένα υπερμικροσκόπιο, που εφευρέθηκε το 1902, το οποίο επέτρεψε την ανίχνευση των μικρότερων σωματιδίων διαχέοντας φως πάνω τους από έναν ισχυρό πλευρικό φωτιστή. Ο Perrin έλαβε μικροσκοπικές μπάλες σχεδόν σφαιρικού σχήματος και περίπου ίδιου μεγέθους από κόμμι, τον συμπυκνωμένο χυμό ορισμένων τροπικών δέντρων (χρησιμοποιείται επίσης ως κίτρινη ακουαρέλα). Αυτά τα μικροσκοπικά σφαιρίδια εναιωρήθηκαν σε γλυκερίνη που περιείχε 12% νερό. το παχύρρευστο υγρό εμπόδιζε την εμφάνιση εσωτερικών ροών σε αυτό που θα θόλωναν την εικόνα. Οπλισμένος με ένα χρονόμετρο, ο Perrin σημείωσε και στη συνέχεια σκιαγράφησε (φυσικά, σε πολύ μεγεθυμένη κλίμακα) σε ένα γραφικό φύλλο χαρτιού τη θέση των σωματιδίων σε τακτά χρονικά διαστήματα, για παράδειγμα, κάθε μισό λεπτό. Συνδέοντας τα σημεία που προέκυψαν με ευθείες γραμμές, απέκτησε περίπλοκες τροχιές, μερικές από αυτές φαίνονται στο σχήμα (προέρχονται από το βιβλίο του Perrin Άτομα, που εκδόθηκε το 1920 στο Παρίσι). Μια τέτοια χαοτική, άτακτη κίνηση των σωματιδίων οδηγεί στο γεγονός ότι κινούνται στο χώρο αρκετά αργά: το άθροισμα των τμημάτων είναι πολύ μεγαλύτερο από τη μετατόπιση του σωματιδίου από το πρώτο σημείο στο τελευταίο.

Διαδοχικές θέσεις κάθε 30 δευτερόλεπτα τριών σωματιδίων Brownian - μπάλες τσίχλας με μέγεθος περίπου 1 micron. Ένα κελί αντιστοιχεί σε απόσταση 3 μm. Εάν ο Perrin μπορούσε να καθορίσει τη θέση των σωματιδίων Brownian όχι μετά από 30, αλλά μετά από 3 δευτερόλεπτα, τότε οι ευθείες γραμμές μεταξύ κάθε γειτονικού σημείου θα μετατρέπονταν στην ίδια πολύπλοκη διακεκομμένη γραμμή ζιγκ-ζαγκ, μόνο σε μικρότερη κλίμακα.
Χρησιμοποιώντας τον θεωρητικό τύπο και τα αποτελέσματά του, ο Perrin έλαβε μια τιμή για τον αριθμό του Avogadro που ήταν αρκετά ακριβής για εκείνη την εποχή: 6,8 . 10 23 . Ο Perrin χρησιμοποίησε επίσης ένα μικροσκόπιο για να μελετήσει την κατακόρυφη κατανομή των σωματιδίων Brown ( εκ. ΝΟΜΟΣ ΤΟΥ AVOGADRO) και έδειξε ότι, παρά τη δράση της βαρύτητας, παραμένουν αιωρούμενα σε διάλυμα. Ο Perrin έχει και άλλα σημαντικά έργα. Το 1895, απέδειξε ότι οι καθοδικές ακτίνες είναι αρνητικά ηλεκτρικά φορτία (ηλεκτρόνια) και το 1901 πρότεινε για πρώτη φορά ένα πλανητικό μοντέλο του ατόμου. Το 1926 τιμήθηκε με το Νόμπελ Φυσικής.
Τα αποτελέσματα που έλαβε ο Perrin επιβεβαίωσαν τα θεωρητικά συμπεράσματα του Αϊνστάιν. Έκανε έντονη εντύπωση. Όπως έγραψε ο Αμερικανός φυσικός A. Pais πολλά χρόνια αργότερα, «δεν παύεις ποτέ να εκπλήσσεσαι με αυτό το αποτέλεσμα, που προκύπτει με έναν τόσο απλό τρόπο: αρκεί να ετοιμάσεις ένα εναιώρημα από μπάλες, το μέγεθος των οποίων είναι μεγάλο σε σύγκριση με το μέγεθος. από απλά μόρια, πάρτε ένα χρονόμετρο και ένα μικροσκόπιο και μπορείτε να προσδιορίσετε τη σταθερά του Avogadro!». Θα μπορούσε επίσης να εκπλαγεί κανείς: περιγραφές νέων πειραμάτων για την κίνηση Brown εξακολουθούν να εμφανίζονται σε επιστημονικά περιοδικά (Nature, Science, Journal of Chemical Education) κατά καιρούς! Μετά τη δημοσίευση των αποτελεσμάτων του Perrin, ο Ostwald, πρώην αντίπαλος του ατομισμού, παραδέχτηκε ότι «η σύμπτωση της κίνησης Brown με τις απαιτήσεις της κινητικής υπόθεσης... δίνει τώρα στον πιο προσεκτικό επιστήμονα το δικαίωμα να μιλήσει για πειραματική απόδειξη της ατομικής θεωρίας της ύλης. Έτσι, η ατομική θεωρία έχει ανυψωθεί στην τάξη μιας επιστημονικής, καλά θεμελιωμένης θεωρίας». Τον απηχεί ο Γάλλος μαθηματικός και φυσικός Ανρί Πουανκαρέ: «Ο λαμπρός προσδιορισμός του αριθμού των ατόμων από τον Περέν ολοκλήρωσε τον θρίαμβο του ατομισμού... Το άτομο των χημικών έχει πλέον γίνει πραγματικότητα».
Brownian κίνηση και διάχυση.
Η κίνηση των σωματιδίων Brown μοιάζει πολύ στην εμφάνιση με την κίνηση μεμονωμένων μορίων ως αποτέλεσμα της θερμικής τους κίνησης. Αυτή η κίνηση ονομάζεται διάχυση. Ακόμη και πριν από το έργο του Smoluchowski και του Einstein, οι νόμοι της μοριακής κίνησης καθιερώθηκαν στην απλούστερη περίπτωση της αέριας κατάστασης της ύλης. Αποδείχθηκε ότι τα μόρια στα αέρια κινούνται πολύ γρήγορα - με την ταχύτητα μιας σφαίρας, αλλά δεν μπορούν να πετάξουν μακριά, καθώς πολύ συχνά συγκρούονται με άλλα μόρια. Για παράδειγμα, τα μόρια οξυγόνου και αζώτου στον αέρα, που κινούνται με μέση ταχύτητα περίπου 500 m/s, αντιμετωπίζουν περισσότερες από ένα δισεκατομμύριο συγκρούσεις κάθε δευτερόλεπτο. Επομένως, η διαδρομή του μορίου, αν μπορούσε να ακολουθηθεί, θα ήταν μια πολύπλοκη διακεκομμένη γραμμή. Τα σωματίδια Brown περιγράφουν επίσης μια παρόμοια τροχιά εάν η θέση τους καταγράφεται σε συγκεκριμένα χρονικά διαστήματα. Τόσο η διάχυση όσο και η κίνηση Brown είναι συνέπεια της χαοτικής θερμικής κίνησης των μορίων και επομένως περιγράφονται από παρόμοιες μαθηματικές σχέσεις. Η διαφορά είναι ότι τα μόρια στα αέρια κινούνται σε ευθεία γραμμή μέχρι να συγκρουστούν με άλλα μόρια, μετά από την οποία αλλάζουν κατεύθυνση. Ένα σωματίδιο Brown, σε αντίθεση με ένα μόριο, δεν εκτελεί «ελεύθερες πτήσεις», αλλά βιώνει πολύ συχνά μικρές και ακανόνιστες «τρεμούλες», με αποτέλεσμα να μετατοπίζεται χαοτικά προς τη μία ή την άλλη κατεύθυνση. Οι υπολογισμοί έχουν δείξει ότι για ένα σωματίδιο μεγέθους 0,1 μm, μια κίνηση συμβαίνει σε τρία δισεκατομμυριοστά του δευτερολέπτου σε απόσταση μόνο 0,5 nm (1 nm = 0,001 μm). Όπως εύστοχα το θέτει ένας συγγραφέας, αυτό θυμίζει τη μετακίνηση ενός άδειου κουτιού μπύρας σε μια πλατεία όπου έχει συγκεντρωθεί πλήθος κόσμου.
Η διάχυση είναι πολύ πιο εύκολο να παρατηρηθεί από την κίνηση Brown, καθώς δεν απαιτεί μικροσκόπιο: οι κινήσεις δεν παρατηρούνται μεμονωμένων σωματιδίων, αλλά των τεράστιων μαζών τους, απλά πρέπει να διασφαλίσετε ότι η διάχυση δεν υπερτίθεται από τη μεταφορά - ανάμειξη της ύλης ως αποτέλεσμα των ροών στροβιλισμού (τέτοιες ροές είναι εύκολο να παρατηρηθούν, τοποθετώντας μια σταγόνα έγχρωμου διαλύματος, όπως μελάνι, σε ένα ποτήρι ζεστό νερό).
Η διάχυση είναι βολικό να παρατηρείται σε παχιά πηκτώματα. Ένα τέτοιο τζελ μπορεί να παρασκευαστεί, για παράδειγμα, σε ένα βάζο πενικιλίνης παρασκευάζοντας ένα διάλυμα ζελατίνης 4-5% σε αυτό. Η ζελατίνη πρέπει πρώτα να φουσκώσει για αρκετές ώρες και στη συνέχεια διαλύεται πλήρως με ανάδευση κατεβάζοντας το βάζο σε ζεστό νερό. Μετά την ψύξη, λαμβάνεται ένα μη ρέον πήκτωμα με τη μορφή μιας διαφανούς, ελαφρώς θολής μάζας. Εάν, χρησιμοποιώντας αιχμηρά τσιμπιδάκια, εισάγετε προσεκτικά έναν μικρό κρύσταλλο υπερμαγγανικού καλίου («υπερμαγγανικό κάλιο») στο κέντρο αυτής της μάζας, ο κρύσταλλος θα παραμείνει κρεμασμένος στο σημείο που έμεινε, καθώς το τζελ εμποδίζει την πτώση του. Μέσα σε λίγα λεπτά, μια βιολετί σφαίρα θα αρχίσει να μεγαλώνει γύρω από τον κρύσταλλο· με την πάροδο του χρόνου, γίνεται όλο και μεγαλύτερη έως ότου τα τοιχώματα του βάζου παραμορφώσουν το σχήμα του. Το ίδιο αποτέλεσμα μπορεί να επιτευχθεί χρησιμοποιώντας έναν κρύσταλλο θειικού χαλκού, μόνο σε αυτή την περίπτωση η μπάλα δεν θα αποδειχθεί μοβ, αλλά μπλε.
Είναι ξεκάθαρο γιατί βγήκε η μπάλα: Τα ιόντα MnO 4 - σχηματίζονται όταν διαλύεται ο κρύσταλλος, μπαίνουν σε διάλυμα (το πήκτωμα είναι κυρίως νερό) και, ως αποτέλεσμα της διάχυσης, κινούνται ομοιόμορφα προς όλες τις κατευθύνσεις, ενώ η βαρύτητα δεν έχει ουσιαστικά καμία επίδραση στο ρυθμός διάχυσης. Η διάχυση στο υγρό είναι πολύ αργή: θα χρειαστούν πολλές ώρες για να μεγαλώσει η μπάλα αρκετά εκατοστά. Στα αέρια, η διάχυση είναι πολύ πιο γρήγορη, αλλά παρόλα αυτά, αν ο αέρας δεν αναμειγνυόταν, η μυρωδιά του αρώματος ή της αμμωνίας θα εξαπλωνόταν στο δωμάτιο για ώρες.
Θεωρία κίνησης Brown: τυχαίοι περίπατοι.
Η θεωρία Smoluchowski-Einstein εξηγεί τους νόμους τόσο της διάχυσης όσο και της κίνησης Brown. Μπορούμε να εξετάσουμε αυτά τα μοτίβα χρησιμοποιώντας το παράδειγμα της διάχυσης. Αν η ταχύτητα του μορίου είναι u, τότε, κινούμενος σε ευθεία γραμμή, στο χρόνο tθα πάει την απόσταση μεγάλο = ut, αλλά λόγω συγκρούσεων με άλλα μόρια, το μόριο αυτό δεν κινείται σε ευθεία γραμμή, αλλά αλλάζει συνεχώς την κατεύθυνση της κίνησής του. Εάν ήταν δυνατό να σκιαγραφηθεί η διαδρομή ενός μορίου, δεν θα διέφερε ουσιαστικά από τα σχέδια που έλαβε ο Perrin. Από αυτά τα σχήματα είναι σαφές ότι λόγω της χαοτικής κίνησης το μόριο μετατοπίζεται από μια απόσταση μικρό, σημαντικά λιγότερο από μεγάλο. Αυτές οι ποσότητες σχετίζονται με τη σχέση μικρό= , όπου l είναι η απόσταση που πετάει ένα μόριο από τη μια σύγκρουση στην άλλη, η μέση ελεύθερη διαδρομή. Οι μετρήσεις έχουν δείξει ότι για μόρια αέρα σε κανονική ατμοσφαιρική πίεση l ~ 0,1 μm, που σημαίνει ότι με ταχύτητα 500 m/s ένα μόριο αζώτου ή οξυγόνου θα διανύσει την απόσταση σε 10.000 δευτερόλεπτα (λιγότερο από τρεις ώρες) μεγάλο= 5000 km και θα μετατοπιστεί από την αρχική θέση μόνο μικρό= 0,7 m (70 cm), γι' αυτό οι ουσίες κινούνται τόσο αργά λόγω της διάχυσης, ακόμη και στα αέρια.
Η διαδρομή ενός μορίου ως αποτέλεσμα της διάχυσης (ή η διαδρομή ενός σωματιδίου Brown) ονομάζεται τυχαίος περίπατος. Οι πνευματώδεις φυσικοί επανερμήνευσαν αυτή την έκφραση ως το περπάτημα του μεθυσμένου - «το μονοπάτι ενός μεθυσμένου». Αυτή η αναλογία επιτρέπει επίσης να συμπεράνει κανείς πολύ απλά ότι η βασική εξίσωση μιας τέτοιας διαδικασίας βασίζεται στο παράδειγμα της μονοδιάστατης κίνησης, η οποία είναι εύκολο να γενικευτεί σε τρισδιάστατη.
Ας υποθέσουμε ότι ένας αγενής ναύτης βγήκε από μια ταβέρνα αργά το βράδυ και κατευθύνθηκε στο δρόμο. Έχοντας περπατήσει το μονοπάτι l μέχρι το πλησιέστερο φανάρι, ξεκουράστηκε και πήγε... είτε πιο μακριά, στο διπλανό φανάρι, είτε πίσω, στην ταβέρνα - άλλωστε δεν θυμάται από πού ήρθε. Το ερώτημα είναι, θα αφήσει ποτέ το κολοκυθάκι, ή απλά θα περιπλανηθεί γύρω του, τώρα απομακρυνόμενος, τώρα πλησιάζοντας το; (Μια άλλη εκδοχή του προβλήματος αναφέρει ότι υπάρχουν βρώμικα χαντάκια και στις δύο άκρες του δρόμου, όπου τελειώνουν τα φώτα του δρόμου, και ρωτά αν ο ναύτης θα μπορέσει να αποφύγει να πέσει σε ένα από αυτά.) Διαισθητικά, φαίνεται ότι η δεύτερη απάντηση είναι σωστή. Αλλά είναι λάθος: αποδεικνύεται ότι ο ναύτης σταδιακά θα απομακρύνεται όλο και περισσότερο από το σημείο μηδέν, αν και πολύ πιο αργά από ό,τι αν περπατούσε μόνο προς μία κατεύθυνση. Δείτε πώς να το αποδείξετε.
Έχοντας περάσει την πρώτη φορά στην πλησιέστερη λάμπα (δεξιά ή αριστερά), ο ναύτης θα βρίσκεται σε απόσταση μικρό 1 = ± l από το σημείο εκκίνησης. Επειδή μας ενδιαφέρει μόνο η απόστασή του από αυτό το σημείο, αλλά όχι η κατεύθυνσή του, θα απαλλαγούμε από τα σημάδια τετραγωνίζοντας αυτήν την έκφραση: μικρό 1 2 = l 2. Μετά από λίγο καιρό, ο ναύτης, έχοντας ήδη ολοκληρώσει Ν«περιπλανώμενος», θα είναι σε απόσταση
s N= από την αρχή. Και έχοντας περπατήσει ξανά (προς μία κατεύθυνση) μέχρι το πλησιέστερο φανάρι, σε απόσταση s N+1 = s N± l ή, χρησιμοποιώντας το τετράγωνο της μετατόπισης, μικρό 2 Ν+1 = μικρό 2 Ν± 2 s N l + l 2. Αν ο ναύτης επαναλάβει αυτή την κίνηση πολλές φορές (από Νπριν Ν+ 1), τότε ως αποτέλεσμα του μέσου όρου (περνά με ίση πιθανότητα Ντο βήμα προς τα δεξιά ή προς τα αριστερά), όρος ± 2 s NΘα ακυρώσω, άρα s 2 Ν+1 = s2 Ν+ l 2> (οι γωνιακές αγκύλες υποδεικνύουν τη μέση τιμή) L = 3600 m = 3,6 km, ενώ η μετατόπιση από το σημείο μηδέν για τον ίδιο χρόνο θα είναι ίση μόνο με μικρό= = 190 μ. Σε τρεις ώρες θα περάσει μεγάλο= 10,8 km, και θα μετατοπιστεί κατά μικρό= 330 m, κ.λπ.
Δουλειά uΤο l στον προκύπτον τύπο μπορεί να συγκριθεί με τον συντελεστή διάχυσης, ο οποίος, όπως έδειξε ο Ιρλανδός φυσικός και μαθηματικός George Gabriel Stokes (1819–1903), εξαρτάται από το μέγεθος των σωματιδίων και το ιξώδες του μέσου. Με βάση παρόμοιες εκτιμήσεις, ο Αϊνστάιν εξήγαγε την εξίσωσή του.
Η θεωρία της κίνησης Brown στην πραγματική ζωή.
Η θεωρία των τυχαίων περιπάτων έχει σημαντικές πρακτικές εφαρμογές. Λένε ότι ελλείψει ορόσημων (ο ήλιος, τα αστέρια, ο θόρυβος ενός αυτοκινητόδρομου ή σιδηροδρόμου κ.λπ.), ένα άτομο περιπλανιέται στο δάσος, σε ένα χωράφι σε μια χιονοθύελλα ή σε πυκνή ομίχλη σε κύκλους, επιστρέφοντας πάντα στο δικό του αρχικό μέρος. Στην πραγματικότητα, δεν περπατά σε κύκλους, αλλά περίπου με τον ίδιο τρόπο κινούνται τα μόρια ή τα σωματίδια Brown. Μπορεί να επιστρέψει στην αρχική του θέση, αλλά μόνο τυχαία. Όμως διασχίζει το δρόμο του πολλές φορές. Λένε επίσης ότι άνθρωποι παγωμένοι σε μια χιονοθύελλα βρέθηκαν «κάποια χιλιόμετρα» από την πλησιέστερη κατοικία ή δρόμο, αλλά στην πραγματικότητα το άτομο δεν είχε καμία πιθανότητα να περπατήσει αυτό το χιλιόμετρο, και να γιατί.
Για να υπολογίσετε πόσο θα μετατοπιστεί ένα άτομο ως αποτέλεσμα τυχαίων περιπάτων, πρέπει να γνωρίζετε την τιμή του l, δηλ. την απόσταση που μπορεί να περπατήσει ένα άτομο σε ευθεία γραμμή χωρίς ορόσημα. Αυτή η τιμή μετρήθηκε από τον Διδάκτωρ Γεωλογικών και Ορυκτολογικών Επιστημών B.S. Gorobets με τη βοήθεια εθελοντών φοιτητών. Αυτός, φυσικά, δεν τους άφησε σε ένα πυκνό δάσος ή σε ένα χιονισμένο γήπεδο, όλα ήταν πιο απλά - ο μαθητής τοποθετήθηκε στο κέντρο ενός άδειου σταδίου, με δεμένα μάτια και του ζητήθηκε να περπατήσει μέχρι το τέλος του γηπέδου ποδοσφαίρου στο πλήρης σιωπή (για να αποκλειστεί ο προσανατολισμός από ήχους). Αποδείχθηκε ότι κατά μέσο όρο ο μαθητής περπάτησε σε ευθεία γραμμή μόνο για περίπου 20 μέτρα (η απόκλιση από την ιδανική ευθεία δεν ξεπερνούσε τις 5°) και στη συνέχεια άρχισε να αποκλίνει όλο και περισσότερο από την αρχική κατεύθυνση. Στο τέλος, σταμάτησε, μακριά από το να φτάσει στην άκρη.
Αφήστε τώρα ένα άτομο να περπατήσει (ή μάλλον, να περιπλανηθεί) στο δάσος με ταχύτητα 2 χιλιομέτρων την ώρα (για έναν δρόμο αυτό είναι πολύ αργό, αλλά για ένα πυκνό δάσος είναι πολύ γρήγορο), τότε αν η τιμή του l είναι 20 μέτρα, μετά σε μια ώρα θα διανύσει 2 χλμ., αλλά θα κινηθεί μόνο 200 μ., σε δύο ώρες - περίπου 280 μ., σε τρεις ώρες - 350 μ., σε 4 ώρες - 400 μ. κ.λπ. Και κινούμενος σε ευθεία γραμμή στο μια τέτοια ταχύτητα, ένα άτομο θα περπατούσε 8 χιλιόμετρα σε 4 ώρες, επομένως, στις οδηγίες ασφαλείας για την εργασία πεδίου υπάρχει ο ακόλουθος κανόνας: εάν χαθούν ορόσημα, πρέπει να μείνετε στη θέση τους, να δημιουργήσετε ένα καταφύγιο και να περιμένετε το τέλος κακοκαιρίας (μπορεί να βγει ήλιος) ή για βοήθεια. Στο δάσος, τα ορόσημα - δέντρα ή θάμνοι - θα σας βοηθήσουν να κινηθείτε σε ευθεία γραμμή και κάθε φορά που χρειάζεται να μένετε σε δύο τέτοια ορόσημα - το ένα μπροστά, το άλλο πίσω. Αλλά, φυσικά, είναι καλύτερο να έχετε μαζί σας μια πυξίδα...
Ilya Leenson
Βιβλιογραφία:
Μάριο Λιότσι. Ιστορία της φυσικής. Μ., Μιρ, 1970
Κέρκερ Μ. Brownian Movements and Molecular Reality Πριν από το 1900. Journal of Chemical Education, 1974, τομ. 51, Νο. 12
Leenson I.A. Χημικές αντιδράσεις
. M., Astrel, 2002
Ο Σκωτσέζος βοτανολόγος Ρόμπερτ Μπράουν (μερικές φορές το επώνυμό του μεταγράφεται ως Μπράουν) κατά τη διάρκεια της ζωής του, ως ο καλύτερος ειδικός στα φυτά, έλαβε τον τίτλο «Πρίγκιπας των Βοτανολόγων». Έκανε πολλές υπέροχες ανακαλύψεις. Το 1805, μετά από μια τετραετή αποστολή στην Αυστραλία, έφερε στην Αγγλία περίπου 4.000 είδη αυστραλιανών φυτών άγνωστα στους επιστήμονες και πέρασε πολλά χρόνια μελετώντας τα. Περιγράφονται φυτά που έφεραν από την Ινδονησία και την Κεντρική Αφρική. Σπούδασε φυσιολογία φυτών και για πρώτη φορά περιέγραψε λεπτομερώς τον πυρήνα ενός φυτικού κυττάρου. Η Ακαδημία Επιστημών της Αγίας Πετρούπολης τον έκανε επίτιμο μέλος. Αλλά το όνομα του επιστήμονα είναι πλέον ευρέως γνωστό όχι λόγω αυτών των εργασιών.
Το 1827 ο Μπράουν διεξήγαγε έρευνα για τη γύρη των φυτών. Ενδιαφερόταν ιδιαίτερα για το πώς η γύρη συμμετέχει στη διαδικασία της γονιμοποίησης. Κάποτε κοίταξε κάτω από ένα μικροσκόπιο κύτταρα γύρης από φυτό της Βόρειας Αμερικής. Clarkia pulchella(όμορφα clarkia) επιμήκεις κυτταροπλασματικοί κόκκοι αιωρούμενοι στο νερό. Ξαφνικά ο Μπράουν είδε ότι οι μικρότεροι στερεοί κόκκοι, που μετά βίας φαινόταν σε μια σταγόνα νερού, έτρεμαν συνεχώς και κινούνταν από μέρος σε μέρος. Διαπίστωσε ότι αυτές οι κινήσεις, σύμφωνα με τα λόγια του, «δεν συνδέονται ούτε με ροές στο υγρό ούτε με τη σταδιακή εξάτμισή του, αλλά είναι εγγενείς στα ίδια τα σωματίδια».
Η παρατήρηση του Μπράουν επιβεβαιώθηκε από άλλους επιστήμονες. Τα μικρότερα σωματίδια συμπεριφέρονταν σαν να ήταν ζωντανά και ο «χορός» των σωματιδίων επιταχύνθηκε με την αύξηση της θερμοκρασίας και τη μείωση του μεγέθους των σωματιδίων και σαφώς επιβραδύνθηκε όταν αντικαθιστούσε το νερό με ένα πιο παχύρρευστο μέσο. Αυτό το εκπληκτικό φαινόμενο δεν σταμάτησε ποτέ: μπορούσε να παρατηρηθεί για όσο χρονικό διάστημα επιθυμείτε. Στην αρχή, ο Μπράουν πίστευε ακόμη ότι τα ζωντανά όντα έπεσαν στο πεδίο του μικροσκοπίου, ειδικά επειδή η γύρη είναι τα αρσενικά αναπαραγωγικά κύτταρα των φυτών, αλλά υπήρχαν και σωματίδια από νεκρά φυτά, ακόμη και από αυτά που είχαν αποξηρανθεί εκατό χρόνια νωρίτερα σε φυτά. Τότε ο Μπράουν σκέφτηκε αν αυτά ήταν «στοιχειώδη μόρια ζωντανών όντων», για τα οποία μίλησε ο διάσημος Γάλλος φυσιοδίφης Ζορζ Μπουφόν (1707–1788), συγγραφέας ενός βιβλίου 36 τόμων. Φυσική ιστορία. Αυτή η υπόθεση χάθηκε όταν ο Μπράουν άρχισε να εξετάζει προφανώς άψυχα αντικείμενα. Στην αρχή ήταν πολύ μικρά σωματίδια άνθρακα, καθώς και αιθάλη και σκόνη από τον αέρα του Λονδίνου, στη συνέχεια λεπτοαλεσμένες ανόργανες ουσίες: γυαλί, πολλά διαφορετικά ορυκτά. «Ενεργά μόρια» υπήρχαν παντού: «Σε κάθε ορυκτό», έγραψε ο Μπράουν, «το οποίο κατάφερα να κονιοποιήσω σε τέτοιο βαθμό ώστε να μπορεί να αιωρηθεί στο νερό για κάποιο χρονικό διάστημα, βρήκα, σε μεγαλύτερες ή μικρότερες ποσότητες, αυτά τα μόρια ."
Πρέπει να πούμε ότι ο Μπράουν δεν διέθετε κανένα από τα πιο πρόσφατα μικροσκόπια. Στο άρθρο του τονίζει συγκεκριμένα ότι είχε συνηθισμένους αμφίκυρτους φακούς, τους οποίους χρησιμοποιούσε για αρκετά χρόνια. Και συνεχίζει λέγοντας: «Σε όλη τη διάρκεια της μελέτης συνέχισα να χρησιμοποιώ τους ίδιους φακούς με τους οποίους ξεκίνησα τη δουλειά, προκειμένου να δώσω μεγαλύτερη αξιοπιστία στις δηλώσεις μου και να τις κάνω όσο το δυνατόν πιο προσιτές στις συνηθισμένες παρατηρήσεις».
Τώρα, για να επαναλάβουμε την παρατήρηση του Μπράουν, αρκεί να έχουμε ένα όχι πολύ δυνατό μικροσκόπιο και να το χρησιμοποιήσουμε για να εξετάσουμε τον καπνό σε ένα μαυρισμένο κουτί, που φωτίζεται μέσα από μια πλευρική οπή με μια δέσμη έντονου φωτός. Σε ένα αέριο, το φαινόμενο εκδηλώνεται πολύ πιο καθαρά από ό,τι σε ένα υγρό: μικρά κομμάτια στάχτης ή αιθάλης (ανάλογα με την πηγή του καπνού) είναι ορατά, διασκορπίζουν το φως και πηδούν συνεχώς μπρος-πίσω.
Όπως συμβαίνει συχνά στην επιστήμη, πολλά χρόνια αργότερα οι ιστορικοί ανακάλυψαν ότι το 1670, ο εφευρέτης του μικροσκοπίου, ο Ολλανδός Antonie Leeuwenhoek, παρατήρησε προφανώς ένα παρόμοιο φαινόμενο, αλλά τη σπανιότητα και την ατέλεια των μικροσκοπίων, την εμβρυϊκή κατάσταση της μοριακής επιστήμης εκείνη την εποχή δεν τράβηξε την προσοχή στην παρατήρηση του Leeuwenhoek, επομένως η ανακάλυψη αποδίδεται δικαίως στον Brown, ο οποίος ήταν ο πρώτος που τη μελέτησε και την περιέγραψε λεπτομερώς.
Κίνηση Brown και ατομική-μοριακή θεωρία.
Το φαινόμενο που παρατήρησε ο Μπράουν έγινε γρήγορα ευρέως γνωστό. Ο ίδιος έδειξε τα πειράματά του σε πολλούς συναδέλφους (ο Μπράουν απαριθμεί δύο δωδεκάδες ονόματα). Αλλά ούτε ο ίδιος ο Μπράουν ούτε πολλοί άλλοι επιστήμονες για πολλά χρόνια μπορούσαν να εξηγήσουν αυτό το μυστηριώδες φαινόμενο, το οποίο ονομάστηκε «κίνημα Μπράουν». Οι κινήσεις των σωματιδίων ήταν εντελώς τυχαίες: σκίτσα των θέσεων τους που έγιναν σε διαφορετικά χρονικά σημεία (για παράδειγμα, κάθε λεπτό) δεν επέτρεψαν με την πρώτη ματιά να βρεθεί οποιοδήποτε σχέδιο σε αυτές τις κινήσεις.
Μια εξήγηση της κίνησης Brown (όπως ονομάστηκε αυτό το φαινόμενο) από την κίνηση των αόρατων μορίων δόθηκε μόνο στο τελευταίο τέταρτο του 19ου αιώνα, αλλά δεν έγινε αμέσως αποδεκτή από όλους τους επιστήμονες. Το 1863, ένας δάσκαλος της περιγραφικής γεωμετρίας από την Καρλσρούη (Γερμανία), ο Ludwig Christian Wiener (1826–1896), πρότεινε ότι το φαινόμενο συνδέθηκε με τις ταλαντωτικές κινήσεις αόρατων ατόμων. Αυτή ήταν η πρώτη, αν και πολύ μακριά από τη σύγχρονη, εξήγηση της κίνησης Brown από τις ιδιότητες των ίδιων των ατόμων και των μορίων. Είναι σημαντικό ότι ο Wiener είδε την ευκαιρία να χρησιμοποιήσει αυτό το φαινόμενο για να διεισδύσει στα μυστικά της δομής της ύλης. Ήταν ο πρώτος που προσπάθησε να μετρήσει την ταχύτητα κίνησης των σωματιδίων Brown και την εξάρτησή της από το μέγεθός τους. Είναι περίεργο ότι το 1921 Εκθέσεις της Εθνικής Ακαδημίας Επιστημών των ΗΠΑΔημοσιεύτηκε ένα έργο σχετικά με την κίνηση Brown ενός άλλου Wiener - του Norbert, του διάσημου ιδρυτή της κυβερνητικής.
Οι ιδέες του L.K. Wiener έγιναν αποδεκτές και αναπτύχθηκαν από πολλούς επιστήμονες - Sigmund Exner στην Αυστρία (και 33 χρόνια αργότερα - ο γιος του Felix), Giovanni Cantoni στην Ιταλία, Karl Wilhelm Negeli στη Γερμανία, Louis Georges Gouy στη Γαλλία, τρεις Βέλγοι ιερείς - Ιησουίτες Carbonelli, Delso και Tirion και άλλοι. Μεταξύ αυτών των επιστημόνων ήταν και ο μετέπειτα διάσημος Άγγλος φυσικός και χημικός William Ramsay. Σταδιακά έγινε σαφές ότι οι μικρότεροι κόκκοι ύλης χτυπιούνταν από όλες τις πλευρές από ακόμη μικρότερα σωματίδια, τα οποία δεν ήταν πλέον ορατά με μικροσκόπιο - όπως τα κύματα που λικνίζουν ένα μακρινό σκάφος δεν είναι ορατά από την ακτή, ενώ οι κινήσεις του σκάφους είναι ορατά αρκετά καθαρά. Όπως έγραψαν σε ένα από τα άρθρα το 1877, «...ο νόμος των μεγάλων αριθμών δεν μειώνει πλέον την επίδραση των συγκρούσεων στη μέση ομοιόμορφη πίεση· το αποτέλεσμά τους δεν θα είναι πλέον ίσο με μηδέν, αλλά θα αλλάζει συνεχώς την κατεύθυνση και μέγεθος."
Ποιοτικά, η εικόνα ήταν αρκετά εύλογη και ακόμη και οπτική. Ένα μικρό κλαδάκι ή ένα ζωύφιο πρέπει να κινείται με τον ίδιο περίπου τρόπο, να σπρώχνεται (ή να τραβιέται) σε διαφορετικές κατευθύνσεις από πολλά μυρμήγκια. Αυτά τα μικρότερα σωματίδια ήταν στην πραγματικότητα στο λεξιλόγιο των επιστημόνων, αλλά κανείς δεν τα είχε δει ποτέ. Ονομάζονταν μόρια. Μετάφραση από τα λατινικά, αυτή η λέξη σημαίνει «μικρή μάζα». Παραδόξως, αυτή ακριβώς είναι η εξήγηση που δίνει σε ένα παρόμοιο φαινόμενο ο Ρωμαίος φιλόσοφος Titus Lucretius Carus (περίπου 99–55 π.Χ.) στο διάσημο ποίημά του Σχετικά με τη φύση των πραγμάτων. Σε αυτό, αποκαλεί τα μικρότερα σωματίδια αόρατα στο μάτι «πρωταρχικές αρχές» των πραγμάτων.
Οι αρχές των πραγμάτων κινούνται πρώτα μόνες τους,
Ακολουθούν σώματα από τον μικρότερο συνδυασμό τους,
Κοντά, σαν να λέγαμε, σε ισχύ στις πρωταρχικές αρχές,
Κρυμμένοι από αυτούς, δεχόμενοι σοκ, αρχίζουν να αγωνίζονται,
Οι ίδιοι να κινούνται, ενθαρρύνοντας στη συνέχεια μεγαλύτερα σώματα.
Ξεκινώντας λοιπόν από την αρχή η κίνηση σιγά σιγά
Αγγίζει τα συναισθήματά μας και γίνεται επίσης ορατό
Σε εμάς και στους κόκκους της σκόνης που κινούνται στο φως του ήλιου,
Αν και οι δονήσεις από τις οποίες εμφανίζεται είναι ανεπαίσθητες...
Στη συνέχεια, αποδείχθηκε ότι ο Λουκρήτιος έκανε λάθος: είναι αδύνατο να παρατηρήσει κανείς την κίνηση του Brown με γυμνό μάτι και τα σωματίδια σκόνης σε μια ηλιαχτίδα που εισχώρησε σε ένα σκοτεινό δωμάτιο «χορεύουν» λόγω των κινήσεων στροβιλισμού του αέρα. Αλλά εξωτερικά και τα δύο φαινόμενα έχουν κάποιες ομοιότητες. Και μόνο τον 19ο αιώνα. Έγινε προφανές σε πολλούς επιστήμονες ότι η κίνηση των σωματιδίων Brown προκαλείται από τυχαίες κρούσεις των μορίων του μέσου. Τα κινούμενα μόρια συγκρούονται με σωματίδια σκόνης και άλλα στερεά σωματίδια που βρίσκονται στο νερό. Όσο υψηλότερη είναι η θερμοκρασία, τόσο πιο γρήγορη είναι η κίνηση. Εάν ένα κομμάτι σκόνης είναι μεγάλο, για παράδειγμα, έχει μέγεθος 0,1 mm (η διάμετρος είναι ένα εκατομμύριο φορές μεγαλύτερη από αυτή ενός μορίου νερού), τότε πολλές ταυτόχρονες κρούσεις σε αυτό από όλες τις πλευρές είναι αμοιβαία ισορροπημένες και πρακτικά δεν το κάνει. «Νιώσε» τα - περίπου το ίδιο με ένα κομμάτι ξύλου στο μέγεθος ενός πιάτου δεν θα «νιώσει» τις προσπάθειες πολλών μυρμηγκιών που θα το τραβήξουν ή θα το σπρώξουν σε διαφορετικές κατευθύνσεις. Εάν το σωματίδιο της σκόνης είναι σχετικά μικρό, θα κινηθεί προς τη μία ή την άλλη κατεύθυνση υπό την επίδραση κρούσεων από τα γύρω μόρια.
Τα σωματίδια Brownian έχουν μέγεθος της τάξης των 0,1–1 μm, δηλ. από το ένα χιλιοστό έως το ένα δέκατο χιλιοστό του χιλιοστού, γι' αυτό ο Μπράουν μπόρεσε να διακρίνει την κίνησή τους επειδή κοίταζε μικροσκοπικούς κυτταροπλασματικούς κόκκους και όχι την ίδια τη γύρη (για την οποία συχνά γράφεται λανθασμένα). Το πρόβλημα είναι ότι τα κύτταρα γύρης είναι πολύ μεγάλα. Έτσι, στη γύρη του λιβαδιού, που μεταφέρεται από τον άνεμο και προκαλεί αλλεργικές ασθένειες στον άνθρωπο (πυρετός εκ χόρτου), το μέγεθος των κυττάρων είναι συνήθως της τάξης των 20 - 50 microns, δηλ. είναι πολύ μεγάλα για να παρατηρήσουν την κίνηση Brown. Είναι επίσης σημαντικό να σημειωθεί ότι μεμονωμένες κινήσεις ενός σωματιδίου Brown συμβαίνουν πολύ συχνά και σε πολύ μικρές αποστάσεις, έτσι ώστε να είναι αδύνατο να τις δούμε, αλλά κάτω από ένα μικροσκόπιο, κινήσεις που έχουν συμβεί σε μια συγκεκριμένη χρονική περίοδο είναι ορατές.
Φαίνεται ότι το ίδιο το γεγονός της ύπαρξης της κίνησης Brown απέδειξε ξεκάθαρα τη μοριακή δομή της ύλης, αλλά ακόμη και στις αρχές του 20ου αιώνα. Υπήρχαν επιστήμονες, συμπεριλαμβανομένων φυσικών και χημικών, που δεν πίστευαν στην ύπαρξη μορίων. Η ατομική-μοριακή θεωρία μόνο αργά και με δυσκολία κέρδισε την αναγνώριση. Έτσι, ο κορυφαίος Γάλλος οργανικός χημικός Marcelin Berthelot (1827–1907) έγραψε: «Η έννοια ενός μορίου, από τη σκοπιά της γνώσης μας, είναι αβέβαιη, ενώ μια άλλη έννοια - ένα άτομο - είναι καθαρά υποθετική». Ο διάσημος Γάλλος χημικός A. Saint-Clair Deville (1818–1881) μίλησε ακόμη πιο ξεκάθαρα: «Δεν αποδέχομαι το νόμο του Avogadro, ούτε το άτομο, ούτε το μόριο, γιατί αρνούμαι να πιστέψω σε αυτό που ούτε μπορώ να δω ούτε να παρατηρήσω. ” Και ο Γερμανός φυσικοχημικός Wilhelm Ostwald (1853–1932), βραβευμένος με Νόμπελ, ένας από τους ιδρυτές της φυσικής χημείας, στις αρχές του 20ού αιώνα. αρνήθηκε κατηγορηματικά την ύπαρξη ατόμων. Κατάφερε να γράψει ένα τρίτομο εγχειρίδιο χημείας στο οποίο η λέξη «άτομο» δεν αναφέρεται ποτέ καν. Μιλώντας στις 19 Απριλίου 1904, με μια μεγάλη έκθεση στο Βασιλικό Ίδρυμα στα μέλη της Αγγλικής Χημικής Εταιρείας, ο Ostwald προσπάθησε να αποδείξει ότι τα άτομα δεν υπάρχουν και «αυτό που ονομάζουμε ύλη είναι μόνο μια συλλογή ενεργειών που συλλέγονται μαζί σε ένα δεδομένο θέση."
Αλλά ακόμη και εκείνοι οι φυσικοί που αποδέχονταν τη μοριακή θεωρία δεν μπορούσαν να πιστέψουν ότι η εγκυρότητα της ατομικής-μοριακής θεωρίας αποδείχθηκε με τόσο απλό τρόπο, έτσι προβλήθηκαν ποικίλοι εναλλακτικοί λόγοι για να εξηγηθεί το φαινόμενο. Και αυτό είναι απολύτως σύμφωνα με το πνεύμα της επιστήμης: μέχρι να εντοπιστεί με σαφήνεια η αιτία ενός φαινομένου, είναι δυνατό (και ακόμη και απαραίτητο) να υποθέσουμε διάφορες υποθέσεις, οι οποίες θα πρέπει, αν είναι δυνατόν, να ελεγχθούν πειραματικά ή θεωρητικά. Έτσι, το 1905, ένα σύντομο άρθρο του καθηγητή φυσικής της Αγίας Πετρούπολης N.A. Gezehus, δασκάλου του διάσημου ακαδημαϊκού A.F. Ioffe, δημοσιεύτηκε στο Εγκυκλοπαιδικό Λεξικό Brockhaus and Efron. Ο Gesehus έγραψε ότι, σύμφωνα με ορισμένους επιστήμονες, η κίνηση Brown προκαλείται από «ακτίνες φωτός ή θερμότητας που περνούν μέσα από ένα υγρό» και καταλήγει σε «απλές ροές μέσα σε ένα υγρό που δεν έχουν καμία σχέση με τις κινήσεις των μορίων» και αυτές οι ροές μπορεί να προκληθεί από «εξάτμιση, διάχυση και άλλους λόγους». Άλλωστε, ήταν ήδη γνωστό ότι μια πολύ παρόμοια κίνηση σωματιδίων σκόνης στον αέρα προκαλείται ακριβώς από ροές δίνης. Αλλά η εξήγηση που έδωσε ο Gesehus θα μπορούσε εύκολα να διαψευσθεί πειραματικά: αν κοιτάξετε δύο σωματίδια Brownian που βρίσκονται πολύ κοντά το ένα στο άλλο μέσω ενός ισχυρού μικροσκοπίου, οι κινήσεις τους θα αποδειχθούν εντελώς ανεξάρτητες. Εάν αυτές οι κινήσεις προκλήθηκαν από οποιεσδήποτε ροές στο υγρό, τότε τέτοια γειτονικά σωματίδια θα κινούνταν συντονισμένα.
Θεωρία της κίνησης Brown.
Στις αρχές του 20ου αιώνα. Οι περισσότεροι επιστήμονες κατανόησαν τη μοριακή φύση της κίνησης Brown. Αλλά όλες οι εξηγήσεις παρέμειναν καθαρά ποιοτικές· καμία ποσοτική θεωρία δεν μπορούσε να αντέξει πειραματικές δοκιμές. Επιπλέον, τα ίδια τα πειραματικά αποτελέσματα ήταν ασαφή: το φανταστικό θέαμα των ασταμάτητα ορμητικών σωματιδίων υπνώτισε τους πειραματιστές και δεν γνώριζαν ακριβώς ποια χαρακτηριστικά του φαινομένου έπρεπε να μετρηθούν.
Παρά τη φαινομενική πλήρη διαταραχή, ήταν ακόμα δυνατό να περιγραφούν οι τυχαίες κινήσεις των σωματιδίων Brown με μια μαθηματική σχέση. Για πρώτη φορά, μια αυστηρή εξήγηση της κίνησης Brown δόθηκε το 1904 από τον Πολωνό φυσικό Marian Smoluchowski (1872–1917), ο οποίος εκείνα τα χρόνια εργαζόταν στο Πανεπιστήμιο του Lviv. Ταυτόχρονα, η θεωρία αυτού του φαινομένου αναπτύχθηκε από τον Albert Einstein (1879–1955), έναν ελάχιστα γνωστό τότε εμπειρογνώμονα 2ης κατηγορίας στο Γραφείο Διπλωμάτων Ευρεσιτεχνίας της ελβετικής πόλης της Βέρνης. Το άρθρο του, που δημοσιεύτηκε τον Μάιο του 1905 στο γερμανικό περιοδικό Annalen der Physik, είχε τον τίτλο Σχετικά με την κίνηση των σωματιδίων που αιωρούνται σε ένα ρευστό σε ηρεμία, που απαιτείται από τη μοριακή κινητική θεωρία της θερμότητας. Με αυτό το όνομα, ο Αϊνστάιν ήθελε να δείξει ότι η μοριακή κινητική θεωρία της δομής της ύλης υπονοεί απαραίτητα την ύπαρξη τυχαίας κίνησης των μικρότερων στερεών σωματιδίων στα υγρά.
Είναι περίεργο ότι στην αρχή αυτού του άρθρου, ο Αϊνστάιν γράφει ότι είναι εξοικειωμένος με το ίδιο το φαινόμενο, αν και επιφανειακά: «Είναι πιθανό οι εν λόγω κινήσεις να είναι ταυτόσημες με τη λεγόμενη μοριακή κίνηση Brown, αλλά τα διαθέσιμα δεδομένα Για μένα σχετικά με τα τελευταία είναι τόσο ανακριβή που δεν μπορούσα να διατυπώσω μια συγκεκριμένη άποψη». Και δεκαετίες αργότερα, ήδη στα τέλη της ζωής του, ο Αϊνστάιν έγραψε κάτι διαφορετικό στα απομνημονεύματά του - ότι δεν ήξερε καθόλου για την κίνηση Brown και στην πραγματικότητα την «ανακάλυψε ξανά» καθαρά θεωρητικά: «Μη γνωρίζοντας ότι οι παρατηρήσεις της «κίνησης Brown» ήταν από καιρό γνωστό, ανακάλυψα ότι η ατομική θεωρία οδηγεί στην ύπαρξη παρατηρήσιμης κίνησης μικροσκοπικών αιωρούμενων σωματιδίων." Όπως και να έχει, το θεωρητικό άρθρο του Αϊνστάιν τελείωσε με μια άμεση κλήση στους πειραματιστές να δοκιμάσουν τα συμπεράσματά του πειραματικά: "Αν κάποιος ερευνητής μπορούσε σύντομα να απαντήσει τα ερωτήματα που τίθενται εδώ ρωτούν!" – τελειώνει το άρθρο του με ένα τόσο ασυνήθιστο επιφώνημα.
Η απάντηση στην παθιασμένη έκκληση του Αϊνστάιν δεν άργησε να έρθει.
Σύμφωνα με τη θεωρία Smoluchowski-Einstein, η μέση τιμή της τετραγωνικής μετατόπισης ενός σωματιδίου Brown ( μικρό 2) για το χρόνο tευθέως ανάλογη της θερμοκρασίας Τκαι αντιστρόφως ανάλογο με το ιξώδες του υγρού h, μέγεθος σωματιδίων rκαι η σταθερά του Avogadro
ΝΕΝΑ: μικρό 2 = 2RTt/6ph rNΕΝΑ,
Οπου R– σταθερά αερίου. Έτσι, εάν σε 1 λεπτό ένα σωματίδιο με διάμετρο 1 μm κινείται κατά 10 μm, τότε σε 9 λεπτά - κατά 10 = 30 μm, σε 25 λεπτά - κατά 10 = 50 μm, κ.λπ. Κάτω από παρόμοιες συνθήκες, ένα σωματίδιο με διάμετρο 0,25 μm για τις ίδιες χρονικές περιόδους (1, 9 και 25 λεπτά) θα κινηθεί κατά 20, 60 και 100 μm, αντίστοιχα, αφού = 2. Είναι σημαντικό ο παραπάνω τύπος να περιλαμβάνει Η σταθερά του Avogadro, η οποία επομένως, μπορεί να προσδιοριστεί με ποσοτικές μετρήσεις της κίνησης ενός σωματιδίου Brown, που έγινε από τον Γάλλο φυσικό Jean Baptiste Perrin (1870–1942).
Το 1908, ο Perrin άρχισε ποσοτικές παρατηρήσεις της κίνησης των σωματιδίων Brown στο μικροσκόπιο. Χρησιμοποίησε ένα υπερμικροσκόπιο, που εφευρέθηκε το 1902, το οποίο επέτρεψε την ανίχνευση των μικρότερων σωματιδίων διαχέοντας φως πάνω τους από έναν ισχυρό πλευρικό φωτιστή. Ο Perrin έλαβε μικροσκοπικές μπάλες σχεδόν σφαιρικού σχήματος και περίπου ίδιου μεγέθους από κόμμι, τον συμπυκνωμένο χυμό ορισμένων τροπικών δέντρων (χρησιμοποιείται επίσης ως κίτρινη ακουαρέλα). Αυτά τα μικροσκοπικά σφαιρίδια εναιωρήθηκαν σε γλυκερίνη που περιείχε 12% νερό. το παχύρρευστο υγρό εμπόδιζε την εμφάνιση εσωτερικών ροών σε αυτό που θα θόλωναν την εικόνα. Οπλισμένος με ένα χρονόμετρο, ο Perrin σημείωσε και στη συνέχεια σκιαγράφησε (φυσικά, σε πολύ μεγεθυμένη κλίμακα) σε ένα γραφικό φύλλο χαρτιού τη θέση των σωματιδίων σε τακτά χρονικά διαστήματα, για παράδειγμα, κάθε μισό λεπτό. Συνδέοντας τα σημεία που προέκυψαν με ευθείες γραμμές, απέκτησε περίπλοκες τροχιές, μερικές από αυτές φαίνονται στο σχήμα (προέρχονται από το βιβλίο του Perrin Άτομα, που εκδόθηκε το 1920 στο Παρίσι). Μια τέτοια χαοτική, άτακτη κίνηση των σωματιδίων οδηγεί στο γεγονός ότι κινούνται στο χώρο αρκετά αργά: το άθροισμα των τμημάτων είναι πολύ μεγαλύτερο από τη μετατόπιση του σωματιδίου από το πρώτο σημείο στο τελευταίο.

Διαδοχικές θέσεις κάθε 30 δευτερόλεπτα τριών σωματιδίων Brownian - μπάλες τσίχλας με μέγεθος περίπου 1 micron. Ένα κελί αντιστοιχεί σε απόσταση 3 μm. Εάν ο Perrin μπορούσε να καθορίσει τη θέση των σωματιδίων Brownian όχι μετά από 30, αλλά μετά από 3 δευτερόλεπτα, τότε οι ευθείες γραμμές μεταξύ κάθε γειτονικού σημείου θα μετατρέπονταν στην ίδια πολύπλοκη διακεκομμένη γραμμή ζιγκ-ζαγκ, μόνο σε μικρότερη κλίμακα.
Χρησιμοποιώντας τον θεωρητικό τύπο και τα αποτελέσματά του, ο Perrin έλαβε μια τιμή για τον αριθμό του Avogadro που ήταν αρκετά ακριβής για εκείνη την εποχή: 6,8 . 10 23 . Ο Perrin χρησιμοποίησε επίσης ένα μικροσκόπιο για να μελετήσει την κατακόρυφη κατανομή των σωματιδίων Brown ( εκ. ΝΟΜΟΣ ΤΟΥ AVOGADRO) και έδειξε ότι, παρά τη δράση της βαρύτητας, παραμένουν αιωρούμενα σε διάλυμα. Ο Perrin έχει και άλλα σημαντικά έργα. Το 1895, απέδειξε ότι οι καθοδικές ακτίνες είναι αρνητικά ηλεκτρικά φορτία (ηλεκτρόνια) και το 1901 πρότεινε για πρώτη φορά ένα πλανητικό μοντέλο του ατόμου. Το 1926 τιμήθηκε με το Νόμπελ Φυσικής.
Τα αποτελέσματα που έλαβε ο Perrin επιβεβαίωσαν τα θεωρητικά συμπεράσματα του Αϊνστάιν. Έκανε έντονη εντύπωση. Όπως έγραψε ο Αμερικανός φυσικός A. Pais πολλά χρόνια αργότερα, «δεν παύεις ποτέ να εκπλήσσεσαι με αυτό το αποτέλεσμα, που προκύπτει με έναν τόσο απλό τρόπο: αρκεί να ετοιμάσεις ένα εναιώρημα από μπάλες, το μέγεθος των οποίων είναι μεγάλο σε σύγκριση με το μέγεθος. από απλά μόρια, πάρτε ένα χρονόμετρο και ένα μικροσκόπιο και μπορείτε να προσδιορίσετε τη σταθερά του Avogadro!». Θα μπορούσε επίσης να εκπλαγεί κανείς: περιγραφές νέων πειραμάτων για την κίνηση Brown εξακολουθούν να εμφανίζονται σε επιστημονικά περιοδικά (Nature, Science, Journal of Chemical Education) κατά καιρούς! Μετά τη δημοσίευση των αποτελεσμάτων του Perrin, ο Ostwald, πρώην αντίπαλος του ατομισμού, παραδέχτηκε ότι «η σύμπτωση της κίνησης Brown με τις απαιτήσεις της κινητικής υπόθεσης... δίνει τώρα στον πιο προσεκτικό επιστήμονα το δικαίωμα να μιλήσει για πειραματική απόδειξη της ατομικής θεωρίας της ύλης. Έτσι, η ατομική θεωρία έχει ανυψωθεί στην τάξη μιας επιστημονικής, καλά θεμελιωμένης θεωρίας». Τον απηχεί ο Γάλλος μαθηματικός και φυσικός Ανρί Πουανκαρέ: «Ο λαμπρός προσδιορισμός του αριθμού των ατόμων από τον Περέν ολοκλήρωσε τον θρίαμβο του ατομισμού... Το άτομο των χημικών έχει πλέον γίνει πραγματικότητα».
Brownian κίνηση και διάχυση.
Η κίνηση των σωματιδίων Brown μοιάζει πολύ στην εμφάνιση με την κίνηση μεμονωμένων μορίων ως αποτέλεσμα της θερμικής τους κίνησης. Αυτή η κίνηση ονομάζεται διάχυση. Ακόμη και πριν από το έργο του Smoluchowski και του Einstein, οι νόμοι της μοριακής κίνησης καθιερώθηκαν στην απλούστερη περίπτωση της αέριας κατάστασης της ύλης. Αποδείχθηκε ότι τα μόρια στα αέρια κινούνται πολύ γρήγορα - με την ταχύτητα μιας σφαίρας, αλλά δεν μπορούν να πετάξουν μακριά, καθώς πολύ συχνά συγκρούονται με άλλα μόρια. Για παράδειγμα, τα μόρια οξυγόνου και αζώτου στον αέρα, που κινούνται με μέση ταχύτητα περίπου 500 m/s, αντιμετωπίζουν περισσότερες από ένα δισεκατομμύριο συγκρούσεις κάθε δευτερόλεπτο. Επομένως, η διαδρομή του μορίου, αν μπορούσε να ακολουθηθεί, θα ήταν μια πολύπλοκη διακεκομμένη γραμμή. Τα σωματίδια Brown περιγράφουν επίσης μια παρόμοια τροχιά εάν η θέση τους καταγράφεται σε συγκεκριμένα χρονικά διαστήματα. Τόσο η διάχυση όσο και η κίνηση Brown είναι συνέπεια της χαοτικής θερμικής κίνησης των μορίων και επομένως περιγράφονται από παρόμοιες μαθηματικές σχέσεις. Η διαφορά είναι ότι τα μόρια στα αέρια κινούνται σε ευθεία γραμμή μέχρι να συγκρουστούν με άλλα μόρια, μετά από την οποία αλλάζουν κατεύθυνση. Ένα σωματίδιο Brown, σε αντίθεση με ένα μόριο, δεν εκτελεί «ελεύθερες πτήσεις», αλλά βιώνει πολύ συχνά μικρές και ακανόνιστες «τρεμούλες», με αποτέλεσμα να μετατοπίζεται χαοτικά προς τη μία ή την άλλη κατεύθυνση. Οι υπολογισμοί έχουν δείξει ότι για ένα σωματίδιο μεγέθους 0,1 μm, μια κίνηση συμβαίνει σε τρία δισεκατομμυριοστά του δευτερολέπτου σε απόσταση μόνο 0,5 nm (1 nm = 0,001 μm). Όπως εύστοχα το θέτει ένας συγγραφέας, αυτό θυμίζει τη μετακίνηση ενός άδειου κουτιού μπύρας σε μια πλατεία όπου έχει συγκεντρωθεί πλήθος κόσμου.
Η διάχυση είναι πολύ πιο εύκολο να παρατηρηθεί από την κίνηση Brown, καθώς δεν απαιτεί μικροσκόπιο: οι κινήσεις δεν παρατηρούνται μεμονωμένων σωματιδίων, αλλά των τεράστιων μαζών τους, απλά πρέπει να διασφαλίσετε ότι η διάχυση δεν υπερτίθεται από τη μεταφορά - ανάμειξη της ύλης ως αποτέλεσμα των ροών στροβιλισμού (τέτοιες ροές είναι εύκολο να παρατηρηθούν, τοποθετώντας μια σταγόνα έγχρωμου διαλύματος, όπως μελάνι, σε ένα ποτήρι ζεστό νερό).
Η διάχυση είναι βολικό να παρατηρείται σε παχιά πηκτώματα. Ένα τέτοιο τζελ μπορεί να παρασκευαστεί, για παράδειγμα, σε ένα βάζο πενικιλίνης παρασκευάζοντας ένα διάλυμα ζελατίνης 4-5% σε αυτό. Η ζελατίνη πρέπει πρώτα να φουσκώσει για αρκετές ώρες και στη συνέχεια διαλύεται πλήρως με ανάδευση κατεβάζοντας το βάζο σε ζεστό νερό. Μετά την ψύξη, λαμβάνεται ένα μη ρέον πήκτωμα με τη μορφή μιας διαφανούς, ελαφρώς θολής μάζας. Εάν, χρησιμοποιώντας αιχμηρά τσιμπιδάκια, εισάγετε προσεκτικά έναν μικρό κρύσταλλο υπερμαγγανικού καλίου («υπερμαγγανικό κάλιο») στο κέντρο αυτής της μάζας, ο κρύσταλλος θα παραμείνει κρεμασμένος στο σημείο που έμεινε, καθώς το τζελ εμποδίζει την πτώση του. Μέσα σε λίγα λεπτά, μια βιολετί σφαίρα θα αρχίσει να μεγαλώνει γύρω από τον κρύσταλλο· με την πάροδο του χρόνου, γίνεται όλο και μεγαλύτερη έως ότου τα τοιχώματα του βάζου παραμορφώσουν το σχήμα του. Το ίδιο αποτέλεσμα μπορεί να επιτευχθεί χρησιμοποιώντας έναν κρύσταλλο θειικού χαλκού, μόνο σε αυτή την περίπτωση η μπάλα δεν θα αποδειχθεί μοβ, αλλά μπλε.
Είναι ξεκάθαρο γιατί βγήκε η μπάλα: Τα ιόντα MnO 4 - σχηματίζονται όταν διαλύεται ο κρύσταλλος, μπαίνουν σε διάλυμα (το πήκτωμα είναι κυρίως νερό) και, ως αποτέλεσμα της διάχυσης, κινούνται ομοιόμορφα προς όλες τις κατευθύνσεις, ενώ η βαρύτητα δεν έχει ουσιαστικά καμία επίδραση στο ρυθμός διάχυσης. Η διάχυση στο υγρό είναι πολύ αργή: θα χρειαστούν πολλές ώρες για να μεγαλώσει η μπάλα αρκετά εκατοστά. Στα αέρια, η διάχυση είναι πολύ πιο γρήγορη, αλλά παρόλα αυτά, αν ο αέρας δεν αναμειγνυόταν, η μυρωδιά του αρώματος ή της αμμωνίας θα εξαπλωνόταν στο δωμάτιο για ώρες.
Θεωρία κίνησης Brown: τυχαίοι περίπατοι.
Η θεωρία Smoluchowski-Einstein εξηγεί τους νόμους τόσο της διάχυσης όσο και της κίνησης Brown. Μπορούμε να εξετάσουμε αυτά τα μοτίβα χρησιμοποιώντας το παράδειγμα της διάχυσης. Αν η ταχύτητα του μορίου είναι u, τότε, κινούμενος σε ευθεία γραμμή, στο χρόνο tθα πάει την απόσταση μεγάλο = ut, αλλά λόγω συγκρούσεων με άλλα μόρια, το μόριο αυτό δεν κινείται σε ευθεία γραμμή, αλλά αλλάζει συνεχώς την κατεύθυνση της κίνησής του. Εάν ήταν δυνατό να σκιαγραφηθεί η διαδρομή ενός μορίου, δεν θα διέφερε ουσιαστικά από τα σχέδια που έλαβε ο Perrin. Από αυτά τα σχήματα είναι σαφές ότι λόγω της χαοτικής κίνησης το μόριο μετατοπίζεται από μια απόσταση μικρό, σημαντικά λιγότερο από μεγάλο. Αυτές οι ποσότητες σχετίζονται με τη σχέση μικρό= , όπου l είναι η απόσταση που πετάει ένα μόριο από τη μια σύγκρουση στην άλλη, η μέση ελεύθερη διαδρομή. Οι μετρήσεις έχουν δείξει ότι για μόρια αέρα σε κανονική ατμοσφαιρική πίεση l ~ 0,1 μm, που σημαίνει ότι με ταχύτητα 500 m/s ένα μόριο αζώτου ή οξυγόνου θα διανύσει την απόσταση σε 10.000 δευτερόλεπτα (λιγότερο από τρεις ώρες) μεγάλο= 5000 km και θα μετατοπιστεί από την αρχική θέση μόνο μικρό= 0,7 m (70 cm), γι' αυτό οι ουσίες κινούνται τόσο αργά λόγω της διάχυσης, ακόμη και στα αέρια.
Η διαδρομή ενός μορίου ως αποτέλεσμα της διάχυσης (ή η διαδρομή ενός σωματιδίου Brown) ονομάζεται τυχαίος περίπατος. Οι πνευματώδεις φυσικοί επανερμήνευσαν αυτή την έκφραση ως το περπάτημα του μεθυσμένου - «το μονοπάτι ενός μεθυσμένου». Αυτή η αναλογία επιτρέπει επίσης να συμπεράνει κανείς πολύ απλά ότι η βασική εξίσωση μιας τέτοιας διαδικασίας βασίζεται στο παράδειγμα της μονοδιάστατης κίνησης, η οποία είναι εύκολο να γενικευτεί σε τρισδιάστατη.
Ας υποθέσουμε ότι ένας αγενής ναύτης βγήκε από μια ταβέρνα αργά το βράδυ και κατευθύνθηκε στο δρόμο. Έχοντας περπατήσει το μονοπάτι l μέχρι το πλησιέστερο φανάρι, ξεκουράστηκε και πήγε... είτε πιο μακριά, στο διπλανό φανάρι, είτε πίσω, στην ταβέρνα - άλλωστε δεν θυμάται από πού ήρθε. Το ερώτημα είναι, θα αφήσει ποτέ το κολοκυθάκι, ή απλά θα περιπλανηθεί γύρω του, τώρα απομακρυνόμενος, τώρα πλησιάζοντας το; (Μια άλλη εκδοχή του προβλήματος αναφέρει ότι υπάρχουν βρώμικα χαντάκια και στις δύο άκρες του δρόμου, όπου τελειώνουν τα φώτα του δρόμου, και ρωτά αν ο ναύτης θα μπορέσει να αποφύγει να πέσει σε ένα από αυτά.) Διαισθητικά, φαίνεται ότι η δεύτερη απάντηση είναι σωστή. Αλλά είναι λάθος: αποδεικνύεται ότι ο ναύτης σταδιακά θα απομακρύνεται όλο και περισσότερο από το σημείο μηδέν, αν και πολύ πιο αργά από ό,τι αν περπατούσε μόνο προς μία κατεύθυνση. Δείτε πώς να το αποδείξετε.
Έχοντας περάσει την πρώτη φορά στην πλησιέστερη λάμπα (δεξιά ή αριστερά), ο ναύτης θα βρίσκεται σε απόσταση μικρό 1 = ± l από το σημείο εκκίνησης. Επειδή μας ενδιαφέρει μόνο η απόστασή του από αυτό το σημείο, αλλά όχι η κατεύθυνσή του, θα απαλλαγούμε από τα σημάδια τετραγωνίζοντας αυτήν την έκφραση: μικρό 1 2 = l 2. Μετά από λίγο καιρό, ο ναύτης, έχοντας ήδη ολοκληρώσει Ν«περιπλανώμενος», θα είναι σε απόσταση
s N= από την αρχή. Και έχοντας περπατήσει ξανά (προς μία κατεύθυνση) μέχρι το πλησιέστερο φανάρι, σε απόσταση s N+1 = s N± l ή, χρησιμοποιώντας το τετράγωνο της μετατόπισης, μικρό 2 Ν+1 = μικρό 2 Ν± 2 s N l + l 2. Αν ο ναύτης επαναλάβει αυτή την κίνηση πολλές φορές (από Νπριν Ν+ 1), τότε ως αποτέλεσμα του μέσου όρου (περνά με ίση πιθανότητα Ντο βήμα προς τα δεξιά ή προς τα αριστερά), όρος ± 2 s NΘα ακυρώσω, άρα s 2 Ν+1 = s2 Ν+ l 2> (οι γωνιακές αγκύλες υποδεικνύουν τη μέση τιμή) L = 3600 m = 3,6 km, ενώ η μετατόπιση από το σημείο μηδέν για τον ίδιο χρόνο θα είναι ίση μόνο με μικρό= = 190 μ. Σε τρεις ώρες θα περάσει μεγάλο= 10,8 km, και θα μετατοπιστεί κατά μικρό= 330 m, κ.λπ.
Δουλειά uΤο l στον προκύπτον τύπο μπορεί να συγκριθεί με τον συντελεστή διάχυσης, ο οποίος, όπως έδειξε ο Ιρλανδός φυσικός και μαθηματικός George Gabriel Stokes (1819–1903), εξαρτάται από το μέγεθος των σωματιδίων και το ιξώδες του μέσου. Με βάση παρόμοιες εκτιμήσεις, ο Αϊνστάιν εξήγαγε την εξίσωσή του.
Η θεωρία της κίνησης Brown στην πραγματική ζωή.
Η θεωρία των τυχαίων περιπάτων έχει σημαντικές πρακτικές εφαρμογές. Λένε ότι ελλείψει ορόσημων (ο ήλιος, τα αστέρια, ο θόρυβος ενός αυτοκινητόδρομου ή σιδηροδρόμου κ.λπ.), ένα άτομο περιπλανιέται στο δάσος, σε ένα χωράφι σε μια χιονοθύελλα ή σε πυκνή ομίχλη σε κύκλους, επιστρέφοντας πάντα στο δικό του αρχικό μέρος. Στην πραγματικότητα, δεν περπατά σε κύκλους, αλλά περίπου με τον ίδιο τρόπο κινούνται τα μόρια ή τα σωματίδια Brown. Μπορεί να επιστρέψει στην αρχική του θέση, αλλά μόνο τυχαία. Όμως διασχίζει το δρόμο του πολλές φορές. Λένε επίσης ότι άνθρωποι παγωμένοι σε μια χιονοθύελλα βρέθηκαν «κάποια χιλιόμετρα» από την πλησιέστερη κατοικία ή δρόμο, αλλά στην πραγματικότητα το άτομο δεν είχε καμία πιθανότητα να περπατήσει αυτό το χιλιόμετρο, και να γιατί.
Για να υπολογίσετε πόσο θα μετατοπιστεί ένα άτομο ως αποτέλεσμα τυχαίων περιπάτων, πρέπει να γνωρίζετε την τιμή του l, δηλ. την απόσταση που μπορεί να περπατήσει ένα άτομο σε ευθεία γραμμή χωρίς ορόσημα. Αυτή η τιμή μετρήθηκε από τον Διδάκτωρ Γεωλογικών και Ορυκτολογικών Επιστημών B.S. Gorobets με τη βοήθεια εθελοντών φοιτητών. Αυτός, φυσικά, δεν τους άφησε σε ένα πυκνό δάσος ή σε ένα χιονισμένο γήπεδο, όλα ήταν πιο απλά - ο μαθητής τοποθετήθηκε στο κέντρο ενός άδειου σταδίου, με δεμένα μάτια και του ζητήθηκε να περπατήσει μέχρι το τέλος του γηπέδου ποδοσφαίρου στο πλήρης σιωπή (για να αποκλειστεί ο προσανατολισμός από ήχους). Αποδείχθηκε ότι κατά μέσο όρο ο μαθητής περπάτησε σε ευθεία γραμμή μόνο για περίπου 20 μέτρα (η απόκλιση από την ιδανική ευθεία δεν ξεπερνούσε τις 5°) και στη συνέχεια άρχισε να αποκλίνει όλο και περισσότερο από την αρχική κατεύθυνση. Στο τέλος, σταμάτησε, μακριά από το να φτάσει στην άκρη.
Αφήστε τώρα ένα άτομο να περπατήσει (ή μάλλον, να περιπλανηθεί) στο δάσος με ταχύτητα 2 χιλιομέτρων την ώρα (για έναν δρόμο αυτό είναι πολύ αργό, αλλά για ένα πυκνό δάσος είναι πολύ γρήγορο), τότε αν η τιμή του l είναι 20 μέτρα, μετά σε μια ώρα θα διανύσει 2 χλμ., αλλά θα κινηθεί μόνο 200 μ., σε δύο ώρες - περίπου 280 μ., σε τρεις ώρες - 350 μ., σε 4 ώρες - 400 μ. κ.λπ. Και κινούμενος σε ευθεία γραμμή στο μια τέτοια ταχύτητα, ένα άτομο θα περπατούσε 8 χιλιόμετρα σε 4 ώρες, επομένως, στις οδηγίες ασφαλείας για την εργασία πεδίου υπάρχει ο ακόλουθος κανόνας: εάν χαθούν ορόσημα, πρέπει να μείνετε στη θέση τους, να δημιουργήσετε ένα καταφύγιο και να περιμένετε το τέλος κακοκαιρίας (μπορεί να βγει ήλιος) ή για βοήθεια. Στο δάσος, τα ορόσημα - δέντρα ή θάμνοι - θα σας βοηθήσουν να κινηθείτε σε ευθεία γραμμή και κάθε φορά που χρειάζεται να μένετε σε δύο τέτοια ορόσημα - το ένα μπροστά, το άλλο πίσω. Αλλά, φυσικά, είναι καλύτερο να έχετε μαζί σας μια πυξίδα...
Ilya Leenson
Βιβλιογραφία:
Μάριο Λιότσι. Ιστορία της φυσικής. Μ., Μιρ, 1970
Κέρκερ Μ. Brownian Movements and Molecular Reality Πριν από το 1900. Journal of Chemical Education, 1974, τομ. 51, Νο. 12
Leenson I.A. Χημικές αντιδράσεις. M., Astrel, 2002








