Серная кислота
H 2 SO 4 , молярная масса 98,082; бесцветная маслянистая без запаха. Очень сильная двухосновная кислота, при 18°С pK a
1 - 2,8, K 2 1,2·10 -2 , pK a
2 1,92; длины связей в S=O 0,143 нм, S-ОН 0,154 нм, угол HOSOH 104°, OSO 119°; кипит с разложением, образуя (98,3% H 2 SO 4 и 1,7% Н 2 О с температурой кипения 338,8°С; см. также табл. 1). Серная кислота
, отвечающая 100%-ному содержанию H 2 SO 4 , имеет состав (%): H 2 SO 4 99,5%, HSO 4 - 0,18%, H 3 SO 4 + 0,14%, H 3 О + 0,09%, H 2 S 2 O 7 0,04%, HS 2 O 7 0,05%. Смешивается с и SO 3 во всех соотношениях. В водных растворах серная кислота
практически полностью диссоциирует на Н + , HSO 4 - и SO 4 2- . Образует H 2 SO 4 ·n
H 2 O, где n
=1, 2, 3, 4 и 6,5.
растворы SO 3 в серной кислоте называются олеумом, они образуют два соединения H 2 SO 4 ·SO 3 и H 2 SO 4 ·2SO 3 . Олеум содержит также пиросерную кислоту, получающуюся по реакции: Н 2 SO 4 +SO 3 =H 2 S 2 O 7 .
Получение серной кислоты
Сырьем для получения серной кислоты
служат: S, сульфиды металлов, H 2 S, отходящие теплоэлектростанций, сульфаты Fe, Ca и др. Основные стадии получения серной кислоты
: 1) сырья с получением SO 2 ; 2) SO 2 до SO 3 (конверсия); 3) SO 3 . В промышленности применяют два метода получения серной кислоты
, отличающихся способом окисления SO 2 , - контактный с использованием твердых катализаторов (контактов) и нитрозный - с оксидами азота. Для получения серной кислоты
контактным способом на современных заводах применяют ванадиевые катализаторы, вытеснившие Pt и оксиды Fe. Чистый V 2 O 5 обладает слабой каталитической активностью, резко возрастающей в присутствии щелочных металлов, причем наибольшее влияние оказывают соли К. Промотирующая роль щелочных металлов обусловлена образованием низкоплавких пиросульфованадатов (3К 2 S 2 О 7 · V 2 О 5 , 2К 2 S 2 O 7 · V 2 O 5 и K 2 S 2 O 7 ·V 2 O 5 , разлагающихся соответственно при 315-330, 365-380 и 400-405 °С). Активный компонент в условиях катализа находится в расплавленном состоянии.
Схему окисления SO 2 в SO 3 можно представить следующим образом:
На первой стадии достигается равновесие, вторая стадия медленная и определяет скорость процесса.
Производство серной кислоты
из серы по методу двойного контактирования и двойной абсорбции (рис. 1) состоит из следующих стадий. Воздух после очистки от пыли подается газодувкой в сушильную башню, где он осушается 93-98%-ной серной кислотой
до содержания влаги 0,01% по объему. Осушенный воздух поступает в серную печь после предварительного подогрева в одном из теплообменников контактного узла. В печи сжигается сера, подаваемая форсунками: S + О 2 = SO 2 + 297,028 кДж. Газ, содержащий 10-14% по объему SO 2 , охлаждается в котле и после разбавления воздухом до содержания SO 2 9-10% по объему при 420°С поступает в контактный аппарат на первую стадию конверсии, которая протекает на трех слоях катализатора (SO 2 + V 2 O 2 = SO 3 + 96,296 кДж), после чего газ охлаждается в теплообменниках. Затем газ, содержащий 8,5-9,5% SO 3 , при 200°С поступает на первую стадию абсорбции в абсорбер, орошаемый и 98%-ной серной кислотой
: SO 3 + Н 2 О = Н 2 SO 4 + 130,56 кДж. Далее газ проходит очистку от брызг серной кислоты
, нагревается до 420°С и поступает на вторую стадию конверсии, протекающую на двух слоях катализатора. Перед второй стадией абсорбции газ охлаждается в экономайзере и подается в абсорбер второй ступени, орошаемый 98%-ной серной кислотой
, и затем после очистки от брызг выбрасывается в атмосферу.
1 - серная печь; 2 - котел-утилизатор; 3 - экономайзер; 4 - пусковая топка; 5, 6 - теплообменники пусковой топки; 7 - контактный аппарат; 8 - теплообменники; 9 - олеумный абсорбер; 10 - сушильная башня; 11 и 12 - соответственно первый и второй моногидратные абсорберы; 13 - сборники кислоты.
1 - тарельчатый питатель; 2 - печь; 3 - котел-утилизатор; 4 - циклоны; 5 - электрофильтры; 6 - промывные башни; 7 - мокрые электрофильтры; 8 - отдувочная башня; 9 - сушильная башня; 10 - брызгоуловитель; 11 - первый моногидратный абсорбер; 12 - теплообменники; 13 - контактный аппарат; 14 - олеумный абсорбер; 15 - второй моногидратный абсорбер; 16 - холодильники; 17 - сборники.
1 - денитрационная башня; 2, 3 - первая и вторая продукционные башни; 4 - окислительная башня; 5, 6, 7 - абсорбционные башни; 8 - электрофильтры.
Производство серной кислоты
из сульфидов металлов (рис. 2) существенно сложнее и состоит из следующих операций. Обжиг FeS 2 производят в печи кипящего слоя на воздушном дутье: 4FeS 2 + 11О 2 = 2Fe 2 O 3 + 8SO 2 + 13476 кДж. Обжиговый газ с содержанием SO 2 13-14%, имеющий температуру 900°С, поступает в котел, где охлаждается до 450°С. Очистку от пыли осуществляют в циклоне и электрофильтре. Далее газ проходит через две промывные башни, орошаемые 40%-ной и 10%-ной серной кислотой
. При этом газ окончательно очищается от пыли, фтора и мышьяка. Для очистки газа от аэрозоля серной кислоты
, образующегося в промывных башнях, предусмотрены две ступени мокрых электрофильтров. После осушки в сушильной башне, перед которой газ разбавляется до содержания 9% SO 2 , его газодувкой подают на первую стадию конверсии (3 слоя катализатора). В теплообменниках газ подогревается до 420°С благодаря теплу газа, поступающего с первой стадии конверсии. SO 2 , окисленный на 92-95% в SO 3 , идет на первую стадию абсорбции в олеумный и моногидратный абсорберы, где освобождается от SO 3 . Далее газ с содержанием SO 2 ~ 0,5% поступает на вторую стадию конверсии, которая протекает на одном или двух слоях катализатора. Предварительно газ нагревается в другой группе теплообменников до420 °С благодаря теплу газов, идущих со второй стадии катализа. После отделения SO 3 на второй стадии абсорбции газ выбрасывается в атмосферу.
Степень превращения SO 2 в SO 3 при контактном способе 99,7%, степень абсорбции SO 3 99,97%. Производство серной кислоты
осуществляют и в одну стадию катализа, при этом степень превращения SO 2 в SO 3 не превышает 98,5%. Перед выбросом в атмосферу газ очищают от оставшегося SO 2 (см. ). Производительность современных установок 1500-3100 т/сут.
Сущность нитрозного метода (рис. 3) состоит в том, что обжиговый газ после охлаждения и очистки от пыли обрабатывают так называемой нитрозой - серной кислотой
, в которой растворены оксиды азота. SO 2 поглощается нитрозой, а затем окисляется: SO 2 + N 2 O 3 + Н 2 О = Н 2 SO 4 + NO. Образующийся NO плохо растворим в нитрозе и выделяется из нее, а затем частично окисляется кислородом в газовой фазе до NO 2 . Смесь NO и NO 2 вновь поглощается серной кислотой
и т.д. Оксиды азота не расходуются в нитрозном процессе и возвращаются в производственный цикл, вследствие неполного поглощения их серной кислотой
они частично уносятся отходящими газами. Достоинства нитрозного метода: простота аппаратурного оформления, более низкая себестоимость (на 10-15% ниже контактной), возможность 100%-ной переработки SO 2 .
Аппаратурное оформление башенного нитрозного процесса несложно: SO 2 перерабатывается в 7-8 футерованных башнях с керамической насадкой, одна из башен (полая) является регулируемым окислительным объемом. Башни имеют сборники кислоты, холодильники, насосы, подающие кислоту в напорные баки над башнями. Перед двумя последними башнями устанавливается хвостовой вентилятор. Для очистки газа от аэрозоля серной кислоты
служит электрофильтр. Оксиды азота, необходимые для процесса, получают из HNO 3 . Для сокращения выброса оксидов азота в атмосферу и 100%-ной переработки SO 2 между продукционной и абсорбционной зонами устанавливается безнитрозный цикл переработки SO 2 в комбинации с водно-кислотным методом глубокого улавливания оксидов азота. Недостаток нитрозного метода - низкое качество продукции: концентрация серной кислоты
75%, наличие оксидов азота, Fe и др. примесей.
Для уменьшения возможности кристаллизации серной кислоты
при перевозке и хранении установлены стандарты на товарные сорта серной кислоты
, концентрация которых соответствует наиболее низким температурам кристаллизации. Содержание серной кислоты
в технических сортах (%): башенная (нитрозная) 75, контактная 92,5-98,0, олеум 104,5, высокопроцентный олеум 114,6, аккумуляторная 92-94. Серную кислоту
хранят в стальных резервуарах объемом до 5000 м 3 , их общая емкость на складе рассчитана на десятисуточньй выпуск продукции. Олеум и серную кислоту
перевозят в стальных железнодорожных цистернах. Концентрированную и аккумуляторную серную кислоту
перевозят в цистернах из кислотостойкой стали. Цистерны для перевозки олеума покрывают теплоизоляцией и перед заливкой олеум подогревают.
Определяют серную кислоту
колориметрически и фотометрически, в виде взвеси BaSO 4 - фототурбидиметрически, а также кулонометрическим методом.
Применение серной кислоты
Серную кислоту применяют в производстве минеральных удобрений, как электролит в свинцовых аккумуляторах, для получения различных минеральных кислот и солей, химических волокон, красителей, дымообразующих веществ и взрывчатых веществ, в нефтяной, металлообрабатывающей, текстильной, кожевенной и др. отраслях промышленности. Ее используют в промышленном органическом синтезе в реакциях дегидратации (получение диэтилового эфира, сложных эфиров), гидратации (этанол из этилена), сульфирования ( и промежуточные продукты в производстве красителей), алкилирования (получение изооктана, полиэтиленгликоля, капролактама) и др. Самый крупный потребитель серной кислоты
- производство минеральных удобрений. На 1 т Р 2 О 5 фосфорных удобрений расходуется 2,2-3,4 т серной кислоты
, а на 1 т (NH 4) 2 SO 4 - 0,75 т серной кислоты
. Поэтому сернокислотные заводы стремятся строить в комплексе с заводами по производству минеральных удобрений. Мировое производство серной кислоты
в 1987 достигло 152 млн. тонн.
Серная кислота и олеум - чрезвычайно агрессивные вещества, поражают дыхательные пути, кожу, слизистые оболочки, вызывают затруднение дыхания, кашель, нередко - ларингит, трахеит, бронхит и т.д. ПДК аэрозоля серной кислоты в воздухе рабочей зоны 1,0 мг/м 3 , в атмосферном 0,3 мг/м 3 (максимальная разовая) и 0,1 мг/м 3 (среднесуточная). Поражающая концентрация паров серной кислоты 0,008 мг/л (экспозиция 60 мин), смертельная 0,18 мг/л (60 мин). Класс опасности 2. Аэрозоль серной кислоты может образовываться в атмосфере в результате выбросов химических и металлургических производств, содержащих оксиды S, и выпадать в виде кислотных дождей.
Автор Химическая энциклопедия г.р. Н.С.ЗефировСЕРНАЯ КИСЛОТА
H 2 SO 4 ,
молекулярная масса 98,082; бесцв. маслянистая жидкость без запаха. Очень сильная двухосновная
кислота, при 18°С pK a
1 - 2,8,
K 2 1,2 10 -2 , pK a 2 l,92;
длины связей в молекуле S=O 0,143 нм, S-ОН 0,154 нм, угол HOSOH 104°, OSO
119°; кипит с различные, образуя азеотропную смесь (98,3% H 2 SO 4
и 1,7% Н 2 О с температура кипения 338,8 °С; см. также табл. 1). СЕРНАЯ КИСЛОТА к., отвечающая
100%-ному содержанию H 2 SO 4 , имеет состав (%): H 2 SO 4
99,5, 0,18,
0,14, Н 3 О +
0,09, H 2 S 2 O 7 0,04, HS 2 O 7
0,05. Смешивается с водой и SO 3 во всех соотношениях. В водных растворах
СЕРНАЯ КИСЛОТА к. практически полностью диссоциирует на Н + ,
и . Образует гидраты
H 2 SO 4 nH 2 O, где n = 1, 2, 3,
4 и 6,5.
Растворы SO 3 в СЕРНАЯ КИСЛОТА
к. называют олеумом, они образуют два соединение H 2 SO 4 SO 3
и H 2 SO 4 2SO 3 . Олеум содержит также пи-росерную
кислоту, получающуюся по реакции: Н 2 SO 4 + + SO 3 :
H 2 S 2 O 7 .


Температура кипения водных растворов
СЕРНАЯ КИСЛОТА к. повышается с ростом ее концентрации и достигает максимума при содержании
98,3% H 2 SO 4 (табл. 2). Температура кипения олеума с увеличением
содержания SO 3 понижается. При увеличении концентрации водных растворов
СЕРНАЯ КИСЛОТА к. общее давление пара над растворами понижается и при содержании 98,3% H 2 SO 4
достигает минимума. С увеличением концентрации SO 3 в олеуме общее
давление пара над ним повышается. Давление пара над водными растворами СЕРНАЯ КИСЛОТА к. и олеума
можно вычислить по уравению: lgp(Пa) = А - В/Т+ 2,126, величины
коэффициент А и В зависят от концентрации СЕРНАЯ КИСЛОТА к. Пар над водными растворами
СЕРНАЯ КИСЛОТА к. состоит из смеси паров воды, Н 2 SO 4 и SO 3 ,
при этом состав пара отличается от состава жидкости при всех концентрациях СЕРНАЯ КИСЛОТА
к., кроме соответствующей азеотропной смеси.
С повышением температуры усиливается
диссоциация H 2 SO 4
H 2 О + SO 3 - Q, уравение температурной зависимости
константы равновесия lnК p = 14,74965 - 6,71464ln(298/T)
- 8, 10161 10 4 T 2 -9643,04/T-9,4577 10 -3 Т+2,19062
x 10 -6 T 2 . При нормальном давлении степень
диссоциации: 10 -5 (373 К), 2,5 (473 К), 27,1 (573 К), 69,1 (673 К).
Плотность 100%-ной СЕРНАЯ КИСЛОТА к. можно определить по уравению: d= 1,8517 - - 1,1
10 -3 t + 2 10 -6 t 2 г/см 3 .
С повышением концентрации растворов СЕРНАЯ КИСЛОТА к. их теплоемкость уменьшается и достигает
минимума для 100%-ной СЕРНАЯ КИСЛОТА к., теплоемкость олеума с повышением содержания SO 3
увеличивается.
При повышении концентрации
и понижении температуры теплопроводность l
уменьшается: l
= 0,518 + 0,0016t
- (0,25 + + t/1293) С/100, где С-концентрация СЕРНАЯ КИСЛОТА к., в %. Макс.
вязкость имеет олеум H 2 SO 4 SO 3 , с повышением
температуры h
снижается. Электрич. сопротивление СЕРНАЯ КИСЛОТА к. минимально при концентрации
30 и 92% H 2 SO 4 и максимально при концентрации 84 и 99,8%
H 2 SO 4 . Для олеума миним. r
при концентрации 10% SO 3 .
С повышением температуры r
СЕРНАЯ КИСЛОТА к. увеличивается. Диэлектрич. проницаемость 100%-ной
СЕРНАЯ КИСЛОТА к. 101 (298,15 К), 122 (281,15 К); криоскопич. постоянная 6,12, эбулиоскопич.
постоянная 5,33; коэффициент диффузии пара СЕРНАЯ КИСЛОТА к. в воздухе изменяется с изменением
температуры; D = 1,67 10 -5 T 3/2 см 2 /с.
СЕРНАЯ КИСЛОТА к.-довольно сильный
окислитель, особенно при нагревании; окисляет HI и частично НВг до свободный галогенов,
углерод-до СО 2 , S-до SO 2 , окисляет многие металлы (Си, Hg
и др.). При этом СЕРНАЯ КИСЛОТА к. восстанавливается до SO 2 , а наиболее сильными
восстановителями-до S и H 2 S. Конц. H 2 SO 4 частично
восстанавливается Н 2 , из-за чего не может применяться для его
сушки. Разб. H 2 SO 4 взаимодействие со всеми металлами, находящимися
в электрохимический ряду напряжений левее водорода, с выделением Н 2 . Окислит.
свойства для разбавленый H 2 SO 4 нехарактерны. СЕРНАЯ КИСЛОТА к. дает два ряда
солей: средние-сульфаты и кислые-гидросульфаты (см. Сульфаты неорганические),
а также эфиры (см. Сульфаты органические). Известны пероксомоносерная
(кислота Каро) H 2 SO 5 и пероксоди-серная H 2 S 2 O 8
кислоты (см. Сера).
Получение.
Сырьем
для получения СЕРНАЯ КИСЛОТА к. служат: S, сульфи-ды металлов, H 2 S, отходящие
газы теплоэлектростанций, сульфаты Fe, Ca и др. Осн. стадии получения СЕРНАЯ КИСЛОТА к.:
1) обжиг сырья с получением SO 2 ; 2) окисление SO 2 до SO 3
(конверсия); 3) абсорбция SO 3 . В промышленности применяют два метода получения
СЕРНАЯ КИСЛОТАк., отличающихся способом окисления SO 2 ,-контактный с использованием
твердых катализаторов (контактов) и нитрозный-с оксидами азота. Для получения
СЕРНАЯ КИСЛОТА к. контактным способом на современной заводах применяют ванадиевые катализаторы,
вытеснившие Pt и оксиды Fe. Чистый V 2 O 5 обладает слабой
каталитических активностью, резко возрастающей в присутствии солей щелочных металлов,
причем наиболее влияние оказывают соли К. Промотирующая роль щелочных металлов
обусловлена образованием низкоплавких пиросульфованадатов (3К 2 S 2 О 7
V 2 О 5 , 2К 2 S 2 O 7 V 2 O 5
и K 2 S 2 O 7 V 2 O 5 ,
разлагающихся соответственно при 315-330, 365-380 и 400-405 °С). Активный компонент
в условиях катализа находится в расплавленном состоянии.
Схему окисления SO 2 в SO 3 можно представить следующей образом:
На первой стадии достигается
равновесие, вторая стадия медленная и определяет скорость процесса.
Произ-во СЕРНАЯ КИСЛОТА к. из серы
по методу двойного контактирования и двойной абсорбции (рис. 1) состоит из следующей
стадий. Воздух после очистки от пыли подается газодувкой в сушильную башню,
где он осушается 93-98%-ной СЕРНАЯ КИСЛОТА к. до содержания влаги 0,01% по объему. Осушенный
воздух поступает в серную печь после предварит. подогрева в одном из теплообменников
контактного узла. В печи сжигается сера, подаваемая форсунками: S + О 2
:
SO 2 + + 297,028 кДж. Газ, содержащий 10-14% по объему SO 2 ,
охлаждается в котле и после разбавления воздухом до содержания SO 2
9-10% по объему при 420 °С поступает в контактный аппарат на первую стадию
конверсии, которая протекает на трех слоях катализатора (SO 2 + V 2 O 2
:
:
SO 3 + 96,296 кДж), после чего газ охлаждается в теплообменниках.
Затем газ, содержащий 8,5-9,5% SO 3 , при 200 °С поступает на первую
стадию абсорбции в абсорбер, орошаемый олеумом и 98%-ной СЕРНАЯ КИСЛОТА к.: SO 3
+ Н 2 О :
Н 2 SO 4 + + 130,56 кДж. Далее
газ проходит очистку от брызг СЕРНАЯ КИСЛОТА к., нагревается до 420 °С и поступает на
вторую стадию конверсии, протекающую на двух слоях катализатора. Перед второй
стадией абсорбции газ охлаждается в экономайзере и подается в абсорбер второй
ступени, орошаемый 98%-ной СЕРНАЯ КИСЛОТА к., и затем после очистки от брызг выбрасывается
в атмосферу.
Рис. 1. Схема производства
серной кислоты из серы: 1-серная печь; 2-котел-утилизатор; 3 - экономайзер; 4-пусковая
топка; 5, 6-теплообменники пусковой топки; 7-контактный аппарат; 8-теплообменники;
9-олеумный абсорбер; 10-сушильная башня; 11 и 12-соответственно первый и второй моногидратные
абсорберы; 13-сборники кислоты.

Рис.2. Схема производства серной
кислоты из колчедана: 1-тарельчатый питатель; 2-печь; 3-котел-утилизатор; 4-циклоны;
5-электрофильтры; 6-промывные башни; 7-мокрые электрофильтры; 8-отдувочная башня;
9-сушильная башня; 10-брызгоуловитель; 11-первый моногидратный абсорбер; 12-теплообмен-вики;
13 - контактный аппарат; 14-олеумный абсорбер; 15-второй моногидратный абсорбер;
16-холодильники; 17-сборники.

Рис. 3. Схема производства
серной кислоты нитроз-ным методом: 1 - денитрац. башня; 2, 3-первая и вторая продукц.
башни; 4-окислит. башня; 5, 6, 7-абсорбц. башни; 8 - электрофильтры.
Произ-во СЕРНАЯ КИСЛОТА к. из сульфидов
металлов (рис. 2) существенно сложнее и состоит из следующей операций. Обжиг FeS 2
производят в печи кипящего слоя на воздушном дутье: 4FeS 2 +
11О 2 :
2Fe 2 O 3 + 8SO 2 + 13476
кДж. Обжиговый газ с содержанием SO 2 13-14%, имеющий температуру 900 °С,
поступает в котел, где охлаждается до 450 °С. Очистку от пыли осуществляют
в циклоне и электрофильтре. Далее газ проходит через две промывные башни, орошаемые
40%-ной и 10%-ной СЕРНАЯ КИСЛОТА к. При этом газ окончательно очищается от пыли, фтора и
мышьяка. Для очистки газа от аэрозоля СЕРНАЯ КИСЛОТА к., образующегося в промывных башнях,
предусмотрены две ступени мокрых электрофильтров. После осушки в сушильной башне,
перед которой газ разбавляется до содержания 9% SO 2 , его газодувкой
подают на первую стадию конверсии (3 слоя катализатора). В теплообменниках газ
подогревается до 420 °С благодаря теплу газа, поступающего с первой стадии
конверсии. SO 2 , окисленный на 92-95% в SO 3 , идет на первую
стадию абсорбции в олеумный и моногидратный абсорберы, где освобождается от
SO 3 . Далее газ с содержанием SO 2 ~ 0,5% поступает на вторую
стадию конверсии, которая протекает на одном или двух слоях катализатора. Предварительно
газ нагревается в др. группе теплообменников до 420 °С благодаря теплу газов,
идущих со второй стадии катализа. После отделения SO 3 на второй стадии
абсорбции газ выбрасывается в атмосферу.
Степень превращения SO 2
в SO 3 при контактном способе 99,7%, степень абсорбции SO 3
99,97%. Произ-во СЕРНАЯ КИСЛОТА к. осуществляют и в одну стадию катализа, при этом степень
превращения SO 2 в SO 3 не превышает 98,5%. Перед выбросом
в атмосферу газ очищают от оставшегося SO 2 (см. Газов очистка).
Производительность современной установок 1500-3100 т/сут.
Сущность нитрозного метода
(рис. 3) состоит в том, что обжиговый газ после охлаждения и очистки от пыли
обрабатывают так называемой нитрозой-С. к., в которой раств. оксиды азота. SO 2
поглощается нитрозой, а затем окисляется: SO 2 + N 2 O 3
+ Н 2 О :
Н 2 SO 4 + NO. Образующийся NO плохо
растворим в нитрозе и выделяется из нее, а затем частично окисляется кислородом
в газовой фазе до NO 2 . Смесь NO и NO 2 вновь поглощается
СЕРНАЯ КИСЛОТАк. и т.д. Оксиды азота не расходуются в нитрозном процессе и возвращаются
в производств. цикл, вследствие неполного поглощения их СЕРНАЯ КИСЛОТА к. они частично уносятся
отходящими газами. Достоинства нитрозного метода: простота аппаратурного оформления,
более низкая себестоимость (на 10-15% ниже контактной), возможность 100%-ной
переработки SO 2 .
Аппаратурное оформление
башенного нитрозного процесса несложно: SO 2 перерабатывается в 7-8
футерованных башнях с керамич. насадкой, одна из башен (полая) является регулируемым
окислит. объемом. Башни имеют сборники кислоты, холодильники, насосы, подающие
кислоту в напорные баки над башнями. Перед двумя последними башнями устанавливается
хвостовой вентилятор. Для очистки газа от аэрозоля СЕРНАЯ КИСЛОТА к. служит электрофильтр.
Оксиды азота, необходимые для процесса, получают из HNO 3 . Для сокращения
выброса оксидов азота в атмосферу и 100%-ной переработки SO 2 между
продукционной и абсорбционной зонами устанавливается безнитрозный цикл переработки
SO 2 в комбинации с водно-кислотным методом глубокого улавливания
оксидов азота. Недостаток нитрозного метода-низкое качество продукции: концентрация
СЕРНАЯ КИСЛОТА к. 75%, наличие оксидов азота, Fe и др. примесей.
Для уменьшения возможности
кристаллизации СЕРНАЯ КИСЛОТА к. при перевозке и хранении установлены стандарты на товарные
сорта СЕРНАЯ КИСЛОТА к., концентрация которых соответствует наиболее низким температурам кристаллизации.
Содержание СЕРНАЯ КИСЛОТА к. в техн. сортах (%): башенная (нитрозная) 75, контактная 92,5-98,0,
олеум 104,5, высокопроцентный олеум 114,6, аккумуляторная 92-94. СЕРНАЯ КИСЛОТА к. хранят
в стальных резервуарах объемом до 5000 м 3 , их общая емкость на складе
рассчитана на десятисуточньш выпуск продукции. Олеум и СЕРНАЯ КИСЛОТА к. перевозят в стальных
железнодорожных цистернах. Конц. и аккумуляторную СЕРНАЯ КИСЛОТА к. перевозят в цистернах
из кислотостойкой стали. Цистерны для
перевозки олеума покрывают теплоизоляцией и перед заливкой олеум подогревают.
Определяют СЕРНАЯ КИСЛОТА к. колориметрически
и фотометрически, в виде взвеси BaSO 4 - фототурбидиметрически, а
также ку-лонометрич. методом.
Применение. СЕРНАЯ КИСЛОТА к. применяют
в производстве минеральных удобрений, как электролит в свинцовых аккумуляторах, для получения
различные минеральных кислот и солей, химический волокон, красителей, дымообразующих веществ и ВВ,
в нефтяной, металлообрабатывающей, текстильной, кожевенной и др. отраслях промышленности.
Ее используют в пром. органическое синтезе в реакциях дегидратации (получение диэтилового
эфира, сложных эфиров), гидратации (этанол из этилена), сульфирования (синтетич.
моющие средства и промежуточные продукты в производстве красителей), алкили-рования (получение
изооктана, полиэтиленгликоля, капро-лактама) и др. Самый крупный потребитель
СЕРНАЯ КИСЛОТАк.-производство минеральных удобрений. На 1 т Р 2 О 5 фосфорных
удобрений расходуется 2,2-3,4 т СЕРНАЯ КИСЛОТА к., а на 1 т (NH 4) 2 SO 4 -0,75
т СЕРНАЯ КИСЛОТА к. Поэтому сернокислотные заводы стремятся строить в комплексе с заводами
по производству минеральных удобрений. Мировое производство СЕРНАЯ КИСЛОТА к. в 1987 достигло 152 млн.
т.
СЕРНАЯ КИСЛОТА к. и олеум - чрезвычайно
агрессивные вещества, поражают дыхательные пути, кожу, слизистые оболочки, вызывают затруднение
дыхания, кашель, нередко-ларингит, трахеит, бронхит и т. д. ПДК аэрозоля СЕРНАЯ КИСЛОТА
к. в воздухе рабочей зоны 1,0 мг/м 3 , в атм. воздухе 0,3 мг/м 3
(макс. разовая) и 0,1 мг/м 3 (среднесуточная). Поражающая концентрация
паров СЕРНАЯ КИСЛОТА к. 0,008 мг/л (экспозиция 60 мин), смертельная 0,18 мг/л (60 мин).
Класс опасности 2. Аэрозоль СЕРНАЯ КИСЛОТА к. может образовываться в атмосфере в результате
выбросов химический и металлургич. производств, содержащих оксиды S, и выпадать в виде
кислотных дождей.
Литература: Справочник
сернокислотчика, под ред. К. М. Малина, 2 изд., М., 1971; Амелин А. Г., Технология
серной кислоты, 2 изд., М., 1983; Васильев Б. Т., Отвагина М. И., Технология
серной кислоты, М., 1985. Ю.В. Филатов.
Химическая энциклопедия. Том 4 >>
ОПРЕДЕЛЕНИЕ
Безводная серная кислота представляет собой тяжелую, вязкую жидкость, которая легко смешивается с водой в любой пропорции: взаимодействие характеризуется исключительно большим экзотермическим эффектом (~880 кДж/моль при бесконечном разбавлении) и может привести к взрывному вскипанию и разбрызгиванию смеси, если воду добавлять к кислоте; поэтому так важно всегда использовать обратный порядок в приготовлении растворов и добавлять кислоту в воду, медленно и при перемешивании.
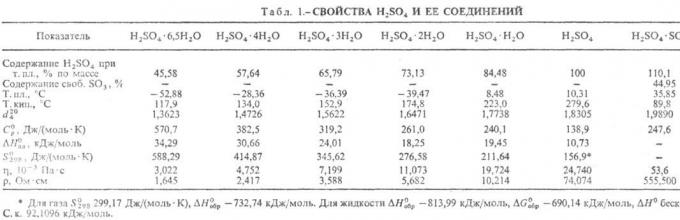
Некоторые физические свойства серной кислоты приведены в таблице.
Безводная H 2 SO 4 — замечательное соединение с необычно высокой диэлектрической проницаемостью и очень высокой электропроводностью, которая обусловлена ионной автодиссоциацией (автопротолизом) соединения, а также эстафетным механизмом проводимости с переносом протона, обеспечивающим протекание электрического тока через вязкую жидкость с большим числом водородных связей.
Таблица 1. Физические свойства серной кислоты.
Получение серной кислоты
Серная кислота — самый важный промышленный химикат и самая дешевая из производимых в большом объеме кислот влюбой стране мира.
Концентрированную серную кислоту («купоросное масло») сначала получали нагреванием «зеленого купороса» FeSO 4 ×nH 2 O и расходовали в большом количестве на получение Na 2 SO 4 и NaCl.
В современном процессе получения серной кислоты используется катализатор, состоящий из оксида ванадия(V) с добавкой сульфата калия на носителе из диоксида кремния или кизельгура. Диоксид серы SO 2 получают сжиганием чистойсеры или при обжиге сульфидной руды (прежде всего пирита или руд Си, Ni и Zn) в процессе извлечения этихметаллов.Затем SO 2 окисляют до триоксида, а потом путем растворения в воде получают серную кислоту:
S + O 2 → SO 2 (ΔH 0 — 297 кДж/моль);
SO 2 + ½ O 2 → SO 3 (ΔH 0 — 9,8 кДж/моль);
SO 3 + H 2 O → H 2 SO 4 (ΔH 0 — 130 кДж/моль).
Химические свойства серной кислоты
Серная кислота - сильная двухосновная кислота. По первой ступени в растворах невысокой концентрации она диссоциирует практически нацело:
H 2 SO 4 ↔H + + HSO 4 — .
Диссоциация по второй ступени
HSO 4 — ↔H + + SO 4 2-
протекает в меньшей степени. Константа диссоциации серной кислоты по второй ступени, выраженная через активности ионов, K 2 = 10 -2 .
Как кислота двухосновная, серная кислота образует два ряда солей: средние и кислые. Средние соли серной кислоты называются сульфатами, а кислые - гидросульфатами.
Серная кислота жадно поглощает пары воды и поэтому часто применяется для осушения газов. Способностью поглощать воду объясняется и обугливание многих органических веществ, особенно относящихся к классу углеводов (клетчатка, сахар и т.д.), при действии на них концентрированной серной кислоты. Серная кислота отнимает от углеводов водород и кислород, которые образуют воду, а углерод выделяется в виде угля.
Концентрированная серная кислота, особенно горячая, — энергичный окислитель. Она окисляет HI и HBr (но не HCl) до свободных галогенов, уголь - до CO 2 , серу - до SO 2 . Указанные реакции выражаются уравнениями:
8HI + H 2 SO 4 = 4I 2 + H 2 S + 4H 2 O;
2HBr + H 2 SO 4 = Br 2 + SO 2 + 2H 2 O;
C + 2H 2 SO 4 = CO 2 + 2SO 2 + 2H 2 O;
S + 2H 2 SO 4 = 3SO 2 + 2H 2 O.
Взаимодействие серной кислоты с металлами протекает различно в зависимости от её концентрации. Разбавленная серная кислота окисляет своим ионом водорода. Поэтому она взаимодействует только с теми металлами, которые стоят в ряду напряжений только до водорода, например:
Zn + H 2 SO 4 = ZnSO 4 + H 2 .
Однако свинец не растворяется в разбавленной кислоте, поскольку образующаяся соль PbSO 4 нерастворима.
Концентрированная серная кислота является окислителем за счет серы (VI). Она окисляет металлы, стоящие в ряду напряжений до серебра включительно. Продукты её восстановления могут быть различными в зависимости от активности металла и от условий (концентрация кислоты, температура). При взаимодействии с малоактивными металлами, например с медью, кислота восстанавливается до SO 2:
Cu + 2H 2 SO 4 = CuSO 4 + SO 2 + 2H 2 O.
При взаимодействии с более активными металлами продуктами восстановления могут быть как диоксид, так и свободная сера и сероводород. Например, при взаимодействии с цинком могут протекать реакции:
Zn + 2H 2 SO 4 = ZnSO 4 + SO 2 + 2H 2 O;
3Zn + 4H 2 SO 4 = 3ZnSO 4 + S↓ + 4H 2 O;
4Zn + 5H 2 SO 4 = 4ZnSO 4 + H 2 S + 4H 2 O.
Применение серной кислоты
Применение серной кислоты меняется от страны к стране и от десятилетия к десятилетию. Так, например в США в настоящее время главная область потребления H 2 SO 4 — производство удобрений (70%), за ним следуют химическое производство, металлургия, очистка нефти (~5% в каждой области). В Великобритании распределение потребления по отраслям иное: только 30% производимой H 2 SO 4 используется в производстве удобрений, зато 18% идет на краски, пигменты и полупродукты производства красителей, 16% на химическое производство, 12% на получение мыла и моющих средств, 10% на производство натуральных и искусственных волокон и 2,5% применяется в металлургии.
Примеры решения задач
ПРИМЕР 1
| Задание | Определите массу серной кислоты, которую можно получить из одной тонны пирита, если выход оксида серы (IV) в реакции обжига составляет 90%, а оксида серы (VI) в реакции каталитического окисления серы (IV) - 95% от теоретического. |
| Решение | Запишем уравнение реакции обжига пирита:
4FeS 2 + 11O 2 = 2Fe 2 O 3 + 8SO 2 . Рассчитаем количество вещества пирита: n(FeS 2) = m(FeS 2) / M(FeS 2); M(FeS 2) = Ar(Fe) + 2×Ar(S) = 56 + 2×32 = 120г/моль; n(FeS 2) = 1000 кг / 120 = 8,33 кмоль. Поскольку в уравнении реакции коэффициент при диоксиде серы в два раза больше, чем коэффициент при FeS 2 , то теоретически возможное количество вещества оксида серы (IV) равно: n(SO 2) theor = 2 ×n(FeS 2) = 2 ×8,33 = 16,66 кмоль. А практически полученное количество моль оксида серы (IV) составляет: n(SO 2) pract = η × n(SO 2) theor = 0,9 × 16,66 = 15 кмоль. Запишем уравнение реакции окисления оксида серы (IV) до оксида серы (VI): 2SO 2 + O 2 = 2SO 3 . Теоретически возможное количество вещества оксида серы (VI) равно: n(SO 3) theor = n(SO 2) pract = 15 кмоль. А практически полученное количество моль оксида серы (VI) составляет: n(SO 3) pract = η × n(SO 3) theor = 0,5 × 15 = 14,25 кмоль. Запишем уравнение реакции получения серной кислоты: SO 3 + H 2 O = H 2 SO 4 . Найдем количество вещества серной кислоты: n(H 2 SO 4) = n(SO 3) pract = 14,25 кмоль. Выход реакции составляет 100%. Масса серной кислоты равна: m(H 2 SO 4) = n(H 2 SO 4) × M(H 2 SO 4); M(H 2 SO 4) = 2×Ar(H) + Ar(S) + 4×Ar(O) = 2×1 + 32 + 4×16 = 98 г/моль; m(H 2 SO 4) = 14,25 × 98 = 1397 кг. |
| Ответ | Масса серной кислоты равна 1397 кг |
Свойства серной кислоты
Безводная серная кислота (моногидрат) представляет собой тяжелую маслянистую жидкость, которая смешивается с водой во всех соотношениях с выделением большого количества тепла. Плотность при 0 °С равна 1,85 г/см 3 . Она кипит при 296 °С и замерзает при - 10 °С. Серной кислотой называют не только моногидрат, но и водные растворы его (), а также растворы трехокиси серы в моногидрате (), называемые олеумом. Олеум на воздухе "дымит" вследствие десорбции из него. Чистая серная кислота бесцветна, техническая окрашена примесями в темный цвет.
Физические свойства серной кислоты, такие, как плотность, температура кристаллизации, температура кипения, зависят от ее состава. На рис. 1 представлена диаграмма кристаллизации системы. Максимумы в ней отвечают составу соединений или, наличие минимумов объясняется тем, что температура кристаллизации смесей двух веществ ниже температуры кристаллизации каждого из них.
Рис. 1
Безводная 100 %-ная серная кислота имеет сравнительно высокую температуру кристаллизации 10,7 °С. Чтобы уменьшить возможность замерзания товарного продукта при перевозке и хранении, концентрацию технической серной кислоты выбирают такой, чтобы она имела достаточно низкую температуру кристаллизации. Промышленность выпускает три вида товарной серной кислоты.
Серная кислота весьма активна. Она растворяет окислы металлов и большинство чистых металлов;вытесняет при повышенной температуре все другие кислоты из солей. Особенно жадно серная кислота соединяется с водой благодаря способности давать гидраты. Она отнимает воду от других кислот, от кристаллогидратов солей и даже кислородных производных углеводородов, которые содержат не воду таковую, а водород и кислород в сочетании Н:О = 2. дерево и другие растительные и животные ткани, содержащие целлюлозу, крахмал и сахар, разрушаются в концентрированной серной кислоте; вода связывается с кислотой и от ткани остается лишь мелкодисперсный углерод. В разбавленной кислоте целлюлоза и крахмал распадаются с образованием сахаров. При попадании на кожу человека концентрированная серная кислота вызывает ожоги.
Высокая активность серной кислоты в сочетании со сравнительно небольшой стоимостью производства предопределили громадные масштабы и чрезвычайное разнообразие ее применения (рис. 2). Трудно найти такую отрасль, в которой не потреблялась в тех или иных количествах серная кислота или произведенные из нее продукты.

Рис. 2
Крупнейшим потребителем серной кислоты является производство минеральных удобрений: суперфосфата, сульфата аммония и др. многие кислоты (например, фосфорная, уксусная, соляная) и соли производятся в значительной части при помощи серной кислоты. Серная кислота широко применяется в производстве цветных и редких металлов. В металлообрабатывающей промышленности серную кислоту или ее соли применяют для травления стальных изделий перед их окраской, лужением, никелированием, хромированием и т.п. значительные количества серной кислоты затрачиваются на очистку нефтепродуктов. Получение ряда красителей (для тканей), лаков и красок (для зданий и машин), лекарственных веществ и некоторых пластических масс также связано с применением серной кислоты. При помощи серной кислоты производятся этиловый и другие спирты, некоторые эфиры, синтетические моющие средства, ряд ядохимикатов для борьбы с вредителями сельского хозяйства и сорными травами. Разбавленные растворы серн6ой кислоты и ее солей применяют в производстве искусственного шелка, в текстильной промышленности для обработки волокна или тканей перед их крашением, а также в других отраслях легкой промышленности. В пищевой промышленности серная кислота применяется при получении крахмала, патоки и ряда других продуктов. Транспорт использует свинцовые сернокислотные аккумуляторы. Серную кислоту используют для осушки газов и при концентрировании кислот. Наконец, серную кислоту применяют в процессах нитрования и при производстве большей части взрывчатых веществ.