Σε ένα ζωντανό κύτταρο, η ροή πληροφοριών μεταξύ του πυρήνα και του κυτταροπλάσματος δεν στεγνώνει ποτέ, αλλά η κατανόηση όλων των «στροβιλισμών» του και η αποκρυπτογράφηση των πληροφοριών που κωδικοποιούνται σε αυτό είναι πραγματικά μια ηράκλεια εργασία. Μια από τις πιο σημαντικές ανακαλύψεις στη βιολογία του περασμένου αιώνα μπορεί να θεωρηθεί η ανακάλυψη μορίων πληροφοριών (ή μήτρας) RNA (mRNA ή mRNA), τα οποία χρησιμεύουν ως ενδιάμεσοι μεταφέροντας «μηνύματα» πληροφοριών από τον πυρήνα (από τα χρωμοσώματα) στο κυτταρόπλασμα. . Ο καθοριστικός ρόλος του RNA στη σύνθεση πρωτεϊνών είχε προβλεφθεί το 1939 στο έργο του Thorbjörn Kaspersson. Torbjörn Caspersson), Jean Brachet ( Jean Brachet) και ο Τζακ Σουλτς ( Τζακ Σουλτς), και το 1971 ο Γιώργος Μαρμπέης ( George Marbaix) πυροδότησε τη σύνθεση αιμοσφαιρίνης σε ωοκύτταρα βατράχου με έγχυση του πρώτου απομονωμένου αγγελιοφόρου RNA κουνελιού που κωδικοποιεί αυτήν την πρωτεΐνη.
Το 1956-1957 στη Σοβιετική Ένωση, ο A. N. Belozersky και ο A. S. Spirin απέδειξαν ανεξάρτητα την ύπαρξη mRNA και επίσης ανακάλυψαν ότι το μεγαλύτερο μέρος του RNA σε ένα κύτταρο δεν είναι πρότυπο, αλλά ριβοσωμικό RNA(rRNA). Το ριβοσωμικό RNA - ο δεύτερος «κύριος» τύπος κυτταρικού RNA - σχηματίζει τον «σκελετό» και το λειτουργικό κέντρο των ριβοσωμάτων σε όλους τους οργανισμούς. Είναι το rRNA (και όχι οι πρωτεΐνες) που ρυθμίζει τα κύρια στάδια της πρωτεϊνοσύνθεσης. Ταυτόχρονα, περιγράφηκε και μελετήθηκε ο τρίτος «κύριος» τύπος RNA - τα RNA μεταφοράς (tRNA), τα οποία σε συνδυασμό με δύο άλλα - mRNA και rRNA - σχηματίζουν ένα ενιαίο σύμπλεγμα πρωτεϊνοσύνθεσης. Σύμφωνα με την αρκετά δημοφιλή υπόθεση του «κόσμου RNA», ήταν αυτό το νουκλεϊκό οξύ που βρισκόταν στην ίδια την αρχή της ζωής στη Γη.
Λόγω του γεγονότος ότι το RNA είναι σημαντικά πιο υδρόφιλο σε σύγκριση με το DNA (λόγω της αντικατάστασης της δεοξυριβόζης με ριβόζη), είναι πιο ασταθές και μπορεί να κινείται σχετικά ελεύθερα στο κύτταρο, και ως εκ τούτου παρέχει βραχύβια αντίγραφα γενετικές πληροφορίες(mRNA) στη θέση όπου αρχίζει η πρωτεϊνοσύνθεση. Ωστόσο, αξίζει να σημειωθεί η "ταλαιπωρία" που σχετίζεται με αυτό - το RNA είναι πολύ ασταθές. Αποθηκεύεται πολύ χειρότερα από το DNA (ακόμη και μέσα σε ένα κύτταρο) και υποβαθμίζεται με την παραμικρή αλλαγή των συνθηκών (θερμοκρασία, pH). Εκτός από τη «δική του» αστάθεια, τεράστια συμβολήανήκει στις ριβονουκλεάσες (ή RNases) - μια κατηγορία ενζύμων διάσπασης RNA που είναι πολύ σταθερά και «πανταχού παρόντα» - ακόμη και το δέρμα των χεριών του πειραματιστή περιέχει αρκετά από αυτά τα ένζυμα για να αναιρέσει ολόκληρο το πείραμα. Εξαιτίας αυτού, η εργασία με RNA είναι πολύ πιο δύσκολη από ό,τι με πρωτεΐνες ή DNA - το τελευταίο μπορεί γενικά να αποθηκευτεί για εκατοντάδες χιλιάδες χρόνια χωρίς ουσιαστικά καμία ζημιά.
Φανταστική φροντίδα κατά τη διάρκεια της εργασίας, τρι-απόσταγμα, αποστειρωμένα γάντια, εργαστηριακά γυάλινα σκεύη μιας χρήσης - όλα αυτά είναι απαραίτητα για την πρόληψη της υποβάθμισης του RNA, αλλά η διατήρηση τέτοιων προτύπων δεν ήταν πάντα δυνατή. Ως εκ τούτου, για μεγάλο χρονικό διάστημα, απλά δεν έδωσαν προσοχή σε μικρά «θραύσματα» RNA, τα οποία αναπόφευκτα μόλυναν διαλύματα. Ωστόσο, με την πάροδο του χρόνου, κατέστη σαφές ότι, παρά όλες τις προσπάθειες να διατηρηθεί η στειρότητα της περιοχής εργασίας, συνέχισαν φυσικά να ανακαλύπτονται «συντρίμμια» και στη συνέχεια αποδείχθηκε ότι χιλιάδες βραχέων δίκλωνων RNAs υπάρχουν πάντα στο κυτταρόπλασμα , εκτελώντας πολύ συγκεκριμένες λειτουργίες και είναι απολύτως απαραίτητες για τη φυσιολογική ανάπτυξη των κυττάρων και του οργανισμού.
Αρχή της παρεμβολής RNA
Οι φαρμακοποιοί ενδιαφέρθηκαν επίσης για τη δυνατότητα χρήσης του siRNA, καθώς η ικανότητα να ρυθμίζεται ειδικά η λειτουργία μεμονωμένων γονιδίων υπόσχεται πρωτόγνωρες προοπτικές στη θεραπεία μιας σειράς ασθενειών. Το μικρό μέγεθος και η υψηλή ειδικότητα δράσης υπόσχονται υψηλή αποτελεσματικότητα και χαμηλή τοξικότητα των φαρμάκων που βασίζονται σε siRNA. λυσε ομως το προβλημα διανομήΤο siRNA σε άρρωστα κύτταρα στο σώμα δεν έχει ακόμη πετύχει - αυτό οφείλεται στην ευθραυστότητα και την ευθραυστότητα αυτών των μορίων. Και παρόλο που δεκάδες ομάδες προσπαθούν τώρα να βρουν έναν τρόπο να κατευθύνουν αυτές τις «μαγικές σφαίρες» ακριβώς στον στόχο (μέσα σε άρρωστα όργανα), δεν έχουν ακόμη επιτύχει ορατή επιτυχία. Εκτός από αυτό, υπάρχουν και άλλες δυσκολίες. Για παράδειγμα, στην περίπτωση της αντιιικής θεραπείας, η υψηλή εκλεκτικότητα της δράσης του siRNA μπορεί να είναι κακό - καθώς οι ιοί μεταλλάσσονται γρήγορα, το τροποποιημένο στέλεχος θα χάσει πολύ γρήγορα την ευαισθησία στο siRNA που επιλέχθηκε στην αρχή της θεραπείας: είναι γνωστό ότι Η αντικατάσταση ενός μόνο νουκλεοτιδίου στο siRNA οδηγεί σε σημαντική μείωση της επίδρασης παρεμβολής.
Σε αυτό το σημείο αξίζει να θυμηθούμε ξανά - ανακαλύφθηκαν τα siRNA μόνο σε φυτά, ασπόνδυλα και μονοκύτταρους οργανισμούς; Αν και ομόλογα πρωτεϊνών για παρεμβολή RNA (Dicer, σύμπλεγμα RISC) υπάρχουν επίσης σε ανώτερα ζώα, τα siRNA δεν ανιχνεύθηκαν με συμβατικές μεθόδους. Τι έκπληξη ήταν όταν εισήχθη τεχνητάσυνθετικά ανάλογα siRNA προκάλεσαν ισχυρή ειδική δοσοεξαρτώμενη επίδραση σε κυτταροκαλλιέργειες θηλαστικών! Αυτό σήμαινε ότι στα κύτταρα σπονδυλωτών η παρεμβολή RNA δεν αντικαταστάθηκε πλέον πολύπλοκα συστήματαανοσία, αλλά εξελίχθηκε μαζί με τους οργανισμούς, μετατρέποντας σε κάτι πιο «προηγμένο». Κατά συνέπεια, στα θηλαστικά ήταν απαραίτητο να αναζητηθούν όχι ακριβή ανάλογα των siRNAs, αλλά για τους εξελικτικούς διαδόχους τους.
Παίκτης #2 - microRNA
Πράγματι, με βάση τον εξελικτικά αρκετά αρχαίο μηχανισμό της παρεμβολής RNA, εμφανίστηκαν δύο εξειδικευμένα συστήματα για τον έλεγχο της λειτουργίας των γονιδίων σε πιο ανεπτυγμένους οργανισμούς, ο καθένας χρησιμοποιώντας τη δική του ομάδα μικρών RNA - microRNA(microRNA) και piRNA(piRNA, Piwi-αλληλεπιδρών RNA). Και τα δύο συστήματα εμφανίστηκαν σε σφουγγάρια και συνεντερικά και εξελίχθηκαν μαζί με αυτά, εκτοπίζοντας το siRNA και τον μηχανισμό της «γυμνής» παρεμβολής RNA. Ο ρόλος τους στην παροχή ανοσίας μειώνεται, αφού αυτή τη λειτουργία έχουν αναλάβει πιο προηγμένοι μηχανισμοί κυτταρικής ανοσίας, ιδίως το σύστημα ιντερφερόνης. Ωστόσο, αυτό το σύστημα είναι τόσο ευαίσθητο που ενεργοποιεί και το ίδιο το siRNA: η εμφάνιση μικρού δίκλωνου RNA σε ένα κύτταρο θηλαστικού ενεργοποιεί ένα «σήμα συναγερμού» (ενεργοποιεί την έκκριση ιντερφερόνης και προκαλεί την έκφραση γονιδίων που εξαρτώνται από την ιντερφερόνη, τα οποία μπλοκάρει πλήρως όλες τις μεταφραστικές διαδικασίες). Από αυτή την άποψη, ο μηχανισμός της παρεμβολής RNA σε ανώτερα ζώα διαμεσολαβείται κυρίως από microRNAs και piRNAs - μονόκλωνα μόρια με συγκεκριμένη δομή που δεν ανιχνεύονται από το σύστημα ιντερφερόνης.
Καθώς το γονιδίωμα γινόταν πιο πολύπλοκο, τα microRNA και τα piRNA εμπλέκονταν όλο και περισσότερο στη ρύθμιση της μεταγραφής και της μετάφρασης. Με τον καιρό, μετατράπηκαν σε ένα πρόσθετο, ακριβές και λεπτό σύστημα ρύθμισης του γονιδιώματος. Σε αντίθεση με το siRNA, το microRNA και το piRNA (που ανακαλύφθηκαν το 2001, βλέπε Πλαίσιο 3) δεν παράγονται από ξένα δίκλωνα μόρια RNA, αλλά κωδικοποιούνται αρχικά στο γονιδίωμα του ξενιστή.
Γνωρίστε: microRNA
Ο πρόδρομος microRNA μεταγράφεται και από τους δύο κλώνους του γονιδιωματικού DNA από την RNA πολυμεράση II, με αποτέλεσμα την εμφάνιση μιας ενδιάμεσης μορφής - pri-microRNA - που φέρει τα χαρακτηριστικά του συνηθισμένου mRNA - m 7 G-cap και polyA ουράς. Αυτός ο πρόδρομος σχηματίζει έναν βρόχο με δύο μονόκλωνες «ουρές» και πολλά μη ζευγαρωμένα νουκλεοτίδια στο κέντρο (Εικ. 3). Ένας τέτοιος βρόχος υφίσταται επεξεργασία δύο σταδίων (Εικ. 4): πρώτον, η ενδονουκλεάση Drosha κόβει τις μονόκλωνες «ουρές» RNA από τη φουρκέτα, μετά την οποία η αποκομμένη φουρκέτα (pre-microRNA) εξάγεται στο κυτταρόπλασμα, όπου αναγνωρίζεται από τον Dicer, ο οποίος κάνει δύο ακόμη τομές (ένα δίκλωνο τμήμα κόβεται , που υποδεικνύεται με χρώμα στο Σχ. 3). Σε αυτή τη μορφή, το ώριμο microRNA, παρόμοιο με το siRNA, περιλαμβάνεται στο σύμπλεγμα RISC.
Εικόνα 3. Δομή ενός δίκλωνου μορίου πρόδρομου microRNA.Κύρια χαρακτηριστικά: η παρουσία διατηρημένων ακολουθιών που σχηματίζουν μια φουρκέτα. την παρουσία ενός συμπληρωματικού αντιγράφου (microRNA*) με δύο «επιπλέον» νουκλεοτίδια στο άκρο 3'. μια συγκεκριμένη αλληλουχία (2–8 bp) που σχηματίζει μια θέση αναγνώρισης για τις ενδονουκλεάσες. Το ίδιο το microRNA επισημαίνεται με κόκκινο χρώμα - αυτό αποκόπτει το Dicer.
Ο μηχανισμός δράσης πολλών microRNA είναι παρόμοιος με τη δράση των siRNA: ένα βραχύ (21-25 νουκλεοτίδια) μονόκλωνο RNA ως μέρος του συμπλέγματος πρωτεϊνών RISC συνδέεται με υψηλή εξειδίκευση στη συμπληρωματική θέση στην 3' αμετάφραστη περιοχή του mRNA στόχου. Η δέσμευση οδηγεί στη διάσπαση του mRNA από την πρωτεΐνη Ago. Ωστόσο, η δραστηριότητα του microRNA (σε σύγκριση με το siRNA) είναι ήδη πιο διαφοροποιημένη - εάν η συμπληρωματικότητα δεν είναι απόλυτη, το mRNA στόχος μπορεί να μην αποικοδομηθεί, αλλά να αποκλειστεί μόνο αναστρέψιμα (δεν θα υπάρξει μετάφραση). Μπορεί επίσης να χρησιμοποιηθεί το ίδιο σύμπλεγμα RISC εισήχθη τεχνητά siRNA. Αυτό εξηγεί γιατί τα siRNAs που παράγονται κατ' αναλογία με τα πρωτόζωα είναι επίσης ενεργά στα θηλαστικά.
Έτσι, μπορούμε να συμπληρώσουμε την απεικόνιση του μηχανισμού δράσης της παρεμβολής RNA σε ανώτερους (αμφίπλευρα συμμετρικούς) οργανισμούς συνδυάζοντας σε ένα σχήμα το διάγραμμα δράσης των microRNAs και των βιοτεχνολογικά εισαγόμενων siRNAs (Εικ. 5).

Εικόνα 5. Γενικευμένο σχήμα δράσης τεχνητών microRNA και siRNA(τεχνητά siRNA εισάγονται στο κύτταρο χρησιμοποιώντας εξειδικευμένα πλασμίδια - στόχευση φορέα siRNA).
Λειτουργίες του microRNA
Οι φυσιολογικές λειτουργίες των microRNA είναι εξαιρετικά διαφορετικές - στην πραγματικότητα, λειτουργούν ως οι κύριοι μη πρωτεϊνικοί ρυθμιστές της οντογένεσης. Τα microRNA δεν ακυρώνουν, αλλά συμπληρώνουν το «κλασικό» σχήμα γονιδιακής ρύθμισης (επαγωγείς, καταστολείς, συμπίεση χρωματίνης κ.λπ.). Επιπλέον, η σύνθεση των ίδιων των microRNAs ρυθμίζεται πολύπλοκα (ορισμένες δεξαμενές microRNA μπορούν να ενεργοποιηθούν από ιντερφερόνες, ιντερλευκίνες, παράγοντα νέκρωσης όγκου α (TNF-α) και πολλές άλλες κυτοκίνες). Ως αποτέλεσμα, αναδύεται ένα πολυεπίπεδο δίκτυο συντονισμού μιας «ορχήστρας» χιλιάδων γονιδίων, εκπληκτικό στην πολυπλοκότητα και την ευελιξία της, αλλά αυτό δεν τελειώνει εκεί.
Τα microRNA είναι πιο «καθολικά» από τα siRNA: τα γονίδια «θάλαμος» δεν χρειάζεται να είναι 100% συμπληρωματικά - η ρύθμιση πραγματοποιείται επίσης μέσω μερικής αλληλεπίδρασης. Σήμερα ένα από τα πιο καυτά θέματα ΜΟΡΙΑΚΗ ΒΙΟΛΟΓΙΑ- αναζήτηση για microRNA που λειτουργούν ως εναλλακτικοί ρυθμιστές γνωστών φυσιολογικών διεργασιών. Για παράδειγμα, τα microRNA που εμπλέκονται στη ρύθμιση του κυτταρικού κύκλου και της απόπτωσης σε φυτά, Drosophila και νηματώδεις έχουν ήδη περιγραφεί. στους ανθρώπους, τα microRNA ρυθμίζουν το ανοσοποιητικό σύστημα και την ανάπτυξη αιμοποιητικών βλαστοκυττάρων. Η χρήση τεχνολογιών που βασίζονται σε βιοτσίπ (διαλογή μικροσυστοιχίας) έχει δείξει ότι ολόκληρες δεξαμενές μικρών RNA ενεργοποιούνται και απενεργοποιούνται σε διαφορετικά στάδια της κυτταρικής ζωής. Για βιολογικές διεργασίεςεντόπισε δεκάδες συγκεκριμένα microRNA, το επίπεδο έκφρασης των οποίων υπό ορισμένες συνθήκες αλλάζει χιλιάδες φορές, τονίζοντας την εξαιρετική δυνατότητα ελέγχου αυτών των διεργασιών.
Μέχρι πρόσφατα, πίστευαν ότι τα microRNA καταστέλλουν μόνο - πλήρως ή εν μέρει - το έργο των γονιδίων. Ωστόσο, πρόσφατα αποδείχθηκε ότι η δράση των microRNA μπορεί να διαφέρει ριζικά ανάλογα με την κατάσταση του κυττάρου! Σε ένα ενεργά διαιρούμενο κύτταρο, το microRNA συνδέεται με μια συμπληρωματική αλληλουχία στην περιοχή 3' του mRNA και αναστέλλει την πρωτεϊνική σύνθεση (μετάφραση). Ωστόσο, σε κατάσταση ανάπαυσης ή στρες (για παράδειγμα, όταν μεγαλώνετε σε φτωχό περιβάλλον), το ίδιο γεγονός οδηγεί στο ακριβώς αντίθετο αποτέλεσμα - αυξημένη σύνθεση της πρωτεΐνης στόχου!
Εξέλιξη του microRNA
Ο αριθμός των ποικιλιών microRNA σε ανώτερους οργανισμούς δεν έχει ακόμη πλήρως τεκμηριωθεί - σύμφωνα με ορισμένα δεδομένα, υπερβαίνει το 1% του αριθμού των γονιδίων που κωδικοποιούν πρωτεΐνες (στον άνθρωπο, για παράδειγμα, λένε ότι υπάρχουν 700 microRNA, και αυτός ο αριθμός είναι συνεχώς αυξάνεται). Τα microRNA ρυθμίζουν τη δραστηριότητα περίπου 30% όλων των γονιδίων (οι στόχοι για πολλά από αυτά δεν είναι ακόμη γνωστοί) και υπάρχουν τόσο πανταχού παρόντα όσο και ειδικά για τον ιστό μόρια - για παράδειγμα, μια τέτοια σημαντική δεξαμενή microRNA ρυθμίζει την ωρίμανση του στελέχους του αίματος κύτταρα.
Ευρύ προφίλ έκφρασης σε διαφορετικούς ιστούς διαφορετικούς οργανισμούςκαι η βιολογική αφθονία των microRNA υποδηλώνει μια εξελικτικά αρχαία προέλευση. Τα MicroRNAs ανακαλύφθηκαν για πρώτη φορά σε νηματώδεις και για μεγάλο χρονικό διάστημα πίστευαν ότι αυτά τα μόρια εμφανίζονται μόνο σε σφουγγάρια και συνεντερικά. Ωστόσο, αργότερα ανακαλύφθηκαν σε μονοκύτταρα φύκια. Είναι ενδιαφέρον ότι καθώς οι οργανισμοί γίνονται πιο περίπλοκοι, ο αριθμός και η ετερογένεια της δεξαμενής miRNA αυξάνεται επίσης. Αυτό δείχνει έμμεσα ότι η πολυπλοκότητα αυτών των οργανισμών παρέχεται, ειδικότερα, από τη λειτουργία των microRNAs. Η πιθανή εξέλιξη των miRNAs φαίνεται στο Σχήμα 6.

Εικόνα 6. Ποικιλότητα MicroRNA σε διαφορετικούς οργανισμούς.Όσο υψηλότερη είναι η οργάνωση του οργανισμού, τόσο περισσότερα microRNA βρίσκονται σε αυτόν (ο αριθμός σε παρένθεση). Τα είδη στα οποία βρέθηκαν επισημαίνονται με κόκκινο χρώμα. μονόκλινο microRNA.
Μια σαφής εξελικτική σύνδεση μπορεί να γίνει μεταξύ του siRNA και του microRNA, με βάση τα ακόλουθα γεγονότα:
- Η δράση και των δύο τύπων είναι εναλλάξιμη και μεσολαβείται από ομόλογες πρωτεΐνες.
- Τα siRNA που εισάγονται σε κύτταρα θηλαστικών «απενεργοποιούν» ειδικά τα επιθυμητά γονίδια (παρά την ενεργοποίηση της προστασίας από ιντερφερόνη).
- microRNAs ανακαλύπτονται σε όλο και περισσότερους αρχαίους οργανισμούς.
Αυτά και άλλα δεδομένα υποδηλώνουν την προέλευση και των δύο συστημάτων από έναν κοινό «πρόγονο». Είναι επίσης ενδιαφέρον να σημειωθεί ότι η ανοσία «RNA» ως ανεξάρτητος πρόδρομος πρωτεϊνικών αντισωμάτων επιβεβαιώνει τη θεωρία της προέλευσης των πρώτων μορφών ζωής που βασίζονται στο RNA, και όχι στις πρωτεΐνες (υπενθυμίζουμε ότι αυτή είναι η αγαπημένη θεωρία του Ακαδημαϊκού A.S. Spirin) .
Όσο προχωράτε, τόσο πιο μπερδεμένο γίνεται. Παίκτης #3 - piRNA
Ενώ υπήρχαν μόνο δύο «παίκτες» στην αρένα της μοριακής βιολογίας - το siRNA και το microRNA - ο κύριος «σκοπός» της παρεμβολής RNA φαινόταν εντελώς ξεκάθαρος. Πράγματι: ένα σύνολο ομόλογων βραχέων RNA και πρωτεϊνών σε διαφορετικούς οργανισμούς πραγματοποιεί παρόμοιες δράσεις. Καθώς οι οργανισμοί γίνονται πιο περίπλοκοι, το ίδιο συμβαίνει και με τη λειτουργικότητα.
Ωστόσο, στη διαδικασία της εξέλιξης, η φύση δημιούργησε ένα άλλο, εξελικτικά πιο πρόσφατο και εξαιρετικά εξειδικευμένο σύστημα που βασίζεται στην ίδια επιτυχημένη αρχή της παρεμβολής RNA. Μιλάμε για piRNA (piRNA, από RNA αλληλεπίδρασης Piwi).
Όσο πιο πολύπλοκο είναι το γονιδίωμα, τόσο πιο ανεπτυγμένος και προσαρμοσμένος είναι ο οργανισμός (ή το αντίστροφο; ;-). Ωστόσο, η αύξηση της πολυπλοκότητας του γονιδιώματος έχει επίσης ένα μειονέκτημα: γίνεται ένα πολύπλοκο γενετικό σύστημα ασταθής. Αυτό οδηγεί στην ανάγκη για μηχανισμούς υπεύθυνους για τη διατήρηση της ακεραιότητας του γονιδιώματος - διαφορετικά η αυθόρμητη «ανάμιξη» του DNA απλώς θα το απενεργοποιήσει. Κινητά γενετικά στοιχεία ( MGE) - ένας από τους κύριους παράγοντες αστάθειας του γονιδιώματος - είναι μικρές ασταθείς περιοχές που μπορούν να μεταγραφούν αυτόνομα και να μεταναστεύσουν σε όλο το γονιδίωμα. Η ενεργοποίηση τέτοιων μετατιθέμενων στοιχείων οδηγεί σε πολλαπλές θραύσεις του DNA στα χρωμοσώματα, που μπορεί να έχουν θανατηφόρες συνέπειες.
Ο αριθμός των MGE αυξάνεται μη γραμμικά με το μέγεθος του γονιδιώματος και η δραστηριότητά τους πρέπει να περιορίζεται. Για να γίνει αυτό, τα ζώα, ξεκινώντας από συνεντερικά, χρησιμοποιούν το ίδιο φαινόμενο παρεμβολής RNA. Αυτή η λειτουργία εκτελείται επίσης από μικρά RNA, αλλά όχι αυτά που έχουν ήδη συζητηθεί, αλλά ένας τρίτος τύπος αυτών - τα piRNA.
«Πορτρέτο» του piRNA
Λειτουργίες του piRNA
Η κύρια λειτουργία του piRNA είναι να καταστέλλει τη δραστηριότητα MGE στο επίπεδο της μεταγραφής και της μετάφρασης. Πιστεύεται ότι τα piRNA είναι ενεργά μόνο κατά τη διάρκεια της εμβρυογένεσης, όταν η απρόβλεπτη ανακάτεμα του γονιδιώματος είναι ιδιαίτερα επικίνδυνη και μπορεί να οδηγήσει στο θάνατο του εμβρύου. Αυτό είναι λογικό - όταν το ανοσοποιητικό σύστημα δεν έχει αρχίσει ακόμη να λειτουργεί, τα κύτταρα του εμβρύου χρειάζονται κάποια απλή αλλά αποτελεσματική προστασία. Το έμβρυο προστατεύεται αξιόπιστα από εξωτερικά παθογόνα από τον πλακούντα (ή το κέλυφος του αυγού). Αλλά εκτός από αυτό, η άμυνα είναι επίσης απαραίτητη από ενδογενείς (εσωτερικούς) ιούς, κυρίως MGE.
Αυτός ο ρόλος του piRNA έχει επιβεβαιωθεί από την εμπειρία - «νοκ-άουτ» ή μεταλλάξεις των γονιδίων Ago3, Piwi ή Aub οδηγούν σε σοβαρές αναπτυξιακές διαταραχές (και απότομη αύξηση του αριθμού των μεταλλάξεων στο γονιδίωμα ενός τέτοιου οργανισμού) και επίσης προκαλούν υπογονιμότητα λόγω διακοπής της ανάπτυξης των γεννητικών κυττάρων.
Κατανομή και εξέλιξη των piRNAs
Τα πρώτα piRNA βρίσκονται ήδη σε θαλάσσιες ανεμώνες και σφουγγάρια. Τα φυτά προφανώς ακολούθησαν διαφορετική διαδρομή - πρωτεΐνες Piwi δεν βρέθηκαν σε αυτά και ο ρόλος ενός "μυγχώματος" για τρανσποζόνια εκτελείται από την ενδονουκλεάση Ago4 και το siRNA.
Στα ανώτερα ζώα - συμπεριλαμβανομένων των ανθρώπων - το σύστημα piRNA είναι πολύ καλά ανεπτυγμένο, αλλά μπορεί να βρεθεί μόνο σε εμβρυϊκά κύτταρα και στο αμνιακό ενδοθήλιο. Γιατί η κατανομή του piRNA στο σώμα είναι τόσο περιορισμένη μένει να φανεί. Μπορεί να υποτεθεί ότι, όπως κάθε ισχυρό όπλο, τα piRNA είναι ωφέλιμα μόνο υπό πολύ συγκεκριμένες συνθήκες (κατά την ανάπτυξη του εμβρύου) και στον ενήλικο οργανισμό η δραστηριότητά τους θα προκαλέσει περισσότερο κακό παρά καλό. Ακόμα, ο αριθμός των piRNAs είναι μια τάξη μεγέθους μεγαλύτερος από τον αριθμό των γνωστών πρωτεϊνών και οι μη ειδικές επιδράσεις των piRNA στα ώριμα κύτταρα είναι δύσκολο να προβλεφθούν.
| siRNA | microRNA | piRNA | |
|---|---|---|---|
| Διάδοση | Φυτά, Δροσοφίλα, C. elegans. Δεν βρίσκεται σε σπονδυλωτά | Ευκαρυωτες | Εμβρυικά κύτταρα ζώων (ξεκινώντας από συνεντερικά). Όχι σε πρωτόζωα και φυτά |
| Μήκος | 21-22 νουκλεοτίδια | 19-25 νουκλεοτίδια | 24–30 νουκλεοτίδια |
| Δομή | Δίκλωνα, 19 συμπληρωματικά νουκλεοτίδια και δύο μη ζευγαρωμένα νουκλεοτίδια στο άκρο 3' | Σύνθετη δομή μονής αλυσίδας | Σύνθετη δομή μονής αλυσίδας. U στο 5′ τέλος, 2′ τέλος Ο-μεθυλιωμένο 3′ άκρο |
| Επεξεργασία | Dicer-εξαρτώμενος | Dicer-εξαρτώμενος | Dicer-ανεξάρτητος |
| Ενδονουκλεάσες | Ago2 | Ago1, Ago2 | Ago3, Piwi, Aub |
| Δραστηριότητα | Αποικοδόμηση συμπληρωματικών mRNA, ακετυλίωση γονιδιωματικού DNA | Αποικοδόμηση ή αναστολή της μετάφρασης του mRNA στόχου | Αποικοδόμηση mRNA που κωδικοποιεί MGE, ρύθμιση μεταγραφής MGE |
| Βιολογικός ρόλος | Αντιϊκή ανοσολογική άμυνα, καταστολή της δραστηριότητας των δικών του γονιδίων | Ρύθμιση της γονιδιακής δραστηριότητας | Καταστολή της δραστηριότητας MGE κατά την εμβρυογένεση |
συμπέρασμα
Εν κατακλείδι, θα ήθελα να παράσχω έναν πίνακα που απεικονίζει την εξέλιξη της συσκευής πρωτεΐνης που εμπλέκεται στην παρεμβολή RNA (Εικ. 9). Μπορεί να φανεί ότι τα πρωτόζωα έχουν το πιο ανεπτυγμένο σύστημα siRNA (οικογένειες πρωτεϊνών Ago, Dicer) και καθώς οι οργανισμοί γίνονται πιο πολύπλοκοι, η έμφαση μετατοπίζεται σε πιο εξειδικευμένα συστήματα - τον αριθμό των ισομορφών πρωτεΐνης για microRNA (Drosha, Pasha) και piRNA ( Piwi, Hen1) αυξάνεται. Ταυτόχρονα, μειώνεται η ποικιλία των ενζύμων που μεσολαβούν στη δράση του siRNA.

Εικόνα 9. Ποικιλομορφία πρωτεϊνών που εμπλέκονται στην παρεμβολή RNA(οι αριθμοί δείχνουν τον αριθμό των πρωτεϊνών κάθε ομάδας). Μπλεεπισημαίνονται στοιχεία που είναι χαρακτηριστικά του siRNA και του microRNA και το κόκκινο- πρωτεΐνη Καιπου σχετίζονται με το piRNA.
Το φαινόμενο της παρεμβολής RNA άρχισε να χρησιμοποιείται από τους πιο απλούς οργανισμούς. Με βάση αυτόν τον μηχανισμό, η φύση δημιούργησε ένα πρωτότυπο ανοσοποιητικό σύστημακαι καθώς οι οργανισμοί γίνονται πιο περίπλοκοι, η παρεμβολή RNA γίνεται απαραίτητος ρυθμιστής της δραστηριότητας του γονιδιώματος. Δύο διαφορετικοί μηχανισμοί συν τρεις τύποι βραχέων RNA ( εκ.αυτί. 1) - ως αποτέλεσμα, βλέπουμε χιλιάδες λεπτούς ρυθμιστές διαφόρων μεταβολικών και γενετικών οδών. Αυτή η εντυπωσιακή εικόνα απεικονίζει την ευελιξία και την εξελικτική προσαρμογή των μοριακών βιολογικά συστήματα. Τα σύντομα RNA αποδεικνύουν και πάλι ότι δεν υπάρχουν «μικρά πράγματα» μέσα στο κύτταρο - υπάρχουν μόνο μικρά μόρια, την πλήρη σημασία του ρόλου των οποίων μόλις αρχίζουμε να καταλαβαίνουμε.
(Αλήθεια, μια τέτοια φανταστική πολυπλοκότητα υποδηλώνει μάλλον ότι η εξέλιξη είναι «τυφλή» και δρα χωρίς προεγκεκριμένο» Κύριο σχέδιο» »;
Η μεταφορά στην οποία βασίζεται το όνομα του φαινομένου παρεμβολής RNA αναφέρεται στο πείραμα με την πετούνια, όταν τα γονίδια συνθετάσης ροζ και μοβ χρωστικής χρωστικής που εισήχθησαν τεχνητά στο φυτό δεν αύξησαν την ένταση του χρώματος, αλλά, αντίθετα, τη μείωσαν. Ομοίως, σε «συνηθισμένη» παρεμβολή, η υπέρθεση δύο κυμάτων μπορεί να οδηγήσει σε αμοιβαία «ακύρωση».
Σε ένα ζωντανό κύτταρο, η ροή πληροφοριών μεταξύ του πυρήνα και του κυτταροπλάσματος δεν στεγνώνει ποτέ, αλλά η κατανόηση όλων των «στροβιλισμών» του και η αποκρυπτογράφηση των πληροφοριών που κωδικοποιούνται σε αυτό είναι πραγματικά μια ηράκλεια εργασία. Μια από τις πιο σημαντικές ανακαλύψεις στη βιολογία του περασμένου αιώνα μπορεί να θεωρηθεί η ανακάλυψη μορίων πληροφοριών (ή μήτρας) RNA (mRNA ή mRNA), τα οποία χρησιμεύουν ως ενδιάμεσοι μεταφέροντας «μηνύματα» πληροφοριών από τον πυρήνα (από τα χρωμοσώματα) στο κυτταρόπλασμα. . Ο καθοριστικός ρόλος του RNA στη σύνθεση πρωτεϊνών είχε προβλεφθεί το 1939 στο έργο των Torbjörn Caspersson, Jean Brachet και Jack Schultz και το 1971 ο George Marbaix ξεκίνησε τη σύνθεση της αιμοσφαιρίνης σε ωοκύτταρα βατράχια με έγχυση του αγγελιοφόρου κουνελιού RNA για την κωδικοποίηση αυτής της πρωτεΐνης. πρώτη φορά.
Το 1956-57 στη Σοβιετική Ένωση, ο A. N. Belozersky και ο A. S. Spirin απέδειξαν ανεξάρτητα την ύπαρξη mRNA και επίσης ανακάλυψαν ότι το μεγαλύτερο μέρος του RNA σε ένα κύτταρο δεν είναι πρότυπο, αλλά ριβοσωμικό RNA (rRNA). Το ριβοσωμικό RNA, ο δεύτερος «κύριος» τύπος κυτταρικού RNA, σχηματίζει τον «σκελετό» και το λειτουργικό κέντρο των ριβοσωμάτων σε όλους τους οργανισμούς. Είναι το rRNA (και όχι οι πρωτεΐνες) που ρυθμίζει τα κύρια στάδια της πρωτεϊνοσύνθεσης. Ταυτόχρονα, περιγράφηκε και μελετήθηκε ο τρίτος «κύριος» τύπος RNA - τα RNA μεταφοράς (tRNA), τα οποία σε συνδυασμό με δύο άλλα - mRNA και rRNA - σχηματίζουν ένα ενιαίο σύμπλεγμα πρωτεϊνοσύνθεσης. Σύμφωνα με την αρκετά δημοφιλή υπόθεση του «κόσμου RNA», ήταν αυτό το νουκλεϊκό οξύ που βρισκόταν στην ίδια την αρχή της ζωής στη Γη.
Λόγω του γεγονότος ότι το RNA είναι πολύ πιο υδρόφιλο σε σύγκριση με το DNA (λόγω της αντικατάστασης της δεοξυριβόζης με ριβόζη), είναι πιο ασταθές και μπορεί να κινείται σχετικά ελεύθερα στο κύτταρο, και επομένως παρέχει βραχύβια αντίγραφα γενετικής πληροφορίας (mRNA). στο μέρος όπου αρχίζει η πρωτεϊνοσύνθεση. Ωστόσο, αξίζει να σημειωθεί η "ταλαιπωρία" που σχετίζεται με αυτό - το RNA είναι πολύ ασταθές. Αποθηκεύεται πολύ χειρότερα από το DNA (ακόμη και μέσα σε ένα κύτταρο) και υποβαθμίζεται με την παραμικρή αλλαγή των συνθηκών (θερμοκρασία, pH). Εκτός από τη «δική» αστάθεια, μια μεγάλη συνεισφορά ανήκει στις ριβονουκλεάσες (ή RNases) - μια κατηγορία ενζύμων διάσπασης RNA που είναι πολύ σταθερά και «πανταχού παρόντα» - ακόμη και το δέρμα των χεριών του πειραματιστή περιέχει αρκετά από αυτά τα ένζυμα για να τα αρνηθεί. ολόκληρο το πείραμα. Εξαιτίας αυτού, η εργασία με RNA είναι πολύ πιο δύσκολη από ό,τι με πρωτεΐνες ή DNA - το τελευταίο μπορεί γενικά να αποθηκευτεί για εκατοντάδες χιλιάδες χρόνια χωρίς ουσιαστικά καμία ζημιά.
Φανταστική φροντίδα κατά τη διάρκεια της εργασίας, τριαπόσταγμα, αποστειρωμένα γάντια, εργαστηριακά γυάλινα σκεύη μιας χρήσης - όλα αυτά είναι απαραίτητα για την πρόληψη της υποβάθμισης του RNA, αλλά η διατήρηση τέτοιων προτύπων δεν ήταν πάντα δυνατή. Ως εκ τούτου, για μεγάλο χρονικό διάστημα, απλά δεν έδωσαν προσοχή σε μικρά «θραύσματα» RNA, τα οποία αναπόφευκτα μόλυναν διαλύματα. Ωστόσο, με την πάροδο του χρόνου, κατέστη σαφές ότι, παρά όλες τις προσπάθειες να διατηρηθεί η στειρότητα της περιοχής εργασίας, συνέχισαν φυσικά να ανακαλύπτονται «συντρίμμια» και στη συνέχεια αποδείχθηκε ότι χιλιάδες βραχέων δίκλωνων RNAs υπάρχουν πάντα στο κυτταρόπλασμα , εκτελώντας πολύ συγκεκριμένες λειτουργίες και είναι απολύτως απαραίτητες για τη φυσιολογική ανάπτυξη των κυττάρων και του οργανισμού.
Αρχή της παρεμβολής RNA
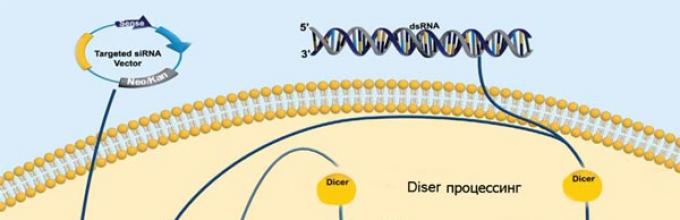
Σήμερα, η μελέτη των μικρών ρυθμιστικών RNA είναι ένας από τους πιο ταχέως αναπτυσσόμενους τομείς της μοριακής βιολογίας. Ανακαλύφθηκε ότι όλα τα βραχέα RNA εκτελούν τις λειτουργίες τους με βάση ένα φαινόμενο που ονομάζεται παρεμβολή RNA (η ουσία αυτού του φαινομένου είναι η καταστολή της γονιδιακής έκφρασης στο στάδιο της μεταγραφής ή της μετάφρασης με την ενεργό συμμετοχή μικρών μορίων RNA). Ο μηχανισμός της παρεμβολής RNA φαίνεται πολύ σχηματικά στο Σχήμα 1:
Ρύζι. 1. Βασικές αρχές παρεμβολής RNA
Τα μόρια δίκλωνου RNA (dsRNA) είναι ασυνήθιστα σε φυσιολογικά κύτταρα, αλλά αποτελούν ουσιαστικό βήμα στον κύκλο ζωής πολλών ιών. Μια ειδική πρωτεΐνη που ονομάζεται Dicer, έχοντας ανιχνεύσει dsRNA στο κύτταρο, το «κόβει» σε μικρά θραύσματα. Ο αντιπληροφοριακός κλώνος ενός τέτοιου θραύσματος, το οποίο μπορεί ήδη να ονομαστεί βραχύ παρεμβαλλόμενο RNA (siRNA, από το siRNA - RNA μικρής παρεμβολής), δεσμεύεται από ένα σύμπλεγμα πρωτεϊνών που ονομάζεται RISC (σύμπλεγμα σιγής που προκαλείται από RNA), το κεντρικό στοιχείο του οποίου είναι μια ενδονουκλεάση της οικογένειας των Αργοναυτών. Η σύνδεση με το siRNA ενεργοποιεί το RISC και ενεργοποιεί μια αναζήτηση στο κύτταρο για μόρια DNA και RNA που είναι συμπληρωματικά με το «πρότυπο» siRNA. Η μοίρα τέτοιων μορίων είναι να καταστραφούν ή να αδρανοποιηθούν από το σύμπλεγμα RISC.
Συνοψίζοντας, σύντομες «περικοπές» ξένου (συμπεριλαμβανομένου σκόπιμα εισαγόμενου) δίκλωνου RNA χρησιμεύουν ως «πρότυπο» για μια μεγάλης κλίμακας αναζήτηση και καταστροφή του συμπληρωματικού mRNA (και αυτό ισοδυναμεί με καταστολή της έκφρασης του αντίστοιχου γονιδίου) , όχι μόνο σε ένα κελί, αλλά και σε γειτονικά. Για πολλούς οργανισμούς -πρωτόζωα, μαλάκια, σκουλήκια, έντομα, φυτά- αυτό το φαινόμενο είναι ένας από τους κύριους τρόπους άμυνας του ανοσοποιητικού έναντι των λοιμώξεων.
Το 2006, ο Andrew Fire και ο Craig Mello έλαβαν βραβείο Νόμπελστη Φυσιολογία και την Ιατρική «Για την ανακάλυψη του φαινομένου της παρεμβολής RNA - ο μηχανισμός της γονιδιακής σίγησης με τη συμμετοχή του dsRNA». Αν και το ίδιο το φαινόμενο της παρεμβολής RNA είχε περιγραφεί πολύ πριν (στις αρχές της δεκαετίας του 1980), ήταν έργο των Fire και Mello στο γενικό περίγραμμαπροσδιόρισε τον ρυθμιστικό μηχανισμό των μικρών RNA και σκιαγράφησε μια άγνωστη μέχρι τώρα περιοχή μοριακής έρευνας. Εδώ είναι τα κύρια αποτελέσματα της δουλειάς τους:
- Κατά τη διάρκεια της παρεμβολής RNA, είναι το mRNA (και κανένα άλλο) που διασπάται.
- Το δίκλωνο RNA δρα (προκαλεί διάσπαση) πολύ πιο αποτελεσματικά από το μονόκλωνο RNA. Αυτές οι δύο παρατηρήσεις προέβλεψαν την ύπαρξη ενός εξειδικευμένου συστήματος που μεσολαβεί στη δράση του dsRNA.
- Το dsRNA, συμπληρωματικό σε ένα τμήμα ώριμου mRNA, προκαλεί διάσπαση του τελευταίου. Αυτό έδειξε τον κυτταροπλασματικό εντοπισμό της διαδικασίας και την παρουσία μιας ειδικής ενδονουκλεάσης.
- Μια μικρή ποσότητα dsRNA (πολλά μόρια ανά κύτταρο) αρκεί για να «απενεργοποιήσει» πλήρως το γονίδιο στόχο, γεγονός που υποδηλώνει την ύπαρξη ενός μηχανισμού καταρράκτη κατάλυσης ή/και ενίσχυσης.
Αυτά τα αποτελέσματα έθεσαν τα θεμέλια για έναν ολόκληρο τομέα της σύγχρονης μοριακής βιολογίας - την παρεμβολή RNA - και καθόρισαν τον φορέα εργασίας πολλών ερευνητικών ομάδων σε όλο τον κόσμο για δεκαετίες. Μέχρι σήμερα, έχουν ανακαλυφθεί τρεις μεγάλες ομάδες μικρών RNA που παίζουν στο μοριακό πεδίο ως «ομάδα παρεμβολής RNA». Ας τους γνωρίσουμε πιο αναλυτικά.
Παίκτης #1 – σύντομο παρεμβαλλόμενο RNA
Η εξειδίκευση της παρεμβολής RNA προσδιορίζεται από βραχύ παρεμβαλλόμενο RNA (siRNA) - μικρά δίκλωνα μόρια RNA με σαφώς καθορισμένη δομή (βλ. Εικ. 2).
Τα siRNA είναι τα πιο πρώιμα στην εξέλιξη και είναι πιο διαδεδομένα στα φυτά, στους μονοκύτταρους οργανισμούς και στα ασπόνδυλα. Στα σπονδυλωτά, πρακτικά δεν ανευρίσκονται κανονικά siRNA, επειδή αντικαταστάθηκαν από μεταγενέστερα «μοντέλα» βραχέων RNA (βλ. παρακάτω).
Το siRNA - «πρότυπα» για αναζήτηση στο κυτταρόπλασμα και καταστροφή μορίων mRNA - έχουν μήκος 20-25 νουκλεοτίδια και ένα «ειδικό χαρακτηριστικό»: 2 μη ζευγαρωμένα νουκλεοτίδια στα άκρα 3' και φωσφορυλιωμένα άκρα 5'. Το αντιπληροφοριακό siRNA είναι ικανό (όχι φυσικά από μόνο του, αλλά με τη βοήθεια του συμπλέγματος RISC) να αναγνωρίσει το mRNA και συγκεκριμένα να προκαλέσει την αποδόμησή του: το mRNA στόχος κόβεται στην ακριβή θέση συμπληρωματικά προς το 10ο και το 11ο νουκλεοτίδιο του αντιπληροφοριακή αλυσίδα siRNA.

Ρύζι. 2. Μηχανισμός «παρεμβολής» μεταξύ mRNA και siRNA
Τα «παρεμβαλλόμενα» βραχέα μόρια RNA μπορούν είτε να εισέλθουν στο κύτταρο από το εξωτερικό είτε να «κοπούν» στη θέση τους από μακρύτερο δίκλωνο RNA. Η κύρια πρωτεΐνη που απαιτείται για την κοπή του dsRNA είναι η ενδονουκλεάση Dicer. Η «απενεργοποίηση» του γονιδίου μέσω του μηχανισμού παρεμβολής πραγματοποιείται από το siRNA μαζί με το σύμπλεγμα πρωτεϊνών RISC, το οποίο αποτελείται από τρεις πρωτεΐνες - την ενδονουκλεάση Ago2 και δύο βοηθητικές πρωτεΐνες PACT και TRBP. Αργότερα ανακαλύφθηκε ότι τα σύμπλοκα Dicer και RISC μπορούν να χρησιμοποιήσουν ως «σπόρο» όχι μόνο dsRNA, αλλά και μονόκλωνο RNA που σχηματίζει μια δίκλωνη φουρκέτα, καθώς και έτοιμο siRNA (το τελευταίο παρακάμπτει την «κοπή» στάδιο και συνδέεται αμέσως με το RISC).
Οι λειτουργίες των siRNA στα κύτταρα ασπόνδυλων είναι αρκετά διαφορετικές. Το πρώτο και κύριο πράγμα είναι η ανοσολογική προστασία. Το «παραδοσιακό» ανοσοποιητικό σύστημα (λεμφοκύτταρα + λευκοκύτταρα + μακροφάγα) υπάρχει μόνο σε σύμπλοκα πολυκύτταροι οργανισμοί. Στους μονοκύτταρους οργανισμούς, τα ασπόνδυλα και τα φυτά (που είτε δεν έχουν τέτοιο σύστημα είτε είναι στα σπάργανα), η ανοσολογική άμυνα βασίζεται στην παρεμβολή RNA. Η ανοσία που βασίζεται σε παρεμβολή RNA δεν απαιτεί πολύπλοκα όργανα «εκπαίδευσης» για πρόδρομους ανοσοκυττάρου (σπληνός, θύμος). Ταυτόχρονα, η ποικιλία των θεωρητικά πιθανών βραχέων αλληλουχιών RNA (421 παραλλαγές) συσχετίζεται με τον αριθμό των πιθανών πρωτεϊνικών αντισωμάτων ανώτερων ζώων. Επιπλέον, τα siRNA συντίθενται με βάση το «εχθρικό» RNA που έχει μολύνει το κύτταρο, πράγμα που σημαίνει ότι, σε αντίθεση με τα αντισώματα, «προσαρμόζονται» αμέσως για έναν συγκεκριμένο τύπο μόλυνσης. Και παρόλο που η προστασία που βασίζεται στην παρεμβολή RNA δεν λειτουργεί έξω από το κύτταρο (τουλάχιστον, δεν υπάρχουν ακόμη τέτοια δεδομένα), παρέχει ενδοκυτταρική ανοσία περισσότερο από ικανοποιητικά.
Πρώτα απ 'όλα, το siRNA δημιουργεί αντιϊκή ανοσία καταστρέφοντας το mRNA ή το γονιδιωματικό RNA μολυσματικών οργανισμών (για παράδειγμα, έτσι ανακαλύφθηκαν τα siRNA στα φυτά). Η εισαγωγή του ιικού RNA προκαλεί ισχυρή ενίσχυση συγκεκριμένων siRNA με βάση το μόριο εκκινητή - το ίδιο το ιικό RNA. Επιπλέον, τα siRNA καταστέλλουν την έκφραση διαφόρων κινητών γενετικών στοιχείων (MGEs) και ως εκ τούτου παρέχουν προστασία από ενδογενείς «λοιμώξεις». Οι μεταλλάξεις στα γονίδια του συμπλέγματος RISC συχνά οδηγούν σε αυξημένη αστάθεια του γονιδιώματος λόγω της υψηλής δραστηριότητας MGE. Το siRNA μπορεί να λειτουργήσει ως περιοριστής στην έκφραση των δικών του γονιδίων, ενεργοποιώντας ως απόκριση στην υπερέκφρασή τους. Η ρύθμιση της γονιδιακής λειτουργίας μπορεί να συμβεί όχι μόνο στο επίπεδο της μετάφρασης, αλλά και κατά τη διάρκεια της μεταγραφής - μέσω της μεθυλίωσης των γονιδίων στην ιστόνη H3.
Στη σύγχρονη πειραματική βιολογία, η σημασία της παρεμβολής RNA και των βραχέων RNA δύσκολα μπορεί να υπερεκτιμηθεί. Αναπτύχθηκε μια τεχνολογία για την «απενεργοποίηση» (ή την καταστροφή) μεμονωμένων γονιδίων in vitro (σε κυτταρικές καλλιέργειες) και in vivo (σε έμβρυα), η οποία έχει ήδη γίνει de facto πρότυπο κατά τη μελέτη οποιουδήποτε γονιδίου. Μερικές φορές, ακόμη και για να καθορίσουν τον ρόλο μεμονωμένων γονιδίων σε κάποια διαδικασία, «απενεργοποιούν» συστηματικά όλα τα γονίδια με τη σειρά τους.
Οι φαρμακοποιοί ενδιαφέρθηκαν επίσης για τη δυνατότητα χρήσης του siRNA, καθώς η ικανότητα να ρυθμίζεται ειδικά η λειτουργία μεμονωμένων γονιδίων υπόσχεται πρωτόγνωρες προοπτικές στη θεραπεία μιας σειράς ασθενειών. Το μικρό μέγεθος και η υψηλή ειδικότητα δράσης υπόσχονται υψηλή αποτελεσματικότητα και χαμηλή τοξικότητα των φαρμάκων που βασίζονται σε siRNA. Ωστόσο, δεν έχει καταστεί ακόμη δυνατό να λυθεί το πρόβλημα της παροχής siRNA σε άρρωστα κύτταρα στο σώμα - αυτό οφείλεται στην ευθραυστότητα και την ευθραυστότητα αυτών των μορίων. Και παρόλο που δεκάδες ομάδες προσπαθούν τώρα να βρουν έναν τρόπο να κατευθύνουν αυτές τις «μαγικές σφαίρες» ακριβώς στον στόχο (μέσα σε άρρωστα όργανα), δεν έχουν ακόμη επιτύχει ορατή επιτυχία. Εκτός από αυτό, υπάρχουν και άλλες δυσκολίες. Για παράδειγμα, στην περίπτωση της αντιιικής θεραπείας, η υψηλή επιλεκτικότητα της δράσης του siRNA μπορεί να είναι κακό - καθώς οι ιοί μεταλλάσσονται γρήγορα, το τροποποιημένο στέλεχος θα χάσει πολύ γρήγορα την ευαισθησία στο siRNA που επιλέχθηκε στην αρχή της θεραπείας: είναι γνωστό ότι Η αντικατάσταση ενός μόνο νουκλεοτιδίου στο siRNA οδηγεί σε σημαντική μείωση της επίδρασης παρεμβολής.
Σε αυτό το σημείο αξίζει να θυμηθούμε για άλλη μια φορά - τα siRNA βρέθηκαν μόνο σε φυτά, ασπόνδυλα και μονοκύτταρους οργανισμούς. Αν και ομόλογα πρωτεϊνών για παρεμβολή RNA (Dicer, σύμπλεγμα RISC) υπάρχουν επίσης σε ανώτερα ζώα, τα siRNA δεν ανιχνεύθηκαν με συμβατικές μεθόδους. Τι έκπληξη ήταν όταν εισήχθησαν τεχνητά συνθετικά ανάλογα siRNA προκάλεσαν μια ισχυρή ειδική δοσοεξαρτώμενη επίδραση σε καλλιέργειες κυττάρων θηλαστικών! Αυτό σήμαινε ότι στα κύτταρα των σπονδυλωτών, η παρεμβολή RNA δεν αντικαταστάθηκε από πιο πολύπλοκα ανοσοποιητικά συστήματα, αλλά εξελίχθηκε μαζί με τους οργανισμούς, μετατρέποντας σε κάτι πιο «προηγμένο». Κατά συνέπεια, στα θηλαστικά ήταν απαραίτητο να αναζητηθούν όχι ακριβή ανάλογα των siRNAs, αλλά για τους εξελικτικούς διαδόχους τους.
Παίκτης #2 – microRNA
Πράγματι, με βάση τον εξελικτικά αρχαίο μηχανισμό παρεμβολής RNA, πιο ανεπτυγμένοι οργανισμοί έχουν αναπτύξει δύο εξειδικευμένα συστήματα για τον έλεγχο της λειτουργίας των γονιδίων, το καθένα χρησιμοποιώντας τη δική του ομάδα μικρών RNAs - microRNA και piRNA (Piwi-interacting RNA). Και τα δύο συστήματα εμφανίστηκαν σε σφουγγάρια και συνεντερικά και εξελίχθηκαν μαζί με αυτά, εκτοπίζοντας το siRNA και τον μηχανισμό της «γυμνής» παρεμβολής RNA. Ο ρόλος τους στην παροχή ανοσίας μειώνεται, αφού αυτή τη λειτουργία έχουν αναλάβει πιο προηγμένοι μηχανισμοί κυτταρικής ανοσίας, ιδίως το σύστημα ιντερφερόνης. Ωστόσο, αυτό το σύστημα είναι τόσο ευαίσθητο που ενεργοποιεί και το ίδιο το siRNA: η εμφάνιση μικρού δίκλωνου RNA σε ένα κύτταρο θηλαστικού ενεργοποιεί ένα «σήμα συναγερμού» (ενεργοποιεί την έκκριση ιντερφερόνης και προκαλεί την έκφραση γονιδίων που εξαρτώνται από την ιντερφερόνη, τα οποία μπλοκάρει πλήρως όλες τις μεταφραστικές διαδικασίες). Από αυτή την άποψη, ο μηχανισμός της παρεμβολής RNA σε ανώτερα ζώα διαμεσολαβείται κυρίως από microRNAs και piRNAs - μονόκλωνα μόρια με συγκεκριμένη δομή που δεν ανιχνεύονται από το σύστημα ιντερφερόνης.
Καθώς το γονιδίωμα γινόταν πιο πολύπλοκο, τα microRNA και τα piRNA εμπλέκονταν όλο και περισσότερο στη ρύθμιση της μεταγραφής και της μετάφρασης. Με τον καιρό, μετατράπηκαν σε ένα πρόσθετο, ακριβές και λεπτό σύστημα ρύθμισης του γονιδιώματος. Σε αντίθεση με το siRNA, το microRNA και το piRNA (που ανακαλύφθηκαν το 2001, βλ. Εικ. 3, Α-Β) δεν παράγονται από ξένα δίκλωνα μόρια RNA, αλλά κωδικοποιούνται αρχικά στο γονιδίωμα του οργανισμού ξενιστή.
Ο πρόδρομος του microRNA μεταγράφεται και από τους δύο κλώνους του γονιδιωματικού DNA από την RNA πολυμεράση II, με αποτέλεσμα την εμφάνιση μιας ενδιάμεσης μορφής - pri-microRNA - που φέρει τα χαρακτηριστικά του κανονικού mRNA - m7G cap και polyA ουρά. Αυτός ο πρόδρομος σχηματίζει έναν βρόχο με δύο μονόκλωνες «ουρές» και πολλά μη ζευγαρωμένα νουκλεοτίδια στο κέντρο (Εικ. 3Α). Ένας τέτοιος βρόχος υφίσταται επεξεργασία δύο σταδίων (Εικ. Β): πρώτον, η ενδονουκλεάση Drosha αποκόπτει τις μονόκλωνες «ουρές» RNA από τη φουρκέτα, μετά την οποία η αποκομμένη φουρκέτα (pre-microRNA) εξάγεται στο κυτταρόπλασμα, όπου αναγνωρίζεται από τον Dicer, ο οποίος κάνει δύο ακόμη κοψίματα (ένα δίκλωνο τμήμα έχει αποκοπεί, χρωματική κωδικοποίηση στο Σχ. 3Α). Σε αυτή τη μορφή, το ώριμο microRNA, παρόμοιο με το siRNA, περιλαμβάνεται στο σύμπλεγμα RISC.
Ο μηχανισμός δράσης πολλών microRNA είναι παρόμοιος με τη δράση των siRNA: ένα βραχύ (21-25 νουκλεοτίδια) μονόκλωνο RNA ως μέρος του συμπλέγματος πρωτεϊνών RISC συνδέεται με υψηλή εξειδίκευση στη συμπληρωματική θέση στην 3'-αμετάφραστη περιοχή του το mRNA στόχο. Η δέσμευση οδηγεί στη διάσπαση του mRNA από την πρωτεΐνη Ago. Ωστόσο, η δραστηριότητα του microRNA (σε σύγκριση με το siRNA) είναι ήδη πιο διαφοροποιημένη - εάν η συμπληρωματικότητα δεν είναι απόλυτη, το mRNA στόχος μπορεί να μην αποικοδομηθεί, αλλά να αποκλειστεί μόνο αναστρέψιμα (δεν θα υπάρξει μετάφραση). Το ίδιο σύμπλεγμα RISC μπορεί επίσης να χρησιμοποιήσει τεχνητά εισαγόμενα siRNA. Αυτό εξηγεί γιατί τα siRNAs που παράγονται κατ' αναλογία με τα πρωτόζωα είναι επίσης ενεργά στα θηλαστικά.
Έτσι, μπορούμε να συμπληρώσουμε την απεικόνιση του μηχανισμού δράσης της παρεμβολής RNA σε ανώτερους (αμφίπλευρα συμμετρικούς) οργανισμούς συνδυάζοντας σε ένα σχήμα το διάγραμμα δράσης των microRNAs και των βιοτεχνολογικά εισαγόμενων siRNAs (Εικ. 3Β).
Ρύζι. 3Α: Δομή ενός δίκλωνου πρόδρομου μορίου microRNA
Κύρια χαρακτηριστικά: η παρουσία διατηρημένων ακολουθιών που σχηματίζουν μια φουρκέτα. την παρουσία ενός συμπληρωματικού αντιγράφου (microRNA*) με δύο "επιπλέον" νουκλεοτίδια στο 3' άκρο. μια συγκεκριμένη αλληλουχία (2–8 bp) που σχηματίζει μια θέση αναγνώρισης για τις ενδονουκλεάσες. Το ίδιο το microRNA επισημαίνεται με κόκκινο χρώμα - είναι αυτό που κόβει το Dicer.

Ρύζι. 3Β: Γενικός μηχανισμός επεξεργασίας microRNA και υλοποίηση της δραστηριότητάς του

Ρύζι. 3Β: Γενικευμένο σχήμα δράσης τεχνητών microRNA και siRNA
Τα τεχνητά siRNA εισάγονται στο κύτταρο χρησιμοποιώντας εξειδικευμένα πλασμίδια (στόχευση siRNA φορέα).
Λειτουργίες του microRNA
Οι φυσιολογικές λειτουργίες των microRNA είναι εξαιρετικά διαφορετικές - στην πραγματικότητα, λειτουργούν ως οι κύριοι μη πρωτεϊνικοί ρυθμιστές της οντογένεσης. Τα microRNA δεν ακυρώνουν, αλλά συμπληρώνουν το «κλασικό» σχήμα γονιδιακής ρύθμισης (επαγωγείς, καταστολείς, συμπίεση χρωματίνης κ.λπ.). Επιπλέον, η σύνθεση των ίδιων των microRNAs ρυθμίζεται πολύπλοκα (ορισμένες δεξαμενές microRNA μπορούν να ενεργοποιηθούν από ιντερφερόνες, ιντερλευκίνες, παράγοντα νέκρωσης όγκου α (TNF-α) και πολλές άλλες κυτοκίνες). Ως αποτέλεσμα, αναδύεται ένα πολυεπίπεδο δίκτυο συντονισμού μιας «ορχήστρας» χιλιάδων γονιδίων, εκπληκτικό στην πολυπλοκότητα και την ευελιξία της, αλλά αυτό δεν τελειώνει εκεί.
Τα microRNA είναι πιο «καθολικά» από τα siRNA: τα γονίδια «θάλαμος» δεν χρειάζεται να είναι 100% συμπληρωματικά - η ρύθμιση πραγματοποιείται επίσης μέσω μερικής αλληλεπίδρασης. Σήμερα, ένα από τα πιο καυτά θέματα στη μοριακή βιολογία είναι η αναζήτηση για microRNA που λειτουργούν ως εναλλακτικοί ρυθμιστές γνωστών φυσιολογικών διεργασιών. Για παράδειγμα, τα microRNA που εμπλέκονται στη ρύθμιση του κυτταρικού κύκλου και της απόπτωσης σε φυτά, Drosophila και νηματώδεις έχουν ήδη περιγραφεί. στους ανθρώπους, τα microRNA ρυθμίζουν το ανοσοποιητικό σύστημα και την ανάπτυξη αιμοποιητικών βλαστοκυττάρων. Η χρήση τεχνολογιών που βασίζονται σε βιοτσίπ (διαλογή μικροσυστοιχίας) έχει δείξει ότι ολόκληρες δεξαμενές μικρών RNA ενεργοποιούνται και απενεργοποιούνται σε διαφορετικά στάδια της κυτταρικής ζωής. Έχουν εντοπιστεί δεκάδες συγκεκριμένα microRNA για βιολογικές διεργασίες, το επίπεδο έκφρασης των οποίων υπό ορισμένες συνθήκες αλλάζει χιλιάδες φορές, δίνοντας έμφαση στην εξαιρετική δυνατότητα ελέγχου αυτών των διεργασιών.
Μέχρι πρόσφατα, πίστευαν ότι τα microRNA καταστέλλουν μόνο - πλήρως ή εν μέρει - το έργο των γονιδίων. Ωστόσο, πρόσφατα αποδείχθηκε ότι η δράση των microRNA μπορεί να διαφέρει ριζικά ανάλογα με την κατάσταση του κυττάρου! Σε ένα ενεργά διαιρούμενο κύτταρο, το microRNA συνδέεται με μια συμπληρωματική αλληλουχία στην περιοχή 3' του mRNA και αναστέλλει την πρωτεϊνική σύνθεση (μετάφραση). Ωστόσο, σε κατάσταση ανάπαυσης ή στρες (για παράδειγμα, όταν μεγαλώνετε σε φτωχό περιβάλλον), το ίδιο γεγονός οδηγεί στο ακριβώς αντίθετο αποτέλεσμα - αυξημένη σύνθεση της πρωτεΐνης στόχου!
Εξέλιξη του microRNA
Ο αριθμός των ποικιλιών microRNA σε ανώτερους οργανισμούς δεν έχει ακόμη πλήρως τεκμηριωθεί· σύμφωνα με ορισμένα δεδομένα, υπερβαίνει το 1% του αριθμού των γονιδίων που κωδικοποιούν πρωτεΐνες (στον άνθρωπο, για παράδειγμα, λένε ότι υπάρχουν 700 microRNA, και αυτός ο αριθμός είναι συνεχώς αυξάνεται). Τα microRNA ρυθμίζουν τη δραστηριότητα περίπου 30% όλων των γονιδίων (οι στόχοι για πολλά από αυτά δεν είναι ακόμη γνωστοί) και υπάρχουν τόσο πανταχού παρόντα όσο και ειδικά για τον ιστό μόρια - για παράδειγμα, μια τέτοια σημαντική δεξαμενή microRNA ρυθμίζει την ωρίμανση του στελέχους του αίματος κύτταρα.
Το ευρύ προφίλ έκφρασης σε διαφορετικούς ιστούς διαφορετικών οργανισμών και ο βιολογικός επιπολασμός των microRNA υποδηλώνουν μια εξελικτικά αρχαία προέλευση. Τα MicroRNAs ανακαλύφθηκαν για πρώτη φορά σε νηματώδεις και για μεγάλο χρονικό διάστημα πίστευαν ότι αυτά τα μόρια εμφανίζονται μόνο σε σφουγγάρια και συνεντερικά. Ωστόσο, αργότερα ανακαλύφθηκαν σε μονοκύτταρα φύκια. Είναι ενδιαφέρον ότι καθώς οι οργανισμοί γίνονται πιο περίπλοκοι, ο αριθμός και η ετερογένεια της δεξαμενής miRNA αυξάνεται επίσης. Αυτό δείχνει έμμεσα ότι η πολυπλοκότητα αυτών των οργανισμών παρέχεται, ειδικότερα, από τη λειτουργία των microRNAs. Η πιθανή εξέλιξη των miRNAs φαίνεται στην Εικ. 4.

Ρύζι. 4. Ποικιλομορφία microRNA σε διαφορετικούς οργανισμούς
Όσο υψηλότερη είναι η οργάνωση του οργανισμού, τόσο περισσότερα microRNA βρίσκονται σε αυτόν (ο αριθμός σε παρένθεση). Τα είδη στα οποία βρέθηκαν μεμονωμένα microRNA επισημαίνονται με κόκκινο χρώμα. Σύμφωνα με .
Μια σαφής εξελικτική σύνδεση μπορεί να γίνει μεταξύ του siRNA και του microRNA, με βάση τα ακόλουθα γεγονότα:
- Η δράση και των δύο τύπων είναι εναλλάξιμη και μεσολαβείται από ομόλογες πρωτεΐνες.
- Τα siRNA που εισάγονται σε κύτταρα θηλαστικών «απενεργοποιούν» ειδικά τα επιθυμητά γονίδια (παρά την ενεργοποίηση της προστασίας από ιντερφερόνη).
- microRNAs ανακαλύπτονται σε όλο και περισσότερους αρχαίους οργανισμούς.
Αυτά και άλλα δεδομένα υποδηλώνουν την προέλευση και των δύο συστημάτων από έναν κοινό «πρόγονο». Είναι επίσης ενδιαφέρον να σημειωθεί ότι η ανοσία «RNA» ως ανεξάρτητος πρόδρομος πρωτεϊνικών αντισωμάτων επιβεβαιώνει τη θεωρία της προέλευσης των πρώτων μορφών ζωής που βασίζονται στο RNA, και όχι στις πρωτεΐνες (υπενθυμίζουμε ότι αυτή είναι η αγαπημένη θεωρία του Ακαδημαϊκού A.S. Spirin) .
Ενώ υπήρχαν μόνο δύο «παίκτες» στην αρένα της μοριακής βιολογίας – το siRNA και το microRNA – ο κύριος «σκοπός» της παρεμβολής RNA φαινόταν εντελώς ξεκάθαρος. Πράγματι: ένα σύνολο ομόλογων βραχέων RNA και πρωτεϊνών σε διαφορετικούς οργανισμούς πραγματοποιεί παρόμοιες δράσεις. Καθώς οι οργανισμοί γίνονται πιο περίπλοκοι, το ίδιο συμβαίνει και με τη λειτουργικότητα.
Ωστόσο, στη διαδικασία της εξέλιξης, η φύση δημιούργησε ένα άλλο, εξελικτικά πιο πρόσφατο και εξαιρετικά εξειδικευμένο σύστημα που βασίζεται στην ίδια επιτυχημένη αρχή της παρεμβολής RNA. Μιλάμε για piRNA (piRNA, από το Piwi-interaction RNA).
Όσο πιο πολύπλοκο είναι το γονιδίωμα, τόσο πιο ανεπτυγμένος και προσαρμοσμένος είναι ο οργανισμός (ή το αντίστροφο; ;-). Ωστόσο, η αυξανόμενη πολυπλοκότητα του γονιδιώματος έχει επίσης ένα μειονέκτημα: ένα σύνθετο γενετικό σύστημα γίνεται ασταθές. Αυτό οδηγεί στην ανάγκη για μηχανισμούς υπεύθυνους για τη διατήρηση της ακεραιότητας του γονιδιώματος - διαφορετικά η αυθόρμητη «ανάμιξη» του DNA απλώς θα το απενεργοποιήσει. Τα κινητά γενετικά στοιχεία (MGEs), ένας από τους κύριους παράγοντες αστάθειας του γονιδιώματος, είναι μικρές ασταθείς περιοχές που μπορούν να μεταγραφούν αυτόνομα και να μεταναστεύσουν σε όλο το γονιδίωμα. Η ενεργοποίηση τέτοιων μετατιθέμενων στοιχείων οδηγεί σε πολλαπλές θραύσεις του DNA στα χρωμοσώματα, που μπορεί να έχουν θανατηφόρες συνέπειες.
Ο αριθμός των MGE αυξάνεται μη γραμμικά με το μέγεθος του γονιδιώματος και η δραστηριότητά τους πρέπει να περιορίζεται. Για να γίνει αυτό, τα ζώα, ξεκινώντας από συνεντερικά, χρησιμοποιούν το ίδιο φαινόμενο παρεμβολής RNA. Αυτή η λειτουργία εκτελείται επίσης από μικρά RNA, αλλά όχι από αυτά που έχουν ήδη συζητηθεί, αλλά από έναν τρίτο τύπο - τα piRNA.
«Πορτρέτο» του piRNA
Τα piRNA είναι μικρά μόρια μήκους 24-30 νουκλεοτιδίων, που κωδικοποιούνται στις κεντρομερείς και τελομερείς περιοχές του χρωμοσώματος. Οι αλληλουχίες πολλών από αυτά είναι συμπληρωματικές με γνωστά κινητά γενετικά στοιχεία, αλλά υπάρχουν πολλά άλλα piRNA που συμπίπτουν με περιοχές λειτουργικών γονιδίων ή με θραύσματα γονιδιώματος των οποίων οι λειτουργίες είναι άγνωστες.
Τα piRNA (καθώς και τα microRNA) κωδικοποιούνται και στους δύο κλώνους του γονιδιωματικού DNA. είναι πολύ μεταβλητά και ποικίλα (έως 500.000 (!) είδη σε έναν οργανισμό). Σε αντίθεση με το siRNA και το microRNA, σχηματίζονται από μία αλυσίδα με χαρακτηριστικό στοιχείο– ουρακίλη (U) στο 5’ άκρο και μεθυλιωμένο 3’ άκρο. Υπάρχουν και άλλες διαφορές:
- Σε αντίθεση με τα siRNA και τα microRNA, δεν απαιτούν επεξεργασία από το Dicer.
- Τα γονίδια piRNA είναι ενεργά μόνο στα γεννητικά κύτταρα (κατά την εμβρυογένεση) και στα γύρω ενδοθηλιακά κύτταρα.
- Η πρωτεϊνική σύνθεση του συστήματος piRNA είναι διαφορετική - αυτές είναι ενδονουκλεάσες της κατηγορίας Piwi (Piwi και Aub) και μια ξεχωριστή ποικιλία Argonaute - Ago3.
Η επεξεργασία και η δραστηριότητα των piRNAs είναι ακόμα ελάχιστα κατανοητές, αλλά είναι ήδη σαφές ότι ο μηχανισμός δράσης είναι εντελώς διαφορετικός από άλλα σύντομα RNA - σήμερα έχει προταθεί ένα μοντέλο πινγκ-πονγκ της δουλειάς τους (Εικ. 5 Α, Β).
Μηχανισμός πινγκ-πονγκ βιογένεσης piRNA

Ρύζι. 5Α: Κυτοπλασματικό μέρος της επεξεργασίας του piRNA
Η βιογένεση και η δραστηριότητα των piRNAs διαμεσολαβείται από την οικογένεια των ενδονουκλεασών Piwi (Ago3, Aub, Piwi). Η δραστηριότητα του piRNA παρέχεται και από τα μονόκλωνα μόρια piRNA - νόημα και αντι-νοηματικά - καθένα από τα οποία συνδέεται με μια συγκεκριμένη ενδονουκλεάση Piwi. Το piRNA αναγνωρίζει τη συμπληρωματική περιοχή του mRNA του τρανσποζονίου (μπλε κλώνος) και την αποκόπτει. Αυτό όχι μόνο απενεργοποιεί το τρανσποζόνιο, αλλά δημιουργεί επίσης ένα νέο piRNA (που συνδέεται με το Ago3 μέσω μεθυλίωσης του 3' άκρου από τη μεθυλάση Hen1). Αυτό το piRNA, με τη σειρά του, αναγνωρίζει το mRNA με μεταγραφές από το σύμπλεγμα πρόδρομων piRNA (κόκκινος κλώνος) - με αυτόν τον τρόπο ο κύκλος κλείνει και το επιθυμητό piRNA παράγεται ξανά.

Ρύζι. 5Β: piRNA στον πυρήνα
Εκτός από την ενδονουκλεάση Aub, η ενδονουκλεάση Piwi μπορεί επίσης να δεσμεύσει αντιπληροφοριακό piRNA. Μετά τη δέσμευση, το σύμπλοκο μεταναστεύει στον πυρήνα, όπου προκαλεί αποικοδόμηση των συμπληρωματικών μεταγραφών και αναδιάταξη της χρωματίνης, προκαλώντας καταστολή της δραστηριότητας του τρανσποζονίου.
Λειτουργίες του piRNA
Η κύρια λειτουργία του piRNA είναι να καταστέλλει τη δραστηριότητα MGE στο επίπεδο της μεταγραφής και της μετάφρασης. Πιστεύεται ότι τα piRNA είναι ενεργά μόνο κατά τη διάρκεια της εμβρυογένεσης, όταν η απρόβλεπτη ανακάτεμα του γονιδιώματος είναι ιδιαίτερα επικίνδυνη και μπορεί να οδηγήσει στο θάνατο του εμβρύου. Αυτό είναι λογικό - όταν το ανοσοποιητικό σύστημα δεν έχει αρχίσει ακόμη να λειτουργεί, τα κύτταρα του εμβρύου χρειάζονται κάποια απλή αλλά αποτελεσματική προστασία. Το έμβρυο προστατεύεται αξιόπιστα από εξωτερικά παθογόνα από τον πλακούντα (ή το κέλυφος του αυγού). Αλλά εκτός από αυτό, η άμυνα είναι επίσης απαραίτητη από ενδογενείς (εσωτερικούς) ιούς, κυρίως MGE.
Αυτός ο ρόλος του piRNA έχει επιβεβαιωθεί από την εμπειρία - «νοκ-άουτ» ή μεταλλάξεις των γονιδίων Ago3, Piwi ή Aub οδηγούν σε σοβαρές αναπτυξιακές διαταραχές (και απότομη αύξηση του αριθμού των μεταλλάξεων στο γονιδίωμα ενός τέτοιου οργανισμού) και επίσης προκαλούν υπογονιμότητα λόγω διακοπής της ανάπτυξης των γεννητικών κυττάρων.
Κατανομή και εξέλιξη των piRNAs
Τα πρώτα piRNA βρίσκονται ήδη σε θαλάσσιες ανεμώνες και σφουγγάρια. Τα φυτά προφανώς ακολούθησαν διαφορετική πορεία - πρωτεΐνες Piwi δεν βρέθηκαν σε αυτά και ο ρόλος ενός "μυγχώματος" για τρανσποζόνια εκτελείται από την ενδονουκλεάση Ago4 και το siRNA.
Σε ανώτερα ζώα, συμπεριλαμβανομένων των ανθρώπων, το σύστημα piRNA είναι πολύ καλά ανεπτυγμένο, αλλά μπορεί να βρεθεί μόνο σε εμβρυϊκά κύτταρα και στο αμνιακό ενδοθήλιο. Γιατί η κατανομή του piRNA στο σώμα είναι τόσο περιορισμένη μένει να φανεί. Μπορούμε να υποθέσουμε ότι, όπως κάθε ισχυρό όπλο, τα piRNA είναι ωφέλιμα μόνο υπό πολύ συγκεκριμένες συνθήκες (κατά την ανάπτυξη του εμβρύου) και στο σώμα των ενηλίκων η δραστηριότητά τους θα προκαλέσει περισσότερο κακό παρά καλό. Ακόμα, ο αριθμός των piRNA υπερβαίνει τον αριθμό των γνωστών πρωτεϊνών κατά μια τάξη μεγέθους και οι μη ειδικές επιδράσεις των piRNA στα ώριμα κύτταρα είναι δύσκολο να προβλεφθούν.
| siRNA | microRNA | piRNA | |
| Διάδοση | Φυτά, Δροσοφίλα, C. elegans. Δεν βρίσκεται σε σπονδυλωτά | Ευκαρυωτες | Εμβρυικά κύτταρα ζώων (ξεκινώντας από συνεντερικά). Όχι σε πρωτόζωα και φυτά |
| Μήκος | 21-22 νουκλεοτίδια | 19-25 νουκλεοτίδια | 24-30 νουκλεοτίδια |
| Δομή | Δίκλωνα, 19 συμπληρωματικά νουκλεοτίδια και δύο μη ζευγαρωμένα νουκλεοτίδια στο 3' άκρο | Σύνθετη δομή μονής αλυσίδας | Σύνθετη δομή μονής αλυσίδας. U στο 5'-τελος, 2'- Ο-μεθυλιωμένο 3' άκρο |
| Επεξεργασία | Dicer-εξαρτώμενος | Dicer-εξαρτώμενος | Dicer-ανεξάρτητος |
| Ενδονουκλεάσες | Ago2 | Ago1, Ago2 | Ago3, Piwi, Aub |
| Δραστηριότητα | Αποικοδόμηση συμπληρωματικών mRNA, ακετυλίωση γονιδιωματικού DNA | Αποικοδόμηση ή αναστολή της μετάφρασης του mRNA στόχου | Αποικοδόμηση mRNA που κωδικοποιεί MGE, ρύθμιση μεταγραφής MGE |
| Βιολογικός ρόλος | Αντιϊκή ανοσολογική άμυνα, καταστολή της δραστηριότητας των δικών του γονιδίων | Ρύθμιση της γονιδιακής δραστηριότητας | Καταστολή της δραστηριότητας MGE κατά την εμβρυογένεση |
συμπέρασμα
Εν κατακλείδι, θα ήθελα να παράσχω έναν πίνακα που απεικονίζει την εξέλιξη της συσκευής πρωτεΐνης που εμπλέκεται στην παρεμβολή RNA (Εικ. 6). Μπορεί να φανεί ότι τα πρωτόζωα έχουν το πιο ανεπτυγμένο σύστημα siRNA (οικογένειες πρωτεϊνών Ago, Dicer) και καθώς οι οργανισμοί γίνονται πιο πολύπλοκοι, η έμφαση μετατοπίζεται σε πιο εξειδικευμένα συστήματα - τον αριθμό των ισομορφών πρωτεΐνης για microRNA (Drosha, Pasha) και piRNA ( Piwi, Hen1) αυξάνεται. Ταυτόχρονα, μειώνεται η ποικιλία των ενζύμων που μεσολαβούν στη δράση του siRNA.

Ρύζι. 6. Ποικιλομορφία πρωτεϊνών που εμπλέκονται στην παρεμβολή RNA
Και
Οι αριθμοί δείχνουν τον αριθμό των πρωτεϊνών σε κάθε ομάδα. Στοιχεία χαρακτηριστικά του siRNA και του microRNA επισημαίνονται με μπλε και οι πρωτεΐνες που σχετίζονται με το piRNA επισημαίνονται με κόκκινο. Σύμφωνα με .
Το φαινόμενο της παρεμβολής RNA άρχισε να χρησιμοποιείται από τους πιο απλούς οργανισμούς. Με βάση αυτόν τον μηχανισμό, η φύση δημιούργησε ένα πρωτότυπο του ανοσοποιητικού συστήματος και καθώς οι οργανισμοί γίνονται πιο πολύπλοκοι, η παρεμβολή RNA γίνεται ένας απαραίτητος ρυθμιστής της δραστηριότητας του γονιδιώματος. Δύο διαφορετικοί μηχανισμοί συν τρεις τύποι βραχέων RNA (βλ. συνοπτικό πίνακα) - ως αποτέλεσμα, βλέπουμε χιλιάδες λεπτούς ρυθμιστές διαφόρων μεταβολικών και γενετικών οδών. Αυτή η εντυπωσιακή εικόνα απεικονίζει την ευελιξία και την εξελικτική προσαρμογή των μοριακών βιολογικών συστημάτων. Τα σύντομα RNA αποδεικνύουν και πάλι ότι δεν υπάρχουν «μικρά πράγματα» μέσα στο κύτταρο - υπάρχουν μόνο μικρά μόρια, την πλήρη σημασία του ρόλου των οποίων μόλις αρχίζουμε να καταλαβαίνουμε.
Είναι αλήθεια ότι μια τέτοια φανταστική πολυπλοκότητα μάλλον υποδηλώνει ότι η εξέλιξη είναι «τυφλή» και δρα χωρίς ένα προεγκεκριμένο «κύριο σχέδιο».
Βιβλιογραφία
- Gurdon J. B., Lane C. D., Woodland Η. R., Marbaix G. (1971). Χρήση αυγών και ωοκυττάρων βατράχου για τη μελέτη του αγγελιαφόρου RNA και τη μετάφρασή του σε ζωντανά κύτταρα. Nature 233, 177-182;
- Spirin A. S. (2001). Η Βιοσύνθεση Πρωτεϊνών, ο Κόσμος του RNA και η Προέλευση της Ζωής. Δελτίο της Ρωσικής Ακαδημίας Επιστημών 71, 320-328;
- Στοιχεία: "Ολόκληρα μιτοχονδριακά γονιδιώματα εξαφανισμένων ζώων μπορούν πλέον να εξαχθούν από τρίχες".
- Fire A., Xu S., Montgomery M.K., Kostas S.A., Driver S.E., Mello C.C. (1998). Ισχυρή και ειδική γενετική παρέμβαση από δίκλωνο RNA Caenorhabditis elegans. Nature 391, 806-311;
- Βιομόριο: «MicroRNA που ανακαλύφθηκαν για πρώτη φορά σε μονοκύτταρο οργανισμό».
- Covey S., Al-Kaff Ν., Lángara Α., Turner D. (1997). Τα φυτά καταπολεμούν τη μόλυνση με γονιδιακή σίγαση. Nature 385, 781-782;
- Biomolecule: "Molecular double-dealing: τα ανθρώπινα γονίδια λειτουργούν για τον ιό της γρίπης".
- Ren B. (2010). Μεταγραφή: Οι ενισχυτές κάνουν μη κωδικοποιητικό RNA. Nature 465, 173–174;
- Taganov K.D., Boldin M.P., Chang K.J., Baltimore D. (2006). Η εξαρτώμενη από το NF-κΒ επαγωγή του microRNA miR-146, ενός αναστολέα που στοχεύει σε πρωτεΐνες σηματοδότησης εγγενών ανοσολογικών αποκρίσεων. Proc. Natl. Ακαδ. Sci. ΗΠΑ. 103, 12481-12486;
- O'Connell R. M., Rao D. S., Chaudhuri A. A., Boldin M. P., Taganov K. D., Nicoll J., Paquette R. L., Baltimore D. (2008). Η παρατεταμένη έκφραση του microRNA-155 σε αιμοποιητικά βλαστοκύτταρα προκαλεί μυελοπολλαπλασιαστική διαταραχή. J. Εχρ. Med. 205, 585-594;
- Βιομόριο: "microRNA - όσο πιο μακριά στο δάσος, τόσο περισσότερα καυσόξυλα";
- Στοιχεία: «Η επιπλοκή του σώματος στα αρχαία ζώα συνδέθηκε με την εμφάνιση νέων ρυθμιστικών μορίων».
- Grimson A., Srivastava M., Fahey B., Woodcroft B.J., Chiang H.R., King N., Degnan B.M., Rokhsar D.S., Bartel D.P. (2008). Πρώιμη προέλευση και εξέλιξη των microRNA και των RNA που αλληλεπιδρούν με Piwi σε ζώα. Nature 455, 1193–1197.
- Aravin A., Hannon G., Brennecke J. (2007). Το μονοπάτι Piwi-piRNA παρέχει μια προσαρμοστική άμυνα στον αγώνα όπλων με transposon. Science 318, 761–764;
- Βιομόριο: "
Οι επιστήμονες πιστεύουν ότι η εσφαλμένη έκφραση μικρών RNA είναι μία από τις αιτίες μιας σειράς ασθενειών που επηρεάζουν σοβαρά την υγεία πολλών ανθρώπων σε όλο τον κόσμο. Αυτές οι ασθένειες περιλαμβάνουν τα καρδιαγγειακά 23 και τον καρκίνο 24 . Όσο για το τελευταίο, αυτό δεν προκαλεί έκπληξη: ο καρκίνος υποδηλώνει ανωμαλίες στην ανάπτυξη των κυττάρων και τη μοίρα τους, και τα μικρά RNA παίζουν κρίσιμο ρόλο στις αντίστοιχες διεργασίες. Εδώ είναι ένα από τα πιο σημαντικά παραδείγματα της τεράστιας επίδρασης που έχουν τα μικρά RNA στο σώμα κατά τη διάρκεια του καρκίνου. Μιλάμε για έναν κακοήθη όγκο, ο οποίος χαρακτηρίζεται από λανθασμένη έκφραση των γονιδίων εκείνων που δρουν κατά την αρχική ανάπτυξη του οργανισμού, και όχι στη μεταγεννητική περίοδο. Πρόκειται για έναν τύπο παιδικού όγκου στον εγκέφαλο που εμφανίζεται συνήθως πριν από την ηλικία των δύο ετών. Δυστυχώς, αυτή είναι μια πολύ επιθετική μορφή καρκίνου και η πρόγνωση εδώ είναι δυσμενής ακόμη και με εντατική θεραπεία. Η ογκολογική διαδικασία αναπτύσσεται λόγω ακατάλληλης ανακατανομής του γενετικού υλικού στα εγκεφαλικά κύτταρα. Ένας προαγωγέας που κανονικά οδηγεί την ισχυρή έκφραση ενός από τα γονίδια που κωδικοποιούν την πρωτεΐνη υφίσταται ανασυνδυασμό με ένα συγκεκριμένο σύμπλεγμα μικρών RNA. Τότε ολόκληρη αυτή η αναδιαταχθείσα περιοχή υφίσταται ενίσχυση: με άλλα λόγια, δημιουργούνται πολλά αντίγραφά της στο γονιδίωμα. Κατά συνέπεια, μικρά RNA που βρίσκονται «κατάντη» του μετατοπισμένου προαγωγέα εκφράζονται πολύ πιο έντονα από ό,τι θα έπρεπε. Το επίπεδο των ενεργών μικρών RNA είναι περίπου 150-1000 φορές υψηλότερο από το κανονικό.
Ρύζι. 18.3.Μικρά RNA που ενεργοποιούνται από το αλκοόλ μπορούν να συνδυαστούν με αγγελιαφόρα RNA που δεν επηρεάζουν την αντίσταση του σώματος στις επιδράσεις του αλκοόλ. Αλλά αυτά τα μικρά RNA δεν συνδέονται με τα μόρια αγγελιαφόρου RNA που προάγουν τέτοια αντίσταση. Αυτό έχει ως αποτέλεσμα μια σχετική υπεροχή της αναλογίας των μορίων αγγελιαφόρου RNA που κωδικοποιούν παραλλαγές πρωτεΐνης που σχετίζονται με την ανοχή στο αλκοόλ.
Αυτό το σύμπλεγμα κωδικοποιεί περισσότερα από 40 διαφορετικά μικρά RNA. Στην πραγματικότητα, αυτό είναι γενικά το μεγαλύτερο από αυτά τα σμήνη που βρέθηκαν σε πρωτεύοντα. Συνήθως εκφράζεται μόνο νωρίς στην ανθρώπινη ανάπτυξη, στις πρώτες 8 εβδομάδες της εμβρυϊκής ζωής. Η ισχυρή ενεργοποίησή του στον εγκέφαλο του βρέφους οδηγεί σε καταστροφικές επιπτώσεις στη γενετική έκφραση. Μια συνέπεια είναι η έκφραση μιας επιγενετικής πρωτεΐνης που προσθέτει τροποποιήσεις στο DNA. Αυτό οδηγεί σε εκτεταμένες αλλαγές σε ολόκληρο το πρότυπο της μεθυλίωσης του DNA, και ως εκ τούτου σε μη φυσιολογική έκφραση όλων των ειδών γονιδίων, πολλά από τα οποία θα πρέπει να εκφράζονται μόνο όταν τα ανώριμα εγκεφαλικά κύτταρα διαιρούνται κατά τη διάρκεια πρώιμα στάδιαανάπτυξη του σώματος. Έτσι ξεκινά το πρόγραμμα καρκίνου στα κύτταρα του μωρού 25.
Μια τέτοια επικοινωνία μεταξύ μικρών RNA και του επιγενετικού μηχανισμού του κυττάρου μπορεί να έχει σημαντικό αντίκτυπο σε άλλες καταστάσεις όπου τα κύτταρα αναπτύσσουν προδιάθεση για καρκίνο. Αυτός ο μηχανισμός πιθανότατα έχει ως αποτέλεσμα η επίδραση της διακοπής της έκφρασης του μικρού RNA να ενισχύεται από αλλαγές στις επιγενετικές τροποποιήσεις που μεταδίδονται στα θυγατρικά κύτταρα από τη μητέρα. Αυτό μπορεί να δημιουργήσει ένα μοτίβο δυνητικά επικίνδυνων αλλαγών στο πρότυπο γονιδιακής έκφρασης.
Μέχρι στιγμής, οι επιστήμονες δεν έχουν καταλάβει όλα τα στάδια της αλληλεπίδρασης των μικρών RNA με τις επιγενετικές διεργασίες, αλλά μπορούν ακόμα να πάρουν κάποιες συμβουλές για τα χαρακτηριστικά αυτού που συμβαίνει. Για παράδειγμα, αποδείχθηκε ότι μια συγκεκριμένη κατηγορία μικρών RNA, που ενισχύουν την επιθετικότητα του καρκίνου του μαστού, στοχεύει ορισμένα ένζυμα στα αγγελιαφόρα RNA που αφαιρούν βασικές επιγενετικές τροποποιήσεις. Αυτό αλλάζει το πρότυπο των επιγενετικών τροποποιήσεων στο καρκινικό κύτταρο και διαταράσσει περαιτέρω τη γενετική έκφραση 26 .
Πολλές μορφές καρκίνου είναι δύσκολο να εντοπιστούν σε έναν ασθενή. Ογκολογικές διεργασίες μπορεί να εμφανιστούν σε δυσπρόσιτα σημεία, γεγονός που περιπλέκει τη διαδικασία δειγματοληψίας. Σε τέτοιες περιπτώσεις, δεν είναι εύκολο για τον γιατρό να παρακολουθεί την εξέλιξη της διαδικασίας του καρκίνου και την ανταπόκριση στη θεραπεία. Συχνά οι γιατροί αναγκάζονται να βασίζονται σε έμμεσες μετρήσεις - ας πούμε, μια τομογραφία ενός όγκου. Ορισμένοι ερευνητές πιστεύουν ότι μικρά μόρια RNA θα μπορούσαν να βοηθήσουν στη δημιουργία μιας νέας τεχνικής για την παρακολούθηση της ανάπτυξης του όγκου, η οποία θα μπορούσε επίσης να μελετήσει την προέλευσή του. Όταν τα καρκινικά κύτταρα πεθαίνουν, μικρά RNA εγκαταλείπουν το κύτταρο όταν αυτό σπάσει. Αυτά τα μικρά άχρηστα μόρια συχνά σχηματίζουν σύμπλοκα με κυτταρικές πρωτεΐνες ή είναι τυλιγμένα σε θραύσματα κυτταρικές μεμβράνες. Λόγω αυτού, είναι πολύ σταθερά στα σωματικά υγρά, πράγμα που σημαίνει ότι τέτοια RNA μπορούν να απομονωθούν και να αναλυθούν. Δεδομένου ότι οι ποσότητες τους είναι μικρές, οι ερευνητές θα πρέπει να χρησιμοποιήσουν πολύ ευαίσθητες μεθόδους ανάλυσης. Ωστόσο, τίποτα δεν είναι αδύνατο εδώ: ευαισθησία αλληλουχίας νουκλεϊκά οξέασυνεχώς αυξάνεται 27. Έχουν δημοσιευθεί δεδομένα που επιβεβαιώνουν την υπόσχεση αυτής της προσέγγισης σε σχέση με τον καρκίνο του μαστού 28 , τον καρκίνο των ωοθηκών 29 και μια σειρά από άλλες ογκολογικές ασθένειες. Η ανάλυση των μικρών κυκλοφορούντων RNA σε ασθενείς με καρκίνο του πνεύμονα έδειξε ότι αυτά τα RNA βοηθούν στη διάκριση μεταξύ ασθενών με μονήρη πνευμονικό όζο (που δεν χρειάζεται θεραπεία) και ασθενών που αναπτύσσουν οζίδια κακοήθους όγκου (που απαιτούν θεραπεία) 30 .
Μικρά RNA που σχηματίζουν φουρκέτες ή κοντά RNA που σχηματίζουν φουρκέτες (shRNA κοντή φουρκέτα RNA, μικρή φουρκέτα RNA) μόρια βραχέων RNA που σχηματίζουν δευτερεύουσα δομήσφιχτά στιλέτο. Τα ShRNA μπορούν να χρησιμοποιηθούν για την απενεργοποίηση της έκφρασης... ... Wikipedia
RNA πολυμεράση- από κύτταρο T. aquaticus κατά την αντιγραφή. Ορισμένα στοιχεία του ενζύμου γίνονται διαφανή και οι αλυσίδες RNA και DNA είναι πιο ευδιάκριτες. Το ιόν μαγνησίου (κίτρινο) βρίσκεται στην ενεργό θέση του ενζύμου. Η RNA πολυμεράση είναι ένα ένζυμο που εκτελεί ... ... Wikipedia
Παρεμβολή RNA- Παράδοση μικρών RNA που περιέχουν φουρκέτες χρησιμοποιώντας φορέα που βασίζεται σε φακοϊό και ο μηχανισμός παρεμβολής RNA σε κύτταρα θηλαστικών Παρεμβολή RNA (μια ... Wikipedia
γονίδιο RNA- Το μη κωδικοποιητικό RNA (ncRNA) είναι μόρια RNA που δεν μεταφράζονται σε πρωτεΐνες. Το προηγουμένως χρησιμοποιούμενο συνώνυμο, μικρό RNA (smRNA, μικρό RNA), δεν χρησιμοποιείται πλέον, καθώς ορισμένα μη κωδικοποιητικά RNA μπορεί να είναι πολύ ... ... Wikipedia
Μικρά πυρηνικά RNA- (snRNA, snRNA) μια κατηγορία RNA που βρίσκεται στον πυρήνα των ευκαρυωτικών κυττάρων. Μεταγράφονται από RNA πολυμεράση II ή RNA πολυμεράση III και εμπλέκονται σε σημαντικές διεργασίες όπως το μάτισμα (αφαίρεση ιντρονίων από ανώριμο mRNA), η ρύθμιση ... Wikipedia
Μικρά πυρηνικά RNA- (snoRNA, αγγλικά snoRNA) μια κατηγορία μικρών RNA που εμπλέκονται σε χημικές τροποποιήσεις (μεθυλίωση και ψευδουριδυλίωση) του ριβοσωμικού RNA, καθώς και του tRNA και του μικρού πυρηνικού RNA. Σύμφωνα με την ταξινόμηση MeSH, τα μικρά πυρηνικά RNA θεωρούνται υποομάδα... ... Wikipedia
μικρά πυρηνικά (πυρηνικά μικρού μοριακού βάρους) RNA- Μια εκτεταμένη ομάδα (105.106) μικρών πυρηνικών RNA (100.300 νουκλεοτίδια), που σχετίζονται με ετερογενές πυρηνικό RNA, αποτελούν μέρος των μικρών κόκκων ριβονουκλεοπρωτεΐνης του πυρήνα. Τα M.n.RNA είναι απαραίτητο συστατικό του συστήματος ματίσματος... ...
μικρά κυτταροπλασματικά RNA- Μικρά (100-300 νουκλεοτίδια) μόρια RNA που εντοπίζονται στο κυτταρόπλασμα, παρόμοια με το μικρό πυρηνικό RNA. [Arefyev V.A., Lisovenko L.A. Αγγλικά Ρωσικά Λεξικόγενετικοί όροι 1995 407 σελ.] Θέματα γενετική EN scyrpssμικρό κυτταροπλασματικό... ... Οδηγός Τεχνικού Μεταφραστή
μικρά πυρηνικά RNA κατηγορίας U- Μια ομάδα μικρών μορίων RNA που σχετίζονται με πρωτεΐνη (από 60 έως 400 νουκλεοτίδια) που αποτελούν σημαντικό μέρος των περιεχομένων του ματιού και εμπλέκονται στη διαδικασία εκτομής των ιντρονίων. σε 4 από τους 5 καλά μελετημένους τύπους Usn, τα U1, U2, U4 και U5 RNA είναι 5... ... Οδηγός Τεχνικού Μεταφραστή
Βιοδείκτες RNA- * Βιοδείκτες RNA * Βιοδείκτες RNA ένας τεράστιος αριθμός ανθρώπινων μεταγραφών που δεν κωδικοποιούν τη σύνθεση πρωτεϊνών (nsbRNA ή npcRNA). Στις περισσότερες περιπτώσεις, τα μικρά (miRNA, snoRNA) και τα μακρά (αντινόημα RNA, dsRNA και άλλοι τύποι) μόρια RNA είναι... ... Γενεσιολογία. εγκυκλοπαιδικό λεξικό
Βιβλία
- Αγορά για 1877 UAH (μόνο για την Ουκρανία)
- Κλινική γενετική. Εγχειρίδιο (+CD), Bochkov Nikolay Pavlovich, Puzyrev Valery Pavlovich, Smirnikhina Svetlana Anatolyevna. Όλα τα κεφάλαια έχουν αναθεωρηθεί και συμπληρωθεί σε σχέση με την ανάπτυξη της ιατρικής επιστήμης και πρακτικής. Τα κεφάλαια για τις πολυπαραγοντικές ασθένειες, την πρόληψη, τη θεραπεία των κληρονομικών ασθενειών,…