Карбоновые кислоты - органические кислоты. Они входят в состав живых организмов и участвуют в метаболизме. Химические свойства карбоновых кислот обуславливаются наличием карбоксильной группы -СООН. К ним относятся уксусная, муравьиная, щавелевая, масляная и ряд других кислот.
Общее описание
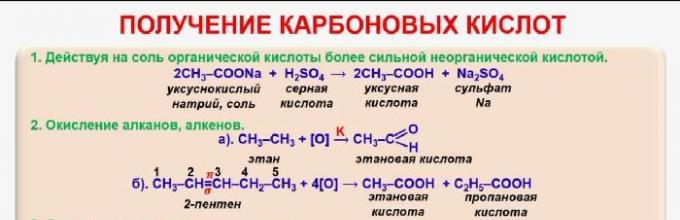
Существует несколько способов получения карбоновых кислот:
- окисление спиртов - C 2 H 5 OH + O2 → CH 3 COOH + H 2 O (из этанола образуется уксусная кислота);
- окисление альдегидов - CH 3 COH + [O] → CH 3 COOH;
- окисление бутана - 2C 4 H 10 + 5O 2 → 4CH 3 COOH + 2H 2 O;
- карбонилирование спирта - CH 3 + CO → CH 3 COOH;
- разложение щавелевой кислоты для получения муравьиной кислоты - C 2 H 2 O 4 → HCOOH + CO 2 ;
- взаимодействие солей с концентрированной серной кислотой - CH 3 COONa + H 2 SO 4 → CH 3 COOH + NaHSO 4 .

Рис. 1. Способы получения карбоновых кислот.
Физические свойства карбоновых кислот:
- температура кипения выше, чем у соответствующих углеводородов и спиртов;
- хорошая растворимость в воде - растворяются на катионы водорода и анионы кислотного остатка (являются слабыми электролитами);
- увеличение числа атомов углерода уменьшает силу кислот.
Карбоновые кислоты имеют прочные водородные связи (прочнее, чем у спиртов), что обуславливается высоким положительным зарядом на атоме водорода в карбоксильной группе.
Взаимодействие
Карбоновые кислоты изменяют окраску индикаторов. Лакмус и метилоранж становятся красными.

Рис. 2. Взаимодействие с индикаторами.
В таблице химических свойств карбоновых кислот описано взаимодействие кислот с другими веществами.
|
Реакции |
Результат |
Пример |
|
С металлами |
Выделяется водород, образуются соли |
2CH 3 COOH + Mg → (CH 3 COO) 2 Mg + H 2 |
|
С оксидами |
Образуются соль и вода |
2CH 3 COOH + ZnO → (CH 3 COO) 2 Zn + H 2 O |
|
С основаниями (нейтрализация) |
Образуются соль и вода |
CH 3 COOH + NaOH → CH 3 COONa + H 2 O |
|
С карбонатами |
Выделяются углекислый газ и вода |
2CH 3 COOH + CaCO 3 → (CH 3 COO) 2 Ca + H 2 O + CO 2 |
|
С солями слабых кислот |
Образуется неорганическая кислота |
2CH 3 COOH + Na 2 SiO 3 → 2CH 3 COONa + H 2 SiO 3 |
|
С аммиаком или гидроксидом аммония |
Образуется ацетат аммония. При взаимодействии с гидроксидом выделяется вода |
CH 3 COOH + NH 3 → CH 3 COONH 4 CH 3 COOH + NH 4 OH → CH 3 COONH 4 + H 2 O |
|
Со спиртами (этерификация) |
Образуются сложные эфиры |
CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O |
|
Галогенирование |
Образуется соль |
CH 3 COOH + Br 2 → CH 2 BrCOOH |
Соли, образующиеся при взаимодействии веществ с муравьиной кислотой, называются формиатами, с уксусной кислотой - ацетатами.
Декарбоксилирование
Отщепление карбоксильной группы называется процессом декарбоксилирования, который происходит в следующих случаях:
- при нагревании солей в присутствии твёрдых щелочей с образованием алканов - RCOONa тв + NaOH тв → RH + Na 2 CO 3 ;
- при нагревании твёрдых солей - (СН 3 СОО) 2 Са → СН 3 -СО-СН 3 + СаСО 3 ;
- при прокаливании бензойной кислоты - Ph-COOH → PhH + CO 2 ;
- при электролизе растворов солей - 2RCOONa + Н 2 О → R-R + 2CO 2 + 2NaOH.
Карбоновыми кислотами называют соединения, в которых содержится карбоксильная группа:
Карбоновые кислоты различают:
- одноосновные карбоновые кислоты;
- двухосновные (дикарбоновые) кислоты (2 группы СООН ).
В зависимости от строения карбоновые кислоты различают:
- алифатические;
- алициклические;
- ароматические.
Примеры карбоновых кислот.


Получение карбоновых кислот.
1. Окисление первичных спиртов перманганатом калия и дихроматом калия:

2. Гибролиз галогензамещенных углеводородов, содержащих 3 атома галогена у одного атома углерода:
3. Получение карбоновых кислот из цианидов:
При нагревании нитрил гидролизуется с образованием ацетата аммония:
При подкисления которого выпадает кислота:
4. Использование реактивов Гриньяра:
5. Гидролиз сложных эфиров:
6. Гидролиз ангидридов кислот:
7. Специфические способы получения карбоновых кислот:
Муравьиная кислота получается при нагревании оксида углерода (II) с порошкообразным гидроксидом натрия под давлением:
Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
Бензойную кислоту получают окислением монозамещенных гомологов раствором перманганата калия:
Реакция Каннициаро . Бензальдегид обрабатывают 40-60% раствором гидроксида натрия при комнатной температуре.

Химические свойства карбоновых кислот.
В водном растворе карбоновые кислоты диссоциируют:

Равновесие сдвинуто сильно влево, т.к. карбоновые кислоты являются слабыми.
Заместители влияют на кислотность вследствие индуктивного эффекта. Такие заместители оттягивают электронную плотность на себя и на них возникает отрицательный индуктивный эффект (-I). Оттягивание электронной плотности приводит к повышению кислотности кислоты. Электронодонорные заместители создают положительный индуктивный заряд.

1. Образование солей. Реагирование с основными оксидами, солями слабых кислот и активными металлами:

Карбоновые кислоты - слабые, т.к. минеральные кислоты вытесняют их из соответствующих солей:
2. Образование функциональных производных карбоновых кислот:
3. Сложные эфиры при нагревании кислоты со спиртом в присутствие серной кислоты - реакция этерификации:
4. Образование амидов, нитрилов:
3. Свойства кислот обуславливаются наличием углеводородного радикала. Если протекает реакция в присутствие красного фосфора, то образует следующий продукт:
4. Реакция присоединения.

8. Декарбоксилирование. Реакцию проводят сплавлением щелочи с солью щелочного металла карбоновой кислоты:
9. Двухосновная кислота легко отщепляет СО 2
при нагревании:
Дополнительные материалы по теме: Карбоновые кислоты.
Калькуляторы по химии |
|
| Химия онлайн на нашем сайте для решения задач и уравнений. | |
Окисление насыщенных углеводородов кислородом на специальных катализаторах до карбоновых кислот осуществляют в промышленности, однако селективностью этот способ не отличается. Как правило, получаются смеси карбоновых кислот, поскольку при окислении происходит разрыв различных углерод-углеродных связей.
Значительно более селективным является окисление алкенов сильными окислителями. При нагревании алкенов, имеющих по одному атому водорода у каждого атома углерода двойной связи, со щелочным раствором перманганата калия образуется смесь двух карбоновых кислот. Если же алкен симметричный, то образуются две молекулы одной карбоновой кислоты. Такое же окисление можно осуществить и при нагревании алкенов с концентрированной азотной кислотой.
![]()
Аналогично при окислении щелочным раствором перманганата калия алкинов получают карбоновые кислоты. Так, например, уксусную кислоту можно получить, окисляя либо 2-бутен, либо 2-бутин.

Алкилбензолы окисляют до бензойной кислоты либо кислородом на катализаторах (в промышленности), либо нагреванием с перманганатом калия. Например, кипячение толуола с водным раствором перманганата калия с последующим подкислением раствора приводит к бензойной кислоте.

Карбоновые кислоты могут быть получены также окислением первичных спиртов или альдегидов. В качестве окислителей обычно используют соединения хрома в высшей степени окисления, например, хромовый ангидрид, перманганат калия в щелочной среде, концентрированную азотную кислоту. Альдегиды легко окисляются и другими окислителями, напрмер, аммиачным раствором оксида серебра (реакция «серебряного зеркала»).

1.2. Синтез карбоновых кислот из галогенопроизводных
1.2.1.Синтез карбоновых кислот через нитрилы
Алкилгалогениды взаимодействием с цианидом натрия превращают в алкилцианиды, которые являются нитрилами карбоновых кислот. Последние гидролизуют в кислой среде до карбоновых кислот.

Таким образом, происходит двухстадийное замещение атома галогена в молекуле галогенопроизводного на карбоксильную группу. Так, для получения валериановой кислоты (5 атомов углерода) необходимо исходить из бутилгалогенида.
1-бромбутан нитрил валериановая кислота
валериановой кислоты
1.2.2. Синтез карбоновых кислот реакцией Гриньяра
Реактивы Гриньяра, которые получают из галогенопроизводных взаимодействием с металлическим магнием, представляют собой нуклеофильные реагенты. Поэтому для синтеза из них карбоновых кислот используют реакцию карбоксилирования с помощью электрофильного диоксида углерода.
Для получения этим методом бензойной кислоты в качестве исходного галогенопроизводного необходимо взять, например, бромбензол, который реакцией с магнием, последующим взаимодействием фенилмагнийбромида с диоксидом углерода и заключительным гидролизом магниевой соли превращают в бензойную кислоту.
1.3. Гидролиз производных карбоновых кислот
Подобно нитрилам и солям, о гидролизе которых речь уже шла, и другие производные карбоновых кислот гидролизуются до карбоновых кислот. Реакции могут катализироваться как кислотами, так и щелочами. Например, при гидролизе метилового эфира пропановой кислоты, катализируемом сильной минеральной кислотой, образуется пропановая кислота и метанол.
При нагревании ацетанилида (фениламида уксусной кислоты) с водным раствором едкого натра получается ацетат натрия и анилин.
Гидролиз молекулы ангидрида бензойной кислоты приводит к образованию двух молекул бензойной кислоты.

Подробнее о катализе и механизме гидролиза речь будет идти в разделах, посвященных производным карбоновых кислот
Получение карбоновых кислот
I . В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
2. Окисление алканов:
2CH 4 + + 3O 2 t,kat → 2HCOOH + 2H 2 O
метанмуравьиная кислота
2CH 3 -CH 2 -CH 2 -CH 3 + 5O 2 t,kat,p →4CH 3 COOH + 2H 2 O
н-бутануксусная кислота
3. Окисление алкенов:
CH 2 =CH 2 + O 2 t,kat → CH 3 COOH
этилен
СH 3 -CH=CH 2 + 4[O] t,kat → CH 3 COOH + HCOOH (уксусная кислота+муравьиная кислота )
4. Окисление гомологов бензола (получение бензойной кислоты):
C 6 H 5 -C n H 2n+1 + 3n[O] KMnO4,H+ → C 6 H 5 -COOH + (n-1)CO 2 + nH 2 O
5C 6 H 5 -CH 3 + 6KMnO 4 + 9H 2 SO 4 → 5C 6 H 5 -COOH + 3K 2 SO 4 + 6MnSO 4 + 14H 2 O
толуолбензойная кислота
5.Получение муравьиной кислоты:
1 стадия: CO + NaOH t , p →HCOONa ( формиат натрия – соль )
2 стадия : HCOONa + H 2 SO 4 → HCOOH + NaHSO 4
6. Получение уксусной кислоты:
CH 3 OH + CO t,p →CH 3 COOH
Метанол
II . В лаборатории
1. Гидролиз сложных эфиров:
2. Из солей карбоновых кислот :
R-COONa + HCl → R-COOH + NaCl
3. Растворением ангидридов карбоновых кислот в воде:
(R-CO) 2 O + H 2 O → 2 R-COOH
4. Щелочной гидролиз галоген производных карбоновых кислот:

III . Общие способы получения карбоновых кислот
1. Окисление альдегидов:
R-COH + [O] → R-COOH
Например, реакция «Серебряного зеркала» или окисление гидроксидом меди (II ) – качественные реакции альдегидов
2. Окисление спиртов:
R-CH 2 -OH + 2[O] t,kat → R-COOH + H 2 O
3. Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода.

4. Из цианидов (нитрилов) – способ позволяет наращивать углеродную цепь:
СH 3 -Br + Na-C≡N → CH 3 -CN + NaBr
CH 3 -CN - метилцианид (нитрил уксусной кислоты)
СH 3 -CN + 2H 2 O t → CH 3 COONH 4
ацетат аммония
CH 3 COONH 4 + HCl → CH 3 COOH + NH 4 Cl
5. Использование реактива Гриньяра
R-MgBr + CO 2 →R-COO-MgBr H2O → R-COOH + Mg(OH)Br
ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ
Муравьиная кислота – в медицине - муравьиный спирт (1,25% спиртовой раствор муравьиной кислоты), в пчеловодстве, в органическом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя.
Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество.
Масляная кислота – для получения ароматизирующих добавок, пластификаторов и флотореагентов.
Щавелевая кислота – в металлургической промышленности (удаление окалины).
Стеариновая C 17 H 35 COOH и пальмитиновая кислота C 15 H 31 COOH – в качестве поверхностно-активных веществ, смазочных материалов в металлообработке.
Олеиновая кислота C 17 H 33 COOH – флотореагент и собиратель при обогащении руд цветных металлов.
Отдельные представители
одноосновных предельных карбоновых кислот
Муравьиная кислота
впервые была
выделена в XVII веке из красных лесных муравьев. Содержится также в соке жгучей
крапивы. Безводная муравьиная кислота – бесцветная жидкость с острым запахом и
жгучим вкусом, вызывающая ожоги на коже. Применяется в текстильной
промышленности в качестве протравы при крашении тканей, для дубления кож, а
также для различных синтезов.
Уксусная
кислота
широко распространена в природе – содержится в выделениях
животных (моче, желчи, испражнениях), в растениях (в зеленых листьях).
Образуется при брожении, гниении, скисании вина, пива, содержится в кислом
молоке и сыре. Температура плавления безводной уксусной кислоты + 16,5°C,
кристаллы ее прозрачны как лед, поэтому ее называют ледяной уксусной кислотой.
Впервые получена в конце XVIII века русским ученым Т. Е. Ловицем. Натуральный
уксус содержит около 5% уксусной кислоты. Из него приготовляют уксусную
эссенцию, используемую в пищевой промышленности для консервирования овощей,
грибов, рыбы. Уксусная кислота широко используется в химической промышленности
для различных синтезов.
Представители ароматических и непредельных карбоновых кислот
Бензойная кислота
C
6 H
5 COOH
- наиболее важный представитель
ароматических кислот. Распространена в природе в растительном мире: в
бальзамах, ладане, эфирных маслах. В животных организмах она содержится в
продуктах распада белковых веществ. Это кристаллическое вещество, температура
плавления 122°C, легко возгоняется. В холодной воде растворяется плохо. Хорошо
растворяется в спирте и эфире.
Ненасыщенные непредельные кислоты с одной двойной связью в молекуле имеют общую формулу C n H 2 n -1 COOH .
Высокомолекулярные непредельные кислоты
часто
упоминаются диетологами (они называют их ненасыщенными). Самая распространенная
из них – олеиновая
СН 3 –(СН 2) 7 –СН=СН–(СН 2) 7 –СООН
или C
17 H
33 COOH
. Она представляет собой бесцветную жидкость,
затвердевающую на холоде.
Особенно важны полиненасыщенные кислоты с несколькими двойными связями: линолевая
СН 3 –(СН 2) 4 –(СН=СН–СН 2) 2 –(СН 2) 6 –СООН
или C
17 H
31 COOH
с двумя двойными связями, линоленовая
СН 3 –СН 2 –(СН=СН–СН 2) 3 –(СН 2) 6 –СООН
или C
17 H
29 COOH
с тремя двойными связями и арахидоновая
СН 3 –(СН 2) 4 –(СН=СН–СН 2) 4 –(СН 2) 2 –СООН
с четырьмя двойными связями; их часто называют незаменимыми жирными кислотами.
Именно эти кислоты обладают наибольшей биологической активностью: они участвуют
в переносе и обмене холестерина, синтезе простагландинов и других жизненно
важных веществ, поддерживают структуру клеточных мембран, необходимы для работы
зрительного аппарата и нервной системы, влияют на иммунитет. Отсутствие в пище
этих кислот тормозит рост животных, угнетает их репродуктивную функцию,
вызывает различные заболевания. Линолевую и линоленовую кислоты организм
человека сам синтезировать не может и должен получать их готовыми с пищей (как
витамины). Для синтеза же арахидоновой кислоты в организме необходима линолевая
кислота. Полиненасыщенные жирные кислоты с 18 атомами углерода в виде эфиров
глицерина находятся в так называемых высыхающих маслах – льняном, конопляном,
маковом и др. Линолевая кислота
C
17 H
31 COOH
и линоленовая
кислота
C
17 H
29 COOH
входят в состав
растительных масел. Например, льняное масло содержит около 25% линолевой
кислоты и до 58% линоленовой.
Сорбиновая (2,4-гексадиеновая) кислота СН 3 –СН=СН–СН=СНСООН была получена из ягод рябины (на латыни – sorbus). Эта кислота – прекрасный консервант, поэтому ягоды рябины не плесневеют.
Простейшая непредельная кислота, акриловая СН 2 =СНСООН, имеет острый запах (на латыни acris – острый, едкий). Акрилаты (эфиры акриловой кислоты) используются для получения органического стекла, а ее нитрил (акрилонитрил) – для изготовления синтетических волокон.
Называя вновь выделенные кислоты, химики, нередко, дают волю фантазии. Так, название ближайшего гомолога акриловой кислоты, кротоновой
СН 3 –СН=СН–СООН, происходит вовсе не от крота, а от растения Croton tiglium , из масла которого она была выделена. Очень важен синтетический изомер кротоновой кислоты – метакриловая кислота СН 2 =С(СН 3)–СООН, из эфира которой (метилметакрилата), как и из метилакрилата, делают прозрачную пластмассу – оргстекло.
Непредельные карбоновые кислоты способны к реакциям присоединения:
СН 2 =СН-СООН + Н 2 → СН 3 -СН 2 -СООН
СН 2 =СН-СООН + Сl 2 → СН 2 Сl -СНСl -СООН
ВИДЕО:
СН 2 =СН-СООН + HCl → СН 2 Сl -СН 2 -СООН
СН 2 =СН-СООН + Н 2 O → НО-СН 2 -СН 2 -СООН
Две последние реакции протекают против правила Марковникова.
Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации.