МОДУЛЬ 1 СТРОЕНИЕ, СВОЙСТВА И ФУНКЦИИ БЕЛКОВ
МОДУЛЬ 1 СТРОЕНИЕ, СВОЙСТВА И ФУНКЦИИ БЕЛКОВ
Структура модуля | Темы |
Модульная единица 1 | 1.1. Структурная организация белков. Этапы формирования нативной конформации белков 1.2. Основы функционирования белков. Лекарства как лиганды, влияющие на функцию белков 1.3. Денатурация белков и возможность их спонтанной ренативации |
Модульная единица 2 | 1.4. Особенности строения и функционирования олигомерных белков на примере гемоглобина 1.5. Поддержание нативной конформации белков в условиях клетки 1.6. Многообразие белков. Семейства белков на примере иммуноглобулинов 1.7. Физико-химические свойства белков и методы их разделения |
Модульная единица 1 СТРУКТУРНАЯ ОРГАНИЗАЦИЯ МОНОМЕРНЫХ БЕЛКОВ И ОСНОВЫ ИХ ФУНКЦИОНИРОВАНИЯ
Цели изучения Уметь:
1. Использовать знания об особенностях структуры белков и зависимости функций белков от их структуры для понимания механизмов развития наследственных и приобретенных протеинопатий.
2. Объяснять механизмы лечебного действия некоторых лекарств как лигандов, взаимодействующих с белками и изменяющих их активность.
3. Использовать знания о строении и конформационной лабильности белков для понимания их структурно-функциональной неустойчивости и склонности к денатурации в изменяющихся условиях.
4. Объяснять применение денатурирующих агентов в качестве средств для стерилизации медицинского материала и инструментов, а также в качестве антисептиков.
Знать:
1. Уровни структурной организации белков.
2. Значение первичной структуры белков, определяющей их структурное и функциональное многообразие.
3. Механизм формирования в белках активного центра и его специфическое взаимодействие с лигандом, лежащее в основе функционирования белков.
4. Примеры влияния экзогенных лигандов (лекарств, токсинов, ядов) на конформацию и функциональную активность белков.
5. Причины и следствия денатурации белков, факторы, вызывающие денатурацию.
6. Примеры использования денатурирующих факторов в медицине в качестве антисептиков и средств для стерилизации медицинских инструментов.
ТЕМА 1.1. СТРУКТУРНАЯ ОРГАНИЗАЦИЯ БЕЛКОВ. ЭТАПЫ ФОРМИРОВАНИЯ НАТИВНОЙ
КОНФОРМАЦИИ БЕЛКОВ
Белки - это полимерные молекулы, мономерами которых являются всего 20 α-аминокислот. Набор и порядок соединения аминокислот в белке определяется строением генов в ДНК индивидумов. Каждый белок в соответствии с его специфической структурой выполняет свойственную ему функцию. Набор белков данного организма определяет его фенотипические особенности, а также наличие наследственных болезней или предрасположенность к их развитию.
1. Аминокислоты, входящие в состав белков. Пептидная связь. Белки - полимеры, построенные из мономеров - 20 α-аминокислот, общая формула которых
Аминокислоты различаются по строению, размерам, физико-химическим свойствам радикалов, присоединенных к α-углеродному атому. Функциональные группы аминокислот определяют особенности свойств разных α-аминокислот. Встречающиеся в α-аминокислотах радикалы можно разделить на несколько групп:
Пролин, в отличие от других 19 мономеров белков, не аминокислота, а иминокислота, радикал в пролине связан как с α-углеродным атомом, так и с иминогруппой
 Аминокислоты различаются по растворимости в воде.
Это связано со способностью радикалов взаимодействовать с водой (гидратироваться).
Аминокислоты различаются по растворимости в воде.
Это связано со способностью радикалов взаимодействовать с водой (гидратироваться).
К гидрофильным относятся радикалы, содержащие анионные, катионные и полярные незаряженные функциональные группы.
К гидрофобным относятся радикалы, содержащие метильные группы, алифатические цепи или циклы.
2. Пептидные связи соединяют аминокислоты в пептиды. При синтезе пептида α-карбоксильная группа одной аминокислоты взаимодействует с α-аминогруппой другой аминокислоты с образованием пептидной связи:
Белки представляют собой полипептиды, т.е. линейные полимеры α-аминокислот, соединенных пептидной связью (рис. 1.1.)
 Рис. 1.1. Термины, используемые при описании строения пептидов
Рис. 1.1. Термины, используемые при описании строения пептидов
Мономеры аминокислот, входящих в состав полипептидов, называются аминокислотными остатками. Цепь повторяющихся групп -NH-CH-CO - образует пептидный остов. Аминокислотный остаток, имеющий свободную α-аминогруппу, называется N-концевым, а имеющий свободную α-карбоксильную группу - С-концевым. Пептиды записывают и читают с N-конца к С-концу.
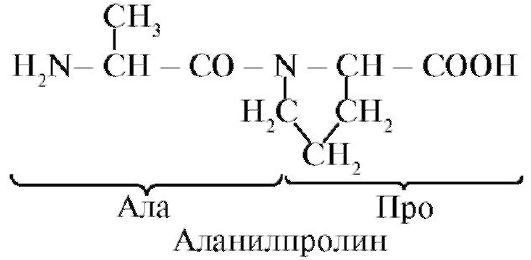
Пептидная связь, образуемая иминогруппой пролина, отличается от других пептидных связей: у атома азота пептидной группы отсутствует водород,
вместо него имеется связь с радикалом, в результате одна сторона цикла включается в пептидный остов:
 Пептиды
различаются аминокислотным составом, количеством аминокислот и порядком
соединения аминокислот, например, Сер-Ала-Глу-Гис и Гис-Глу-Ала-Сер -
два разных пептида.
Пептиды
различаются аминокислотным составом, количеством аминокислот и порядком
соединения аминокислот, например, Сер-Ала-Глу-Гис и Гис-Глу-Ала-Сер -
два разных пептида.
Пептидные связи очень прочные, и для их химического неферментативного гидролиза требуются жесткие условия: анализируемый белок гидролизуют в концентрированной соляной кислоте при температуре около 110° в течение 24 часов. В живой клетке пептидные связи могут разрываться с помощью протеолитических ферментов, называемых протеазами или пептидгидролазами.
3. Первичная структура белков. Аминокислотные остатки в пептидных цепях разных белков чередуются не случайным образом, а расположены в определенном порядке. Линейная последовательность или порядок чередования аминокислотных остатков в полипептидной цепи называется первичной структурой белка.
Первичная структура каждого индивидуального белка закодирована в молекуле ДНК (в участке, называемом геном) и реализуется в ходе транскрипции (переписывания информации на мРНК) и трансляции (синтез первичной структуры белка). Следовательно, первичная структура белков индивидуального человека - наследственно передаваемая от родителей детям информация, определяющая особенности строения белков данного организма, от которых зависит функция имеющихся белков (рис. 1.2.).
 Рис. 1.2. Взаимосвязь между генотипом и конформацией белков, синтезирующихся в организме индивидума
Рис. 1.2. Взаимосвязь между генотипом и конформацией белков, синтезирующихся в организме индивидума
Каждый из примерно 100 000 индивидуальных белков в организме человека имеет уникальную первичную структуру. В молекулах одного типа белка (например, альбумина) одинаковое чередование аминокислотных остатков, что отличает альбумин от любого другого индивидуального белка.
Последовательность аминокислотных остатков в пептидной цепи можно рассматривать как форму записи информации. Эта информация определяет пространственную укладку линейной пептидной цепи в более компактную трехмерную структуру, называемую конформацией белка. Процесс формирования функционально активной конформации белка носит название фолдинг.
4. Конформация белков. Свободное вращение в пептидном остове возможно между атомом азота пептидной группы и соседним α-углеродным атомом, а также между α-углеродным атомом и углеродом карбонильной группы. Вследствие взаимодействия функциональных групп аминокислотных остатков первичная структура белков может приобретать более сложные пространственные структуры. В глобулярных белках различают два основных уровня укладки конформации пептидных цепей: вторичную и третичную структуры.
Вторичная структура белков - это пространственная структура, формирующаяся в результате образования водородных связей между функциональными группами -С=О и - NH- пептидного остова. При этом пептидная цепь может приобретать регулярные структуры двух типов: α-спирали и β-структуры.
В α-спирали водородные связи образуются между атомом кислорода карбонильной группы и водородом амидного азота 4-й от него аминокислоты; боковые цепи аминокислотных остатков
располагаются по периферии спирали, не участвуя в образовании вторичной структуры (рис. 1.3.).
Объемные радикалы или радикалы, несущие одинаковые заряды, препятствуют формированию α-спирали. Остаток пролина, имеющий кольцевую структуру, прерывает α-спираль, так как из-за отсутствия водорода у атома азота в пептидной цепи невозможно образовать водородную связь. Связь между азотом и α-углеродным атомом входит в состав цикла пролина, поэтому пептидный остов в этом месте приобретает изгиб.
β-Структура формируется между линейными областями пептидного остова одной полипептидной цепи, образуя при этом складчатые структуры. Полипептидные цепи или их части могут формировать параллельные или антипараллельные β-структуры. В первом случае N- и С-концы взаимодействующих пептидных цепей совпадают, а во втором - имеют противоположное направление (рис. 1.4).
Рис. 1.3. Вторичная структура белка - α-спираль
 Рис. 1.4. Параллельные и антипараллельные β-складчатые структуры
Рис. 1.4. Параллельные и антипараллельные β-складчатые структуры
β-структуры обозначены широкими стрелками: А - Антипараллельная β-структура. Б - Параллельные β-складчатые структуры
В некоторых белках β-структуры могут формироваться за счет образования водородных связей между атомами пептидного остова разных полипептидных цепей.
В белках также встречаются области с нерегулярной вторичной структурой, к которым относят изгибы, петли, повороты полипептидного остова. Они часто располагаются в местах, где меняется направление пептидной цепи, например, при формировании параллельной β-складчатой структуры.
По наличию α-спиралей и β-структур глобулярные белки могут быть разделены на четыре категории.
Рис. 1.5. Вторичная структура миоглобина (А) и β-цепи гемоглобина (Б), содержащие восемь α-спиралей

 Рис. 1.6. Вторичная структура триозофосфатизомеразы и домена пируваткиназы
Рис. 1.6. Вторичная структура триозофосфатизомеразы и домена пируваткиназы
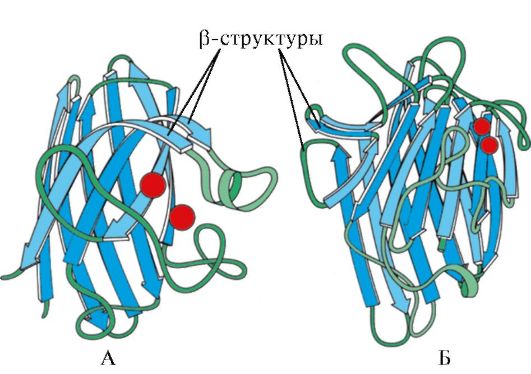 Рис. 1.7. Вторичная структура константного домена иммуноглобулина (А) и фермента супероксиддисмутазы (Б)
Рис. 1.7. Вторичная структура константного домена иммуноглобулина (А) и фермента супероксиддисмутазы (Б)
В четвертую категорию включены белки, имеющие в своем составе незначительное количество регулярных вторичных структур. К таким белкам можно отнести небольшие, богатые цистеином белки или металлопротеины.
Третичная структура белка - тип конформации, образующийся за счет взаимодействий между радикалами аминокислот, которые могут находиться на значительном расстоянии друг от друга в пептидной цепи. Большинство белков при этом формируют пространственную структуру, напоминающую глобулу (глобулярные белки).
Так как гидрофобные радикалы аминокислот имеют тенденцию к объединению с помощью так называемых гидрофобных взаимодействий и межмолекулярных ван-дер-ваальсовых сил, внутри белковой глобулы образуется плотное гидрофобное ядро. Гидрофильные ионизированные и неионизированные радикалы в основном располагаются на поверхности белка и определяют его растворимость в воде.
 Рис. 1.8. Типы связей, возникающих между радикалами аминокислот при формировании третичной структуры белка
Рис. 1.8. Типы связей, возникающих между радикалами аминокислот при формировании третичной структуры белка
1 - ионная связь - возникает между положительно и отрицательно заряженными функциональными группами;
2 - водородная связь - возникает между гидрофильной незаряженной и любой другой гидрофильной группой;
3 - гидрофобные взаимодействия - возникают между гидрофобными радикалами;
4 - дисульфидная связь - формируется за счет окисления SH-групп остатков цистеина и их взаимодействия друг с другом
Гидрофильные аминокислотные остатки, оказавшиеся внутри гидрофобного ядра, могут взаимодействовать друг с другом с помощью ионных и водородных связей (рис. 1.8).
Ионные и водородные связи, а также гидрофобные взаимодействия относятся к числу слабых: их энергия ненамного превышает энергию теплового движения молекул при комнатной температуре. Конформация белка поддерживается за счет возникновения множества таких слабых связей. Так как атомы, из которых состоит белок, находятся в постоянном движении, то возможен разрыв одних слабых связей и образование других, что приводит к небольшим перемещениям отдельных участков полипептидной цепи. Это свойство белков изменять конформацию в результате разрыва одних и образования других слабых связей называется конформационной лабильностью.
В организме человека функционируют системы, поддерживающие гомеостаз - постоянство внутренней среды в определенных допустимых для здорового организма пределах. В условиях гомеостаза небольшие изменения конформации не нарушают общую структуру и функцию белков. Функционально активная конформация белка называется нативной конформацией. Изменение внутренней среды (например, концентрации глюкозы, ионов Са, протонов и т.д.) приводит к изменению конформации и нарушению функций белков.
Третичная структура некоторых белков стабилизирована дисульфидными связями, образующимися за счет взаимодействия -SH групп двух остатков
 Рис. 1.9. Образование дисульфидной связи в молекуле белка
Рис. 1.9. Образование дисульфидной связи в молекуле белка
цистеина (рис. 1.9). Большинство внутриклеточных белков не имеет в третичной структуре ковалентных дисульфидных связей. Их наличие характерно для секретируемых клеткой белков, что обеспечивает их большую стабильность во внеклеточных условиях. Так, дисульфидные связи имеются в молекулах инсулина и иммуноглобулинов.
Инсулин - белковый гормон, синтезирующийся в β-клетках поджелудочной железы и секретируемый в кровь в ответ на повышение концентрации глюкозы в крови. В структуре инсулина имеются две дисульфидные связи, соединяющие полипептидные А- и В-цепи, и одна дисульфидная связь внутри А-цепи (рис. 1.10).
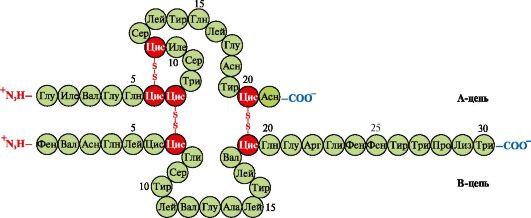 Рис. 1.10. Дисульфидные связи в структуре инсулина
Рис. 1.10. Дисульфидные связи в структуре инсулина
5. Супервторичная структура белков. В разных по первичной структуре и функциям белках иногда выявляются сходные сочетания и взаиморасположение вторичных структур, которые называются супервторичной структурой. Она занимает промежуточное положение между вторичной и третичной структурами, поскольку это специфическое сочетание элементов вторичной структуры при формировании третичной структуры белка. Супервторичные структуры имеют специфические названия, такие как «α-спираль-поворот-а-спираль», «лейциновая застежка молния», «цинковые пальцы» и др. Такие супервторичные структуры характерны для ДНК-связывающих белков.
«Лейциновая застежка-молния». Этот вид супервторичной структуры используется для соединения двух белков. На поверхности взаимодействующих белков имеются α-спиральные участки, содержащие не менее четырех остатков лейцина. Лейциновые остатки в α-спирали располагаются через шесть аминокислот один от другого. Так как каждый виток α-спирали содержит 3,6 аминокислотных остатка, радикалы лейцина находятся на поверхности каждого второго витка. Лейциновые остатки α-спирали одного белка могут взаимодействовать с лейциновыми остатками другого белка (гидрофобные взаимодействия), соединяя их вместе (рис. 1.11.). Многие ДНК связывающие белки функционируют в составе олигомерных комплексов, где отдельные субъединицы связываются друг с другом «лейциновыми застежками».
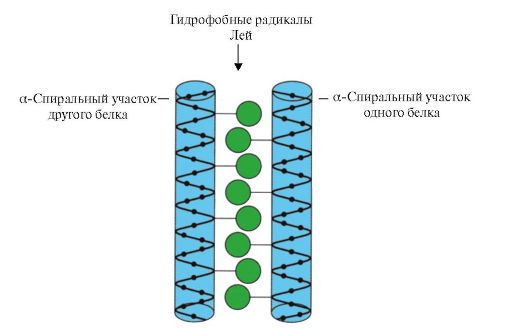 Рис. 1.11. «Лейциновая застежка-молния» между α-спиральными участками двух белков
Рис. 1.11. «Лейциновая застежка-молния» между α-спиральными участками двух белков
Примером таких белков могут служить гистоны. Гистоны - ядерные белки, в состав которых входит большое количество положительно заряженных аминокислот - аргинина и лизина (до 80%). Молекулы гистонов объединяются в олигомерные комплексы, содержащие восемь мономеров с помощью «лейциновых застежек», несмотря на значительный одноименный заряд этих молекул.
«Цинковый палец» - вариант супервторичной структуры, характерный для ДНК-связывающих белков, имеет вид вытянутого фрагмента на поверхности белка и содержит около 20 аминокислотных остатков (рис. 1.12). Форму «вытянутого пальца» поддерживает атом цинка, связанный с радикалами четыре аминокислот - двух остатков цистеина и двух - гистидина. В некоторых случаях вместо остатков гистидина находятся остатки цистеина. Два близко лежащих остатка цистеина отделены от двух других остатков Гисили Циспоследовательностью, состоящей примерно из 12 аминокислотных остатков. Этот участок белка образует α-спираль, радикалы которой могут специфично связываться с регуляторными участками большой бороздки ДНК. Специфичность связывания индивидуального
 Рис.
1.12. Первичная структура участка ДНК-связывающих белков, формирующих
структуру «цинкового пальца» (буквами обозначены аминокислоты, входящие в
состав этой структуры)
Рис.
1.12. Первичная структура участка ДНК-связывающих белков, формирующих
структуру «цинкового пальца» (буквами обозначены аминокислоты, входящие в
состав этой структуры)
регуляторного ДНК-связывающего белка зависит от последовательности аминокислотных остатков, расположенных в области «цинкового пальца». Такие структуры содержат, в частности, рецепторы стероидных гормонов, участвующих в регуляции транскрипции (считывание информации с ДНК на РНК).
ТЕМА 1.2. ОСНОВЫ ФУНКЦИОНИРОВАНИЯ БЕЛКОВ. ЛЕКАРСТВА КАК ЛИГАНДЫ, ВЛИЯЮЩИЕ НА ФУНКЦИЮ БЕЛКОВ
1. Активный центр белка и его взаимодействие с лигандом. В процессе формирования третичной структуры на поверхности функционально активного белка, обычно в углублении, образуется участок, сформированный радикалами аминокислот, далеко стоящими друг от друга в первичной структуре. Этот участок, имеющий уникальное строение для данного белка и способный специфично взаимодействовать с определенной молекулой или группой похожих молекул, называется центром связывания белка с лигандом или активным центром. Лигандами называются молекулы, взаимодействующие с белками.
Высокая специфичность взаимодействия белка с лигандом обеспечивается комплементарностью структуры активного центра структуре лиганда.
Комплементарность - это пространственное и химическое соответствие взаимодействующих поверхностей. Активный центр должен не только пространственно соответствовать входящему в него лиганду, но и между функциональными группами радикалов, входящих в активный центр, и лигандом должны образоваться связи (ионные, водородные, а также гидрофобные взаимодействия), которые удерживают лиганд в активном центре (рис. 1.13).
 Рис. 1.13. Комплементарное взаимодействие белка с лигандом
Рис. 1.13. Комплементарное взаимодействие белка с лигандом
Некоторые лиганды, присоединяясь к активному центру белка, выполняют вспомогательную роль в функционировании белков. Такие лиганды называются кофакторами, а белки, имеющие в своем составе небелковую часть, - сложными белками (в отличие от простых белков, состоящих только из белковой части). Небелковая часть, прочно соединенная с белком, носит название простетической группы. Например, в составе миоглобина, гемоглобина и цитохромов содержится прочно прикрепленная к активному центру простетическая группа - гем, содержащий ион железа. Сложные белки, содержащие гем, называются гемопротеинами.
При присоединении к белкам специфических лигандов проявляется функция этих белков. Так, альбумин - важнейший белок плазмы крови - проявляет свою транспортную функцию, присоединяя к активному центру гидрофобные лиганды, такие как жирные кислоты, билирубин, некоторые лекарства и др. (рис. 1.14)
Лигандами, взаимодействующими с трехмерной структурой пептидной цепи, могут быть не только низкомолекулярные органические и неорганические молекулы, но и макромолекулы:
ДНК (рассмотренные выше примеры с ДНК-связывающими белками);
Полисахариды;
 Рис. 1.14. Взаимосвязь генотипа и фенотипа
Рис. 1.14. Взаимосвязь генотипа и фенотипа
Уникальная первичная структура белков человека, закодированная в молекуле ДНК, в клетках реализуется в виде уникальной конформации, структуры активного центра и функций белков
В этих случаях белок узнает определенный участок лиганда, соразмерный и комплементарный центру связывания. Так на поверхности гепатоцитов имеются белки-рецепторы к гормону инсулину, имеющему также белковое строение. Взаимодействие инсулина с рецептором вызывает изменение его конформации и активации сигнальных систем, приводящих к запасанию в гепатоцитах питательных веществ после еды.
Таким образом, в основе функционирования белков лежит специфическое взаимодействие активного центра белка с лигандом.
2. Доменная структура и ее роль в функционировании белков. Длинные полипептидные цепи глобулярных белков часто складываются в несколько компактных, относительно независимых областей. Они имеют самостоятельную третичную структуру, напоминающую таковую у глобулярных белков, и называются доменами. Благодаря доменной структуре белков легче формируется их третичная структура.
В доменных белках центры связывания с лигандом часто располагаются между доменами. Так, трипсин - протеолитический фермент, который вырабатывается экзокринной частью поджелудочной железы и необходим для переваривания белков пищи. Он имеет двухдоменное строение, а центр связывания трипсина с его лигандом - пищевым белком - располагается в бороздке между двумя доменами. В активном центре создаются условия, необходимые для эффективного связывания специфического участка пищевого белка и гидролиза его пептидных связей.
Разные домены в белке при взаимодействии активного центра с лигандом могут перемещаться друг относительно друга (рис. 1.15).
Гексокиназа - фермент, катализирующий фосфорилирование глюкозы с помощью АТФ. Активный центр фермента располагается в расщелине между двумя доменами. При связывании гексокиназы с глюкозой окружающие ее домены смыкаются и субстрат оказывается в «ловушке», где и происходит фосфорилирование (см. рис. 1.15).
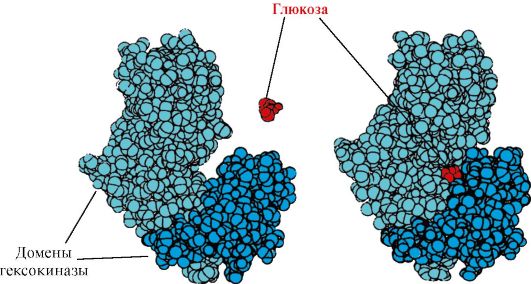 Рис. 1.15. Связывание доменов гексокиназы с глюкозой
Рис. 1.15. Связывание доменов гексокиназы с глюкозой
В некоторых белках домены выполняют самостоятельные функции, связываясь с различными лигандами. Такие белки называются многофункциональными.
3. Лекарства - лиганды, влияющие на функцию белков. Взаимодействие белков с лигандами специфично. Однако благодаря конформационной лабильности белка и его активного центра можно подобрать другое вещество, которое также могло бы взаимодействовать с белком в активном центре или ином участке молекулы.
Вещество, по структуре похожее на природный лиганд, называют структурным аналогом лиганда или неприродным лигандом. Оно также взаимодействует с белком в активном центре. Структурный аналог лиганда может как усиливать функцию белка (агонист), так и снижать ее (антагонист). Лиганд и его структурные аналоги конкурируют друг с другом за связывание с белком в одном центре. Такие вещества называются конкурентными модуляторами (регуляторами) белковых функций. Многие лекарственные препараты действуют как ингибиторы белков. Некоторые из них получают химической модификацией природных лигандов. Ингибиторы белковых функций могут быть лекарствами и ядами.
Атропин - конкурентный ингибитор М-холинорецепторов. Ацетилхолин - нейромедиатор передачи нервного импульса через холинэргические синапсы. Для проведения возбуждения выделившийся в синаптическую щель ацетилхолин должен взаимодействовать с белком - рецептором постсинаптической мембраны. Обнаружены два типа холинорецепторов:
М-рецептор, кроме ацетилхолина избирательно взаимодействующий с мускарином (токсином мухомора). М - холинорецепторы имеются на гладких мышцах и при взаимодействии с ацетилхолином вызывают их сокращение;
Н-рецептор, специфично связывающийся с никотином. Н-холинорецепторы обнаружены в синапсах поперечнополосатых скелетных мышц.
Специфическим ингибитором М-холинорецепторов является атропин. Он содержится в растениях красавке и белене.
 Атропин
имеет в структуре схожие с ацетилхолином функциональные группы и их
пространственное расположение, поэтому относится к конкурентным
ингибиторам М-холинорецепторов. Учитывая, что связывание ацетилхолина с
М-холинорецепторами вызывает сокращение гладких мышц, атропин используют
как лекарство, снимающее их спазм (спазмолитик).
Так, известно
применение атропина для расслабления глазных мышц при просмотре глазного
дна, а также для снятия спазмов при желудочнокишечных коликах.
М-холинорецепторы имеются и в центральной нервной системе (ЦНС), поэтому
большие дозы атропина могут вызвать нежелательную реакцию со стороны
ЦНС: двигательное и психическое возбуждение, галлюцинации, судороги.
Атропин
имеет в структуре схожие с ацетилхолином функциональные группы и их
пространственное расположение, поэтому относится к конкурентным
ингибиторам М-холинорецепторов. Учитывая, что связывание ацетилхолина с
М-холинорецепторами вызывает сокращение гладких мышц, атропин используют
как лекарство, снимающее их спазм (спазмолитик).
Так, известно
применение атропина для расслабления глазных мышц при просмотре глазного
дна, а также для снятия спазмов при желудочнокишечных коликах.
М-холинорецепторы имеются и в центральной нервной системе (ЦНС), поэтому
большие дозы атропина могут вызвать нежелательную реакцию со стороны
ЦНС: двигательное и психическое возбуждение, галлюцинации, судороги.
Дитилин - конкурентный агонист Н-холинорецепторов, ингибирующий функцию нервно-мышечных синапсов.
 Нервно-мышечные
синапсы скелетных мышц содержат Н-холинорецепторы. Их взаимодействие с
ацетилхолином приводит к мышечным сокращениям. При некоторых
хирургических операциях, а также в эндоскопических исследованиях
используют препараты, вызывающие расслабление скелетных мышц (миорелаксанты).
К
ним относится дитилин, являющийся структурным аналогом ацетилхолина. Он
присоединяется к Н-холинорецепторам, но в отличие от ацетилхолина очень
медленно разрушается ферментом - ацетилхолинэстеразой. В результате
длительного открытия ионных каналов и стойкой деполяризации мембраны
нарушается проведение нервного импульса и происходит мышечное
расслабление. Первоначально эти свойства были обнаружены у яда кураре,
поэтому такие препараты называют курареподобными.
Нервно-мышечные
синапсы скелетных мышц содержат Н-холинорецепторы. Их взаимодействие с
ацетилхолином приводит к мышечным сокращениям. При некоторых
хирургических операциях, а также в эндоскопических исследованиях
используют препараты, вызывающие расслабление скелетных мышц (миорелаксанты).
К
ним относится дитилин, являющийся структурным аналогом ацетилхолина. Он
присоединяется к Н-холинорецепторам, но в отличие от ацетилхолина очень
медленно разрушается ферментом - ацетилхолинэстеразой. В результате
длительного открытия ионных каналов и стойкой деполяризации мембраны
нарушается проведение нервного импульса и происходит мышечное
расслабление. Первоначально эти свойства были обнаружены у яда кураре,
поэтому такие препараты называют курареподобными.
ТЕМА 1.3. ДЕНАТУРАЦИЯ БЕЛКОВ И ВОЗМОЖНОСТЬ ИХ СПОНТАННОЙ РЕНАТИВАЦИИ
1. Так как нативная конформация белков поддерживается за счет слабых взаимодействий, изменение состава и свойств окружающей белок среды, воздействие химических реагентов и физических факторов вызывают изменение их конформации (свойство конформационной лабильности). Разрыв большого количества связей приводит к разрушению нативной конформации и денатурации белков.
Денатурация белков - это разрушение их нативной конформации под действием денатурирующих агентов, вызванное разрывом слабых связей, стабилизирующих пространственную структуру белка. Денатурация сопровождается разрушением уникальной трехмерной структуры и активного центра белка и потерей его биологической активности (рис. 1.16).
Все денатурированные молекулы одного белка приобретают случайную конформацию, отличающуюся от других молекул того же белка. Радикалы аминокислот, формирующие активный центр, оказываются пространственно удаленными друг от друга, т.е. разрушается специфический центр связывания белка с лигандом. При денатурации первичная структура белков остается неизменной.
Применение денатурирующих агентов в биологических исследованиях и медицине. В биохимических исследованиях перед определением в биологическом материале низкомолекулярных соединений обычно из раствора вначале удаляют белки. Для этой цели чаще всего используют трихлоруксусную кислоту (ТХУ). После добавления ТХУ в раствор денатурированные белки выпадают в осадок и легко удаляются фильтрованием (табл. 1.1.)
В медицине денатурирующие агенты часто применяют для стерилизации медицинского инструмента и материала в автоклавах (денатурирующий агент - высокая температура) и в качестве антисептиков (спирт, фенол, хлорамин) для обработки загрязненных поверхностей, содержащих патогенную микрофлору.
2. Спонтанная ренативация белков - доказательство детерминированности первичной структуры, конформации и функции белков. Индивидуальные белки - это продукты одного гена, которые имеют идентичную аминокислотную последовательность и в клетке приобретают одинаковую конформацию. Фундаментальный вывод о том, что в первичной структуре белка уже заложена информация о его конформации и функции, был сделан на основе способности некоторых белков (в частности, рибонуклеазы и миоглобина) к спонтанной ренативации - восстановлению их нативной конформации после денатурации.
Формирование пространственных структур белка осуществляется способом самосборки - самопроизвольного процесса, при котором полипептидная цепь, имеющая уникальную первичную структуру, стремится принять в растворе конформацию с наименьшей свободной энергией. Способность к ренативации белков, сохраняющих после денатурации первичную структуру, описана в опыте с ферментом рибонуклеазой.
Рибонуклеаза - фермент, разрушающий связи между отдельными нуклеотидами в молекуле РНК. Этот глобулярный белок имеет одну полипептидную цепь, третичная структура которой стабилизирована множеством слабых и четырьмя дисульфидными связями.
Обработка рибонуклеазы мочевиной, разрушающей водородные связи в молекуле, и восстановителем, разрывающим дисульфидные связи, приводит к денатурации фермента и потере его активности.
Удаление денатурирующих агентов диализом приводит к восстановлению конформации и функции белка, т.е. к ренативации. (рис. 1.17).
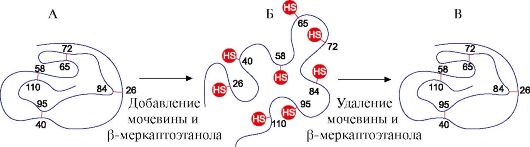 Рис. 1.17. Денатурация и ренативация рибонуклеазы
Рис. 1.17. Денатурация и ренативация рибонуклеазы
А - нативная конформация рибонуклеазы, в третичной структуре которой имеются четыре дисульфидные связи; Б - денатурированная молекула рибонуклеазы;
В - ренативированная молекула рибонуклеазы с восстановленной структурой и функцией
1. Заполните таблицу 1.2.
Таблица 1.2. Классификация аминокислот по полярности радикалов
2. Напишите формулу тетрапептида:
Асп - Про - Фен - Лиз
а) выделите в пептиде повторяющиеся группы, образующие пептидный остов, и вариабельные группы, представленные радикалами аминокислот;
б) обозначьте N- и С-концы;
в) подчеркните пептидные связи;
г) напишите другой пептид, состоящий из тех же аминокислот;
д) подсчитайте количество возможных вариантов тетрапептида с аналогичным аминокислотным составом.
3. Объясните роль первичной структуры белков на примере сравнительного анализа двух сходных по структуре и эволюционно близких пептидных гормонов нейрогипофиза млекопитающих - окситоцина и вазопрессина (табл. 1.3).
Таблица 1.3. Структура и функции окситоцина и вазопрессина
 Для этого:
Для этого:
а) сравните состав и последовательность аминокислот двух пептидов;
б) найдите сходство первичной структуры двух пептидов и сходство их биологического действия;
в) найдите различия в структуре двух пептидов и различие их функций;
г) сделайте вывод о влиянии первичной структуры пептидов на их функции.
4. Опишите основные этапы формирования конформации глобулярных белков (вторичная, третичная структуры, понятие о супервторичной структуре). Укажите типы связей, участвующих в формировании структур белка. Радикалы каких аминокислот могут участвовать в образовании гидрофобных взаимодействий, ионных, водородных связях.
Приведите примеры.
5. Дайте определение понятию «конформационная лабильность белков», укажите причины ее существования и значение.
6. Раскройте смысл следующей фразы: «В основе функционирования белков лежит их специфическое взаимодействие с лигандом», используя термины и объясняя их значение: конформация белка, активный центр, лиганд, комплементарность, функция белка.
7. На одном из примеров объясните, что такое домены и какова их роль в функционировании белков.
ЗАДАНИЯ ДЛЯ САМОКОНТРОЛЯ
1. Установите соответствие.
Функциональная группа в радикале аминокислоты:
А. Карбоксильная группа Б. Гидроксильная группа В Гуанидиновая группа Г. Тиольная группа Д. Аминогруппа
2. Выберите правильные ответы.
Аминокислоты с полярными незаряженными радикалами - это:
A. Цис Б. Асн
B. Глу Г. Три
3. Выберите правильные ответы.
Радикалы аминокислот:
A. Обеспечивают специфичность первичной структуры Б. Участвуют в формировании третичной структуры
B. Располагаясь на поверхности белка, влияют на его растворимость Г. Формируют активный центр
Д. Участвуют в образовании пептидных связей
4. Выберите правильные ответы.
Гидрофобные взаимодействия могут образовываться между радикалами аминокислот:
A. Тре Лей Б. Про Три
B. Мет Иле Г. Тир Ала Д. Вал Фен
5. Выберите правильные ответы.
Ионные связи могут образовываться между радикалами аминокислот:
A. Глн Асп Б. Apr Лиз
B. Лиз Глу Г. Гис Асп Д. Асн Apr
6. Выберите правильные ответы.
Водородные связи могут образовываться между радикалами аминокислот:
A. Сер Глн Б. Цис Тре
B. Асп Лиз Г. Глу Асп Д. Асн Тре
7. Установите соответствие.
Тип связи, участвующий в формировании структуры белка:
A. Первичная структура Б. Вторичная структура
B. Третичная структура
Г. Супервторичная структура Д. Конформация.
1. Водородные связи между атомами пептидного остова
2. Слабые связи между функциональными группами радикалов аминокислот
3. Связи между α-амино и α-карбоксильными группами аминокислот
8. Выберите правильные ответы. Трипсин:
A. Протеолитический фермент Б. Содержит два домена
B. Гидролизирует крахмал
Г. Активный центр расположен между доменами. Д. Состоит из двух полипептидных цепей.
9. Выберите правильные ответы. Атропин:
A. Нейромедиатор
Б. Структурный аналог ацетилхолина
B. Взаимодействует с Н-холинорецепторами
Г. Усиливает проведение нервного импульса через холинэргические синапсы
Д. Конкурентный ингибитор М-холинорецепторов
10. Выберите правильные утверждения. В белках:
A. Первичная структура содержит информацию о строении его активного центра
Б. Активный центр формируется на уровне первичной структуры
B. Конформация жестко фиксирована ковалентными связями
Г. Активный центр может взаимодействовать с группой похожих лигандов
благодаря конформационной лабильности белков Д. Изменение окружающей среды, может влиять на сродство активного
центра к лиганду
1. 1-В, 2-Г, 3-Б.
3. А, Б, В, Г.
7. 1-Б, 2-Д, 3-А.
8. А, Б, В, Г.
ОСНОВНЫЕ ТЕРМИНЫ И ПОНЯТИЯ
1. Белок, полипептид, аминокислоты
2. Первичная, вторичная, третичная структуры белка
3. Конформация, нативная конформация белка
4. Ковалентные и слабые связи в белке
5. Конформационная лабильность
6. Активный центр белка
7. Лиганды
8. Фолдинг белков
9. Структурные аналоги лигандов
10. Доменные белки
11. Простые и сложные белки
12. Денатурация белка, денатурирующие агенты
13. Ренативация белков
Решите задачи
«Структурная организация белков и основы их функционирования»
1. Основная функция белка - гемоглобина А (НвА) - транспорт кислорода к тканям. В популяции людей известны множественные формы этого белка с измененными свойствами и функцией - так называемые аномальные гемоглобины. Например, установлено, что гемоглобин S, обнаруженный в эритроцитах больных серповидно-клеточной анемией (HbS), имеет низкую растворимость в условиях низкого парциального давления кислорода (как это имеет место в венозной крови). Это приводит к образованию агрегатов данного белка. Белок утрачивает свою функцию, выпадает в осадок, а эритроциты приобретают неправильную форму (некоторые из них образуют форму серпа) и быстрее обычного разрушаются в селезенке. В результате развивается серповидноклеточная анемия.
Единственное различие в первичной структуре НвА и обнаружено в N-концевом участке β-цепи гемоглобина. Сравните N-концевые участки β-цепи и покажите, как изменения в первичной структуре белка влияют на его свойства и функции.
 Для этого:
Для этого:
а) напишите формулы аминокислот, по которым различаются НвА и сравните свойства этих аминокислот (полярность, заряд).
б) сделайте вывод о причине снижения растворимости и нарушении транспорта кислорода в ткани.
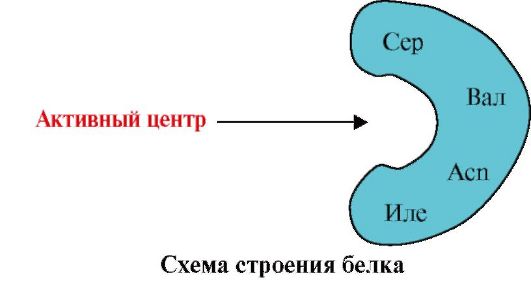
2. На рисунке представлена схема строения белка, имеющего центр связывания с лигандом (активный центр). Объясните, почему белок обладает избирательностью в выборе лиганда. Для этого:
а) вспомните, что такое активный центр белка, и рассмотрите строение активного центра белка, представленного на рисунке;
б) напишите формулы радикалов аминокислот, входящих в состав активного центра;
в) нарисуйте лиганд, который мог бы специфически взаимодействовать с активным центром белка. Укажите на нем функциональные группы, способные образовать связи с радикалами аминокислот, входящих в состав активного центра;
г) укажите типы связей, возникающих между лигандом и радикалами аминокислот активного центра;
д) объясните, на чем основана специфичность взаимодействия белка с лигандом.
 3.
На рисунке представлен активный центр белка и несколько лигандов.
3.
На рисунке представлен активный центр белка и несколько лигандов.
Определите, какой из лигандов с наибольшей вероятностью будет взаимодействовать с активным центром белка и почему.
 Какие типы связей возникают в процессе образования комплекса белок-лиганд»?
Какие типы связей возникают в процессе образования комплекса белок-лиганд»?
4. Структурные аналоги естественных лигандов белков могут использоваться в качестве лекарственных препаратов для изменения активности белков.
Ацетилхолин - медиатор передачи возбуждения в нервно-мышечных синапсах. При взаимодействии ацетилхолина с белками - рецепторами постсинаптической мембраны скелетных мышц происходит открытие ионных каналов и мышечное сокращение. Дитилин - лекарство, применяемое при некоторых операциях для расслабления мышц, так как он нарушает передачу нервного импульса через нервно-мышечные синапсы. Объясните механизм действия дитилина как миорелаксирующего препарата. Для этого:
а) напишите формулы ацетилхолина и дитилина и сравните их структуры;
б) опишите механизм расслабляющего действия дитилина.
5. При некоторых заболеваниях у больного повышается температура тела, что рассматривают как защитную реакцию организма. Однако высокие температуры губительны для белков организма. Объясните, почему при температуре выше 40 °С нарушается функция белков и возникает угроза для жизни человека. Для этого вспомните:
1) Строение белков и связи, удерживающие его структуру в нативной конформации;
2) Как меняется структура и функция белков при повышении температуры?;
3) Что такое гомеостаз и почему он важен для поддержания здоровья человека.
Модульная единица 2 ОЛИГОМЕРНЫЕ БЕЛКИ КАК МИШЕНИ РЕГУЛЯТОРНЫХ ВОЗДЕЙСТВИЙ. СТРУКТУРНО-ФУНКЦИОНАЛЬНОЕ МНОГООБРАЗИЕ БЕЛКОВ. МЕТОДЫ РАЗДЕЛЕНИЯ И ОЧИСТКИ БЕЛКОВ
Цели изучения Уметь:
1. Использовать знания об особенностях структуры и функций олигомерных белков для понимания адаптивных механизмов регуляции их функций.
2. Объяснять роль шаперонов в синтезе и поддержании конформации белков в условиях клетки.
3. Объяснять многообразие проявления жизни многообразием структур и функций синтезирующихся в организме белков.
4. Анализировать связь структуры белков с их функцией на примерах сравнения родственных гемопротеинов - миоглобина и гемоглобина, а также представителей пяти классов белков семейства иммуноглобулинов.
5. Применять знания об особенностях физико-химических свойств белков для выбора методов их очистки от других белков и примесей.
6. Интерпретировать результаты количественного и качественного состава белков плазмы крови для подтверждения или уточнения клинического диагноза.
Знать:
1. Особенности строения олигомерных белков и адаптивные механизмы регуляции их функций на примере гемоглобина.
2. Строение и функции шаперонов и их значение для поддержания нативной конформации белков в условиях клетки.
3. Принципы объединения белков в семейства по схожести их конформации и функций на примере иммуноглобулинов.
4. Методы разделения белков, основанные на особенностях их физикохимических свойств.
5. Электрофорез плазмы крови как метод оценки качественного и количественного состава белков.
ТЕМА 1.4. ОСОБЕННОСТИ СТРОЕНИЯ И ФУНКЦИОНИРОВАНИЯ ОЛИГОМЕРНЫХ БЕЛКОВ НА ПРИМЕРЕ ГЕМОГЛОБИНА
1. Многие белки имеют в своем составе несколько полипептидных цепей. Такие белки называют олигомерными, а отдельные цепи - протомерами. Протомеры в олигомерных белках соединены множеством слабых нековалентных связей (гидрофобных, ионных, водородных). Взаимодействие
протомеров осуществляется благодаря комплементарности их контактирующих поверхностей.
Количество протомеров в олигомерных белках может сильно варьировать: гемоглобин содержит 4 протомера, фермент аспартатаминотрансфераза - 12 протомеров, а в белок вируса табачной мозаики входит 2120 протомеров, соединенных нековалентными связями. Следовательно, олигомерные белки могут иметь очень большую молекулярную массу.
Взаимодействие одного протомера с другими можно рассматривать как частный случай взаимодействия белка с лигандом, так как каждый протомер служит лигандом для других протомеров. Количество и способ соединения протомеров в белке называется четвертичной структурой белка.
В состав белков могут входить одинаковые или разные по строению протомеры, например, гомодимеры - белки, содержащие два одинаковых протомера, а гетеродимеры - белки, содержащие два разных протомера.
Если в состав белков входят разные протомеры, то на них могут формироваться отличающиеся по структуре центры связывания с разными лигандами. При связывании лиганда с активным центром проявляется функция данного белка. Центр, расположенный на другом протомере, называется аллостерическим (другим, отличным от активного). Связываясь с аллостерическим лигандом или эффектором, он выполняет регуляторную функцию (рис. 1.18). Взаимодействие аллостерического центра с эффектором вызывает конформационные изменения в структуре всего олигомерного белка благодаря его конформационной лабильности. Это влияет на сродство активного центра к специфическому лиганду и регулирует функцию данного белка. Изменение конформации и функции всех протомеров при взаимодействии олигомерного белка хотя бы с одним лигандом носит название кооперативных изменений конформации. Эффекторы, усиливающие функцию белка, называются активаторами, а эффекторы, угнетающие его функцию, - ингибиторами.
Таким образом, у олигомерных белков, а также белков, имеющих доменное строение, появляется новое по сравнению с мономерными белками свойство - способность к аллостерической регуляции функций (регуляции присоединением к белку разных лигандов). Это можно проследить, сравнивая структуры и функции двух близко родственных сложных белков миоглобина и гемоглобина.
 Рис. 1.18. Схема строения димерного белка
Рис. 1.18. Схема строения димерного белка
2. Формирование пространственных структур и функционирование миоглобина.
Миоглобин (Мв) - белок, находящийся в красных мышцах, основная функция которого - создание запасов О 2 , необходимых при интенсивной мышечной работе. Мв - сложный белок, содержащий белковую часть - апоМв и небелковую часть - гем. Первичная структура апоМв определяет его компактную глобулярную конформацию и структуру активного центра, к которому присоединяется небелковая часть миоглобина - гем. Кислород, поступающий из крови в мышцы, связывается с Fe+ 2 гема в составе миоглобина. Мв - мономерный белок, имеющий очень высокое сродство к О 2 , поэтому отдача кислорода миоглобином происходит только при интенсивной мышечной работе, когда парциальное давление O 2 резко снижается.
Формирование конформации Мв. В красных мышцах на рибосомах в ходе трансляции идет синтез первичной структуры Мв, представленной специфической последовательностью 153 аминокислотных остатков. Вторичная структура Мв содержит восемь α-спиралей, называемых латинскими буквами от А до Н, между которыми имеются неспирализованные участки. Третичная структура Мв имеет вид компактной глобулы, в углублении которой между F и Е α-спиралями расположен активный центр (рис. 1.19).
 Рис. 1.19. Структура миоглобина
Рис. 1.19. Структура миоглобина
3. Особенности строения и функционирования активного центра Мв. Активный центр Мв сформирован преимущественно гидрофобными радикалами аминокислот, далеко отстоящими друг от друга в первичной структуре (например, Три 3 9 и Фен 138) К активному центру присоединяется плохо растворимые в воде лиганды - гем и О 2 . Гем - специфический лиганд апоМв (рис. 1.20), основу которого составляют четыре пиррольных кольца, соединенных метенильными мостиками; в центре расположен атом Fe+ 2 , соединенный с атомами азота пиррольных колец четырьмя координационными связями. В активном центре Мв кроме гидрофобных радикалов аминокислот имеются также остатки двух аминокислот с гидрофильными радикалами - Гис Е 7 (Гис 64) и Гис F 8 (Гис 93) (рис. 1.21).
 Рис. 1.20. Строение гема - небелковой части миоглобина и гемоглобина
Рис. 1.20. Строение гема - небелковой части миоглобина и гемоглобина
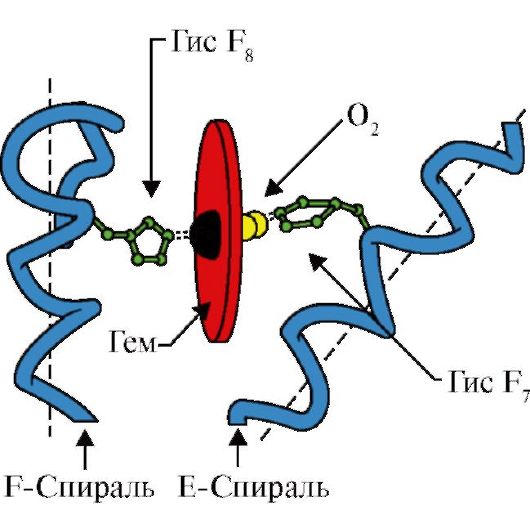 Рис. 1.21. Расположение гема и O 2 в активном центре апомиоглобина и протомеров гемоглобина
Рис. 1.21. Расположение гема и O 2 в активном центре апомиоглобина и протомеров гемоглобина
Гем через атом железа ковалентно связан с Гис F 8 . O 2 присоединяется к железу с другой стороны плоскости гема. Гис Е 7 необходим для правильной ориентации О 2 и облегчает присоединение кислорода к Fe+ 2 гема
Гис F 8 образует координационную связь с Fe+ 2 и прочно фиксирует гем в активном центре. Гис Е 7 необходим для правильной ориентации в активном центре другого лиганда - O 2 при его взаимодействии с Fe+ 2 гема. Микроокружение гема создает условия для прочного, но обратимого связывания O 2 с Fe +2 и препятствует попаданию в гидрофобный активный центр воды, что может привести к его окислению в Fе+ 3 .
Мономерное строение Мв и его активного центра определяет высокое сродство белка к О 2 .
4. Олигомерное строение Нв и регуляция сродства Нв к О 2 лигандами. Гемоглобины человека - семейство белков, так же как и миоглобин относящиеся к сложным белкам (гемопротеинам). Они имеют тетрамерное строение и содержат две α-цепи, но различаются по строению двух других полипептидных цепей (2α-, 2х-цепи). Строение второй полипептидной цепи определяет особенности функционирования этих форм Нв. Около 98% гемоглобина эритроцитов взрослого человека составляет гемоглобин А (2α-, 2р-цепи).
В период внутриутробного развития функционируют два основных типа гемоглобинов: эмбриональный Нв (2α, 2ε), который обнаруживается на ранних этапах развития плода, и гемоглобин F (фетальный) - (2α, 2γ), который приходит на смену раннему гемоглобину плода на шестом месяце внутриутробного развития и только после рождения замещается на Нв А.
Нв А - белок, родственный миоглобину (Мв), содержится в эритроцитах взрослого человека. Строение его отдельных протомеров аналогично таковому у миоглобина. Вторичная и третичная структуры миоглобина и протомеров гемоглобина очень сходны, несмотря на то что в первичной структуре их полипептидных цепей идентичны только 24 аминокислотных остатка (вторичная структура протомеров гемоглобина, так же как миоглобин, содержит восемь α-спиралей, обозначаемых латинскими буквами от А до Н, а третичная структура имеет вид компактной глобулы). Но в отличие от миоглобина гемоглобин имеет олигомерное строение, состоит из четырех полипептидных цепей, соединенных нековалентными связями (рис 1.22).
Каждый протомер Нв связан с небелковой частью - гемом и соседними протомерами. Соединение белковой части Нв с гемом аналогично таковому у миоглобина: в активном центре белка гидрофобные части гема окружены гидрофобными радикалами аминокислот за исключением Гис F 8 и Гис Е 7 , которые расположены по обе стороны от плоскости гема и играют аналогичную роль в функционировании белка и связывании его с кислородом (см. строение миоглобина).
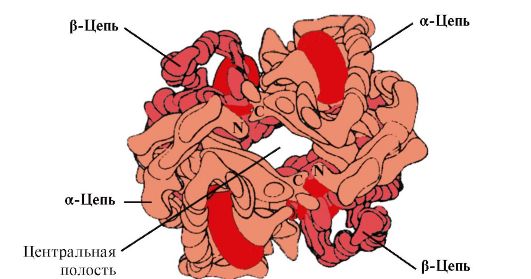 Рис. 1.22. Олигомерная структура гемоглобина
Рис. 1.22. Олигомерная структура гемоглобина
Кроме того, Гис Е 7 выполняет важную дополнительную роль в функционировании Нв. Свободный гем имеет в 25 000 раз более высокое сродство к СО, чем к О 2 . СО в небольших количествах образуется в организме и, учитывая его высокое сродство к гему, он мог бы нарушать транспорт необходимого для жизни клеток О 2 . Однако в составе гемоглобина сродство гема к оксиду углерода превышает сродство к О 2 всего в 200 раз благодаря наличию в активном центре Гис Е 7 . Остаток этой аминокислоты создает оптимальные условия для связывания гема с O 2 и ослабляет взаимодействие гема с СО.
5. Основная функция Нв - транспорт О 2 из легких в ткани. В отличие от мономерного миоглобина, имеющего очень высокое сродство к О 2 и выполняющего функцию запасания кислорода в красных мышцах, олигомерная структура гемоглобина обеспечивает:
1) быстрое насыщение Нв кислородом в легких;
2) способность Нв отдавать кислород в тканях при относительно высоком парциальном давлении O 2 (20-40 мм рт. ст.);
3) возможность регуляции сродства Нв к О 2 .
6. Кооперативные изменения конформации протомеров гемоглобина ускоряют связывание O 2 в легких и отдачу его в ткани. В легких высокое парциальное давление O 2 способствует связыванию его с Нв в активном центре четырех протомеров (2α и 2β). Активный центр каждого протомера, так же как и в миоглобине, расположен между двумя α-спиралями (F и Е) в гидрофобном кармане. Он содержит небелковую часть - гем, прикрепленный к белковой части множеством слабых гидрофобных взаимодействий и одной прочной связью между Fe 2 + гема и Гис F 8 (см. рис. 1.21).
В дезоксигемоглобине, благодаря этой связи с Гис F 8 , атом Fe 2 + выступает из плоскости гема по направлению к гистидину. Связывание O 2 с Fe 2 + происходит по другую сторону гема в области Гис Е 7 с помощью единственной свободной координационной связи. Гис Е 7 обеспечивает оптимальные условия для связывания O 2 с железом гема.
Присоединение O 2 к атому Fe +2 одного протомера вызывает его перемещение в плоскость гема, а за ним и остатка гистидина, связанного с ним
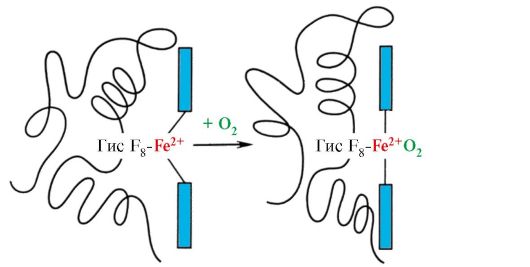 Рис. 1.23. Изменение конформации протомера гемоглобина при соединении с O 2
Рис. 1.23. Изменение конформации протомера гемоглобина при соединении с O 2
Это приводит к изменению конформации всех полипептидных цепей за счет их конформационной лабильности. Изменение конформации других цепей облегчает их взаимодействие со следующими молекулами О 2 .
Четвертая молекула О 2 присоединяется к гемоглобину в 300 раз легче, чем первая (рис. 1.24).
 Рис. 1.24. Кооперативные изменения конформации протомеров гемоглобина при его взаимодействии с О 2
Рис. 1.24. Кооперативные изменения конформации протомеров гемоглобина при его взаимодействии с О 2
В тканях каждая следующая молекула O 2 отщепляется легче, чем предыдущая, также за счет кооперативных изменений конформации протомеров.
7. CO 2 и Н+, образующиеся при катаболизме органических веществ, уменьшают сродство гемоглобина к О 2 пропорционально их концентрации. Энергия, необходимая для работы клеток, вырабатывается преимущественно в митохондриях при окислении органических веществ с использованием O 2 , доставляемого из легких гемоглобином. В результате окисления органических веществ образуются конечные продукты их распада: СО 2 и K 2 O, количество которых пропорционально интенсивности протекающих процессов окисления.
СO 2 диффузией попадает из клеток в кровь и проникает в эритроциты, где под действием фермента карбангидразы превращается в угольную кислоту. Эта слабая кислота диссоциирует на протон и бикарбонат ион.
Н+ способны присоединятся к радикалам Гис 14 6 в α- и β-цепях гемоглобина, т.е. в участках, удаленных от гема. Протонирование гемоглобина снижает его сродство к О 2 , способствует отщеплению О 2 от оксиНв, образованию дезоксиНв и увеличивает поступление кислорода в ткани пропорционально количеству образовавшихся протонов (рис. 1.25).
Увеличение количества освобожденного кислорода в зависимости от увеличения концентрации Н+ в эритроцитах называется эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект).
В легких высокое парциальное давление кислорода способствует его связыванию с дезоксиНв, что уменьшает сродство белка к Н + . Освободившиеся протоны под действием карбангидразы взаимодействуют с бикарбонатами с образованием СО 2 и Н 2 О

 Рис. 1.25. Зависимость сродства Нв к О 2 от концентрации СО 2 и протонов (эффект Бора):
Рис. 1.25. Зависимость сродства Нв к О 2 от концентрации СО 2 и протонов (эффект Бора):
А - влияние концентрации СО 2 и Н+ на высвобождение О 2 из комплекса с Нв (эффект Бора); Б - оксигенирование дезоксигемоглобина в легких, образование и выделение СО 2 .
Образовавшийся СО 2 поступает в альвеолярное пространство и удаляется с выдыхаемым воздухом. Таким образом, количество высвобождаемого гемоглобином кислорода в тканях регулируется продуктами катаболизма органических веществ: чем интенсивнее распад веществ, например при физических нагрузках, тем выше концентрация СО 2 и Н + и тем больше кислорода получают ткани в результате уменьшения сродства Нв к О 2 .
8. Аллостерическая регуляция сродства Нв к О 2 лигандом - 2,3-бис- фосфоглицератом. В эритроцитах из продукта окисления глюкозы - 1,3-бисфосфоглицерата синтезируется аллостерический лиганд гемоглобина - 2,3-бисфосфоглицерат (2,3-БФГ). В нормальных условиях концентрация 2,3-БФГ высокая и сравнима с концентрацией Нв. 2,3-БФГ имеет сильный отрицательный заряд -5.
 Бисфосфоглицерат
в капиллярах тканей, связываясь с дезоксигемоглобином, увеличивает
выход кислорода в ткани, уменьшая сродство Нв к О 2 .
Бисфосфоглицерат
в капиллярах тканей, связываясь с дезоксигемоглобином, увеличивает
выход кислорода в ткани, уменьшая сродство Нв к О 2 .
В центре тетрамерной молекулы гемоглобина находится полость. Ее образуют аминокислотные остатки всех четырех протомеров (см. рис. 1.22). В капиллярах тканей протонирование Нв (эффект Бора) приводит к разрыву связи между железом гема и О 2 . В молекуле
дезоксигемоглобина по сравнению с оксигемоглобином возникают дополнительные ионные связи, соединяющие протомеры, вследствие чего размеры центральной полости по сравнению с оксигемоглобином увеличиваются. Центральная полость является местом присоединения 2,3-БФГ к гемоглобину. Из-за различия в размерах центральной полости 2,3-БФГ может присоединяться только к дезоксигемоглобину.
2,3-БФГ взаимодействует с гемоглобином в участке, удаленном от активных центров белка и относится к аллостерическим (регуляторным) лигандам, а центральная полость Нв является аллостерическим центром. 2,3-БФГ имеет сильный отрицательный заряд и взаимодействует с пятью положительно заряженными группами двух β-цепей Нв: N-концевой α-аминогруппой Вал и радикалами Лиз 82 Гис 143 (рис. 1.26).
 Рис. 1.26. БФГ в центральной полости дезоксигемоглобина
Рис. 1.26. БФГ в центральной полости дезоксигемоглобина
БФГ связывается с тремя положительно заряженными группами в каждой β-цепи.
В капиллярах тканей образующийся дезоксигемоглобин взаимодействует с 2,3-БФГ и между положительно заряженными радикалами β-цепей и отрицательно заряженным лигандом образуются ионные связи, которые изменяют конформацию белка и снижают сродство Нв к О 2 . Уменьшение сродства Нв к О 2 способствует более эффективному выходу О 2 в ткани.
В легких при высоком парциальном давлении кислород взаимодействует с Нв, присоединяясь к железу гема; при этом изменяется конформация белка, уменьшается центральная полость и происходит вытеснение 2,3-БФГ из аллостерического центра
Таким образом, олигомерные белки обладают новыми по сравнению с мономерными белками свойствами. Присоединение лигандов на участках,
пространственно удаленных друг от друга (аллостерических), способно вызывать конформационные изменения во всей белковой молекуле. Благодаря взаимодействию с регуляторными лигандами происходит изменение конформации и адаптация функции белковой молекулы к изменениям окружающей среды.
ТЕМА 1.5. ПОДДЕРЖАНИЕ НАТИВНОЙ КОНФОРМАЦИИ БЕЛКОВ В УСЛОВИЯХ КЛЕТКИ
В клетках в процессе синтеза полипептидных цепей, их транспорта через мембраны в соответствующие отделы клетки, в процессе фолдинга (формирования нативной конформации) и при сборке олигомерных белков, а также в период их функционирования в структуре белков возникают промежуточные, склонные к агрегации, нестабильные конформации. Гидрофобные радикалы, в нативной конформации обычно спрятанные внутри белковой молекулы, в нестабильной конформации оказываются на поверхности и стремятся к объединению с такими же плохо растворимыми в воде группами других белков. В клетках всех известных организмов обнаружены специальные белки, которые обеспечивают оптимальный фолдинг белков клетки, стабилизируют их нативную конформацию при функционировании и, что особенно важно, поддерживают структуру и функции внутриклеточных белков при нарушении гомеостаза. Эти белки получили название «шапероны», что в переводе с французского обозначает «няня».
1. Молекулярные шапероны и их роль в предотвращении денатурации белков.
Шапероны (Ш) классифицируются по массе субъединиц. Высокомолекулярные шапероны имеют массу от 60 до 110 кД. Среди них наиболее изучены три класса: Ш-60, Ш-70 и Ш-90. Каждый класс включает семейство родственных белков. Так, в состав Ш-70 входят белки с молекулярной массой от 66 до 78 кД. Низкомолекулярные шапероны имеют молекулярную массу от 40 до 15 кД.
Среди шаперонов различают конститутивные белки, высокий базальный синтез которых не зависит от стрессовых воздействий на клетки организма, и индуцибельные, синтез которых в нормальных условиях идет слабо, но резко возрастает при стрессовых воздействиях. Индуцибельные шапероны называют также «белками теплового шока», так как впервые они были обнаружены в клетках, подвергавшихся воздействию высоких температур. В клетках из-за высокой концентрации белков самопроизвольная ренативация частично денатурированных белков затруднена. Ш-70 могут предотвращать начавшийся процесс денатурации и способствовать восстановлению нативной конформации белков. Молекулярные шапероны-70 - высококонсервативный класс белков, находящихся во всех отделах клетки: цитоплазме, ядре, эндоплазматическом ретикулуме, митохондриях. На карбоксильном конце единственной полипептидной цепи Ш-70 имеется участок, который представляет собой бороздку, способный взаимодействовать с пептидами длиной
от 7 до 9 аминокислотных остатков, обогащенных гидрофобными радикалами. Такие участки в глобулярных белках встречаются примерно через каждые 16 аминокислот. Ш-70 способны защищать белки от температурной инактивации и восстанавливать конформацию и активность частично денатурированных белков.
2. Роль шаперонов в фолдинге белков. При синтезе белков на рибосоме N-концевая область полипептида синтезируется раньше С-концевой. Для формирования нативной конформации необходима полная аминокислотная последовательность белка. В процессе синтеза белков шапероны-70, благодаря строению их активного центра, способны закрывать склонные к агрегации участки полипептида, обогащенные гидрофобными радикалами аминокислот до завершения синтеза (рис 1.27, А).
 Рис. 1.27. Участие шаперонов в фолдинге белков
Рис. 1.27. Участие шаперонов в фолдинге белков
А - участие шаперонов-70 в предотвращении гидрофобных взаимодействий между участками синтезирующегося полипептида; Б - формирование нативной конформации белка в шапероновом комплексе
Многие высокомолекулярные белки, имеющие сложную конформацию, например доменное строение, осуществляют фолдинг в специальном пространстве, сформированном Ш-60. Ш-60 функционируют в виде олигомерного комплекса, состоящего из 14 субъединиц. Они формируют два полых кольца, каждое из которых состоит из семи субъединиц, эти кольца соединены друг с другом. Каждая субъединица Ш-60 состоит из трех доменов: апикального (верхушечного), обогащенного гидрофобными радикалами, обращенными в полость кольца, промежуточного и экваториального (рис. 1.28).
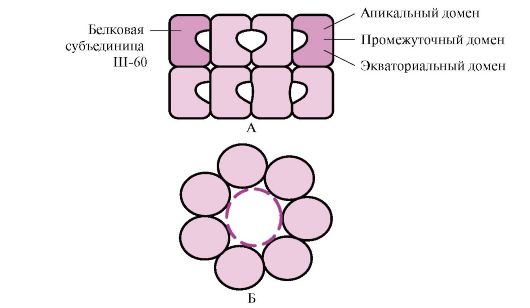 Рис. 1.28 . Структура шаперонинового комплекса, состоящего из 14 Ш-60
Рис. 1.28 . Структура шаперонинового комплекса, состоящего из 14 Ш-60
А - вид сбоку; Б - вид сверху
Синтезированные белки, имеющие на поверхности элементы, характерные для несвернутых молекул, в частности гидрофобные радикалы, попадают в полость шапероновых колец. В специфической среде этих полостей происходит перебор возможных конформаций, пока не будет найдена единственная, энергетически наиболее выгодная (рис. 1.27, Б). Формирование конформаций и высвобождение белка сопровождается гидролизом АТФ в экваториальной области. Обычно такой шаперонозависимый фолдинг требует затрат значительного количества энергии.
Кроме участия в формировании трехмерной структуры белков и ренативации частично денатурированных белков, шапероны также необходимы для протекания таких фундаментальных процессов, как сборка олигомерных белков, узнавание и транспорт в лизосомы денатурированных белков, транспорт белков через мембраны, участие в регуляции активности белковых комплексов.
ТЕМА 1.6. МНОГООБРАЗИЕ БЕЛКОВ. СЕМЕЙСТВА БЕЛКОВ НА ПРИМЕРЕ ИММУНОГЛОБУЛИНОВ
1. Белки играют решающую роль в жизнедеятельности отдельных клеток и всего многоклеточного организма, а их функции удивительно многообразны. Это определяется особенностями первичной структуры и конформаций белков, уникальностью строения активного центра и способностью связывать специфические лиганды.
Лишь очень небольшая часть всех возможных вариантов пептидных цепей может принять стабильную пространственную структуру; большинство
из них может принимать множество конформаций с примерно одинаковой энергией Гиббса, но с различными свойствами. Первичная структура большинства известных белков, отобранных биологической эволюцией, обеспечивает исключительную стабильность одной из конформаций, которая определяет особенности функционирования этого белка.
2. Семейства белков. В пределах одного биологического вида замены аминокислотных остатков могут приводить к возникновению разных белков, выполняющих родственные функции и имеющих гомологичные последовательности аминокислот. Такие родственные белки имеют поразительно сходные конформации: количество и взаиморасположение α-спиралей и (или) β-структур, большинство поворотов и изгибов полипептидных цепей похожи или идентичны. Белки с гомологичными участками полипептидной цепи, сходной конформацией и родственными функциями выделяют в семейства белков. Примеры семейств белков: сериновые протеиназы, семейство иммуноглобулинов, семейство миоглобина.
Сериновые протеиназы - семейство белков, выполняющих функцию протеолитических ферментов. К ним относятся пищеварительные ферменты - химотрипсин, трипсин, эластаза и многие факторы свертывания крови. Эти белки имеют в 40% положений идентичные аминокислоты и очень близкую конформацию (рис. 1.29).
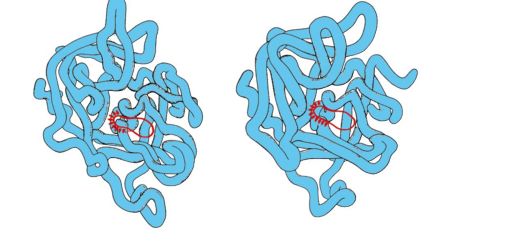
Рис. 1.29 . Пространственные структуры эластазы (А) и химотрипсина (Б)
Некоторые аминокислотные замены привели к изменению субстратной специфичности этих белков и возникновению функционального многообразия внутри семейства.
3. Семейство иммуноглобулинов. В работе иммунной системы огромную роль играют белки суперсемейства иммуноглобулинов, которое включает в себя три семейства белков:
Антитела (иммуноглобулины);
Рецепторы Т-лимфоцитов;
Белки главного комплекса гистосовместимости - МНС 1-го и 2-го классов (Major Histocompatibility Complex).
Все эти белки имеют доменное строение, состоят из гомологичных иммуноподобных доменов и выполняют сходные функции: взаимодействуют с чужеродными структурами, либо растворенными в крови, лимфе или межклеточной жидкости (антитела), либо находящимися на поверхности клеток (собственных или чужеродных).
4. Антитела - специфические белки, вырабатываемые В-лимфоцитами в ответ на попадание в организм чужеродной структуры, называемой антигеном.
Особенности строения антител
Простейшие молекулы антител состоят из четырех полипептидных цепей: двух идентичных легких - L, содержащих около 220 аминокислот, и двух идентичных тяжелых - Н, состоящих из 440-700 аминокислот. Все четыре цепи в молекуле антитела соединены множеством нековалентных связей и четырьмя дисульфидными связями (рис. 1.30).
Легкие цепи антитела состоят из двух доменов: вариабельного (VL), находящегося в N-концевой области полипептидной цепи, и константного (CL), расположенного на С-конце. Тяжелые цепи обычно имеют четыре домена: один вариабельный (VH), находящийся на N-конце, и три константных (CH1, CH2, СНЗ) (см. рис. 1.30). Каждый домен иммуноглобулина имеет β-складчатую суперструктуру, в которой два остатка цистеина соединены дисульфидной связью.
Между двумя константными доменами СН1 и СН2 имеется участок, содержащий большое число остатков пролина, которые препятствуют формированию вторичной структуры и взаимодействию соседних Н-цепей на этом отрезке. Эта шарнирная область придает молекуле антитела гибкость. Между вариабельными доменами тяжелых и легких цепей находятся два идентичных антигенсвязывающих участка (активные центры для связывания антигенов), поэтому такие антитела часто называют бивалентами. В связывании антигена с антителом участвует не вся аминокислотная последовательность вариабельных участков обеих цепей, а всего лишь 20-30 аминокислот, расположенных в гипервариабельных областях каждой цепи. Именно эти области определяют уникальную способность каждого вида антитела взаимодействовать с соответствующим комплементарным антигеном.
Антитела - одна из линий защиты организма против внедрившихся чужеродных организмов. Их функционирование можно разделить на два этапа: первый этап - узнавание и связывание антигена на поверхности чужеродных организмов, что возможно благодаря наличию в структуре антитела антигенсвязывающих участков; второй этап - инициация процесса инактивации и разрушения антигена. Специфичность второго этапа зависит от класса антител. Существует пять классов тяжелых цепей, отличающихся друг от друга по строению константных доменов: α, δ, ε, γ и μ, в соответствии с которыми различают пять классов иммуноглобулинов: A, D, Е, G и М.
Особенности строения тяжелых цепей придают шарнирным участкам и С-концевым областям тяжелых цепей характерную для каждого класса конформацию. После связывания антигена с антителом конформационные изменения константных доменов определяют путь удаления антигена.
 Рис. 1. 30. Доменное строение IgG
Рис. 1. 30. Доменное строение IgG
Иммуноглобулины М
Иммуноглобулины М имеют две формы.
Мономерная форма - 1-й класс антител, продуцируемый развивающимся В-лимфоцитом. Впоследствии многие В-клетки переключаются на выработку других классов антител, но с тем же антигенсвязывающим участком. IgM встраивается в мембрану и выполняет роль антигенраспознающего рецептора. Встраивание IgM в мембрану клеток возможно благодаря наличию в хвостовой части участка 25 гидрофобных аминокислотных остатков.
Секреторная форма IgM содержит пять мономерных субъединиц, связанных друг с другом дисульфидными связями и дополнительной полипептидной J-цепью (рис. 1.31). Тяжелые цепи мономеров этой формы не содержат гидрофобной хвостовой части. Пентамер имеет 10 центров связывания с антигеном и поэтому эффективен в распознавании и удалении впервые попавшего в организм антигена. Секреторная форма IgM - основной класс антител, секретируемых в кровь при первичном иммунном ответе. Связывание IgM с антигеном изменяет конформацию IgM и индуцирует связывание его с первым белковым компонентом системы комплемента (система комплемента - набор белков, участвующих в уничтожении антигена) и активацию этой системы. Если антиген расположен на поверхности микроорганизма, система комплемента вызывает нарушение целостности клеточной мембраны и гибель бактериальной клетки.
Иммуноглобулины G
В количественном отношении этот класс иммуноглобулинов преобладает в крови (75% от всех Ig). IgG - мономеры, основной класс антител, секретируемый в кровь при вторичном иммунном ответе. После взаимодействия IgG с поверхностными антигенами микроорганизмов комплекс антиген-антитело способен связывать и активировать белки системы комплемента или может взаимодействовать со специфическими рецепторами макрофагов и нейтрофилов. Взаимодействие с фагоцитами приводит
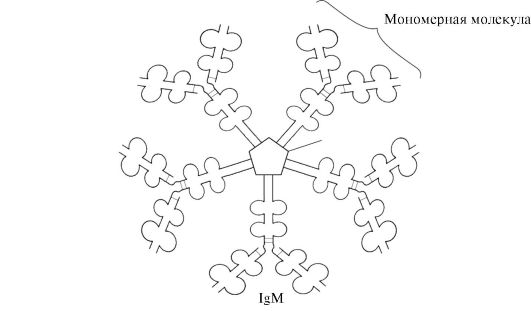 Рис. 1.31. Строение секреторной формы IgM
Рис. 1.31. Строение секреторной формы IgM
к поглощению комплексов антиген-антитело и разрушению их в фагосомах клеток. IgG - единственный класс антител, которые способны проникать через плацентарный барьер и обеспечивать внутриутробную защиту плода от инфекций.
Иммуноглобулины А
Основной класс антител, присутствующий в секретах (молоке, слюне, секретах дыхательных путей и кишечного тракта). IgA секретируются в основном в димерной форме, где мономеры связаны друг с другом через дополнительную J-цепь (рис. 1.32).
IgA не взаимодействуют с системой комплемента и фагоцитирующими клетками, но, связываясь с микроорганизмами, антитела препятствуют их присоединению к эпителиальным клеткам и проникновению в организм.
Иммуноглобулины Е
Иммуноглобулины Е представлены мономерами, в которых тяжелые ε-цепи содержат, так же как и μ-цепи иммуноглобулинов М, один вариабельный и четыре константных домена. IgE после секреции связываются своими
 Рис. 1.32. Строение IgA
Рис. 1.32. Строение IgA
С-концевыми участками с соответствующими рецепторами на поверхности тучных клеток и базофилов. В результате они становятся рецепторами для антигенов на поверхности данных клеток (рис. 1.33).
 Рис. 1.33. Взаимодействие IgE с антигеном на поверхности тучной клетки
Рис. 1.33. Взаимодействие IgE с антигеном на поверхности тучной клетки
После того как происходит присоединение антигена к соответствующим антигенсвязывающим участкам IgE, клетки получают сигнал к секреции биологически активных веществ (гистамина, серотонина), которые в большой мере ответственны за развитие воспалительной реакции и за проявление таких аллергических реакций, как астма, крапивница, сенная лихорадка.
Иммуноглобулины D
Иммуноглобулины D обнаружены в сыворотке в очень небольшом количестве, они являются мономерами. В тяжелых δ-цепях имеются один вариабельный и три константных домена. IgD выполняют роль рецепторов В-лимфоцитов, другие функции пока неизвестны. Взаимодействие специфических антигенов с рецепторами на поверхности В-лимфоцитов (IgD) приводит к передаче этих сигналов в клетку и включению механизмов, обеспечивающих размножение данного клона лимфоцитов.
ТЕМА 1.7. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛКОВ И МЕТОДЫ ИХ РАЗДЕЛЕНИЯ
1. Индивидуальные белки различаются по физико-химическим свойствам:
Форме молекул;
Молекулярной массе;
Суммарному заряду, величина которого зависит от соотношения анионных и катионных групп аминокислот;
Соотношению полярных и неполярных радикалов аминокислот на поверхности молекул;
Степени устойчивости к воздействию различных денатурирующих агентов.
2. Растворимость белков зависит от свойств белков, перечисленных выше, а также от состава среды, в которой растворяется белок (значения рН, солевого состава, температуры, наличия других органических веществ, способных взаимодействовать с белком). Величина заряда белковых молекул - один из факторов, влияющих на их растворимость. При потере заряда в изоэлектрической точке белки легче агрегируют и выпадают в осадок. Это особенно характерно для денатурированных белков, у которых на поверхности оказываются гидрофобные радикалы аминокислот.
На поверхности белковой молекулы имеются как положительно, так и отрицательно заряженные радикалы аминокислот. Количество этих групп, а следовательно, и суммарный заряд белков зависят от рН среды, т.е. соотношения концентрации Н+- и ОН - -групп. В кислой среде повышение концентрации Н+ приводит к подавлению диссоциации карбоксильных групп -СОО - + Н+ > - СООН и понижению отрицательного заряда белков. В щелочной среде связывание избытка ОН - протонами, образующимися при диссоциации аминогрупп -NH 3 + + ОН - - NH 2 + Н 2 О с образованием воды, приводит к уменьшению положительного заряда белков. Значение рН, при котором белок имеет суммарный нулевой заряд, называется изоэлектрической точкой (ИЭТ). В ИЭТ число положительно и отрицательно заряженных групп одинаково, т.е. белок находится в изоэлектрическом состоянии.
3. Разделение индивидуальных белков. Особенности строения и функционирования организма зависят от набора белков, синтезирующихся в нем. Изучение строения и свойств белков невозможно без их выделения из клетки и очистки от других белков и органических молекул. Стадии выделения и очистки индивидуальных белков:
Разрушение клеток изучаемой ткани и получение гомогената.
Разделение гомогената на фракции центрифугированием, получение ядерной, митохондриальной, цитозольной или иной фракции, содержащей искомый белок.
Избирательная тепловая денатурация - кратковременное нагревание раствора белков, при котором можно удалить часть денатурированных белковых примесей (в том случае, если белок относительно термостабилен).
Высаливание. Различные белки выпадают в осадок при разных концентрациях соли в растворе. Постепенно повышая концентрацию соли, можно получить ряд отдельных фракций с преимущественным содержанием выделяемого белка в одной из них. Наиболее часто для фракционирования белков используют сульфат аммония. Белки с наименьшей растворимостью выпадают в осадок при небольших концентрациях солей.
Гель-фильтрация - метод просеивания молекул через набухшие гранулы сефадекса (трехмерные полисахаридные цепи декстрана, имеющие поры). Скорость прохождения белков через колонку, заполненную сефадексом, будет зависеть от их молекулярной массы: чем меньше масса молекул белка, тем легче они проникают внутрь гранул и дольше там задерживаются, чем больше масса, тем быстрее они элюируют с колонки.
Ультрацентрифугирование - метод, заключающийся в том, что белки в центрифужной пробирке помещают в ротор ультрацентрифуги. При вращении ротора скорость оседания белков пропорциональна их молекулярной массе: фракции более тяжелых белков расположены ближе ко дну пробирки, более легкие - ближе к поверхности.
Электрофорез - метод, в основе которого лежат различия в скорости движения белков в электрическом поле. Эта величина пропорциональна заряду белков. Электрофорез белков проводят на бумаге (в этом случае скорость движения белков пропорциональна только их заряду) или в полиакриламидном геле с определенной величиной пор (скорость движения белков пропорциональна их заряду и молекулярной массе).
Ионообменная хроматография - метод фракционирования, основанный на связывании ионизированных групп белков с противоположно заряженными группами ионообменных смол (нерастворимых полимерных материалов). Прочность связывания белка со смолой пропорциональна заряду белка. Белки, адсорбированные на ионообменном полимере, можно смыть растворами NaCl с возрастающими концентрациями; чем меньше заряд белка, тем меньшая концентрация NaCl потребуется, чтобы смыть белок, связанный с ионогенными группами смолы.
Аффинная хроматография - наиболее специфический метод выделения индивидуальных белков.К инертному полимеру ковалентно присоединяется лиганд какого-либо белка. При пропускании раствора белков через колонку с полимером за счет комплементарного связывания белка с лигандом на колонке адсорбируется только специфичный для данного лиганда белок.
Диализ - метод, применяемый для удаления низкомолекулярных соединений из раствора выделяемого белка. Метод основан на неспособности белков проходить через полупроницаемую мембрану в отличие от низкомолекулярных веществ. Применяется для очистки белков от низкомолекулярных примесей, например от солей после высаливания.
ЗАДАНИЯ ДЛЯ ВНЕАУДИТОРНОЙ РАБОТЫ
1. Заполните табл. 1.4.
Таблица 1.4. Сравнительный анализ структуры и функций родственных белков - миоглобина и гемоглобина
а) вспомните строение активного центра Мв и НЬ. Какую роль играют гидрофобные радикалы аминокислот в формировании активных центров этих белков? Опишите строение активного центра Мв и НЬ и механизмы присоединения к нему лигандов. Какую роль играют остатки Гис F 8 и Гис Е 7 в функционировании активного центра Мв иНв?
б) какими новыми свойствами по сравнению с мономерным миоглобином обладает близко родственный олигомерный белок - гемоглобин? Объясните роль кооперативных изменений конформации протомеров в молекуле гемоглобина, влияние концентраций СО 2 и протонов на сродство гемоглобина к кислороду, а также роль 2,3-БФГ в аллостерической регуляции функции НЬ.
2. Дайте характеристику молекулярным шаперонам, обращая внимание на связь их структуры с функцией.
3. Какие белки объединяют в семейства? На примере семейства иммуноглобулинов определите сходные черты строения и родственные функции белков этого семейства.
4. Часто для биохимических и медицинских целей требуются очищенные индивидуальные белки. Объясните, на каких физико-химических свойствах белков основаны используемые методы их разделения и очистки.
ЗАДАНИЯ ДЛЯ САМОКОНТРОЛЯ
1. Выберите правильные ответы.
Функции гемоглобина:
A. Транспорт О 2 из легких в ткани Б. Транспорт Н + из тканей в легкие
B. Поддержание постоянства рН крови Г. Транспорт СО 2 из легких в ткани
Д. Транспорт СО 2 из тканей в легкие
2. Выберите правильные ответы. Лигандом α-протомера Нв является: A. Гем
Б. Кислород
B. СО Г. 2,3-БФГ
Д. β-Протомер
3. Выберите правильные ответы.
Гемоглобин в отличие от миоглобина:
A. Имеет четвертичную структуру
Б. Вторичная структура представлена только α-спиралями
B. Относится к сложным белкам
Г. Взаимодействует с аллостерическим лигандом Д. Ковалентно связан с гемом
4. Выберите правильные ответы.
Сродство Нв к О 2 уменьшается:
A. При присоединении одной молекулы О 2 Б. При отщеплении одной молекулы О 2
B. При взаимодействии с 2,3-БФГ
Г. При присоединении к протомерам Н + Д. При снижении концентрации 2,3-БФГ
5. Установите соответствие.
Для типов Нв характерно:
A. В дезокси форме образует фибриллярные агрегаты Б. Содержит в составе две α- и две δ-цепи
B. Преобладающая форма Нв в эритроцитах взрослого человека Г. В активном центре содержит гем с Fе+ 3
Д. Содержит в составе две α- и две γ-цепи 1. НвА 2.
6. Установите соответствие.
Лиганды Нв:
A. Связывается с Нв в аллостерическом центре
Б. Имеет очень высокое сродство к активному центру Нв
B. Присоединяясь, повышает сродство Нв к O 2 Г. Окисляет Fe+ 2 в Fе+ 3
Д. Образует ковалентную связь с гисF8
7. Выберите правильные ответы.
Шапероны:
A. Белки, присутствующие во всех отделах клетки
Б. Синтез усиливается при стрессовых воздействиях
B. Участвуют в гидролизе денатурированных белков
Г. Участвуют в поддержании нативной конформации белков
Д. Создают органеллы, в которых формируется конформация белков
8. Установите соответствие. Иммуноглобулины:
A. Секреторная форма имеет пентамерную форму
Б. Класс Ig, проникающих через плацентарный барьер
B. Ig - рецептор тучных клеток
Г. Основной класс Ig, присутствующих в секретах эпителиальных клеток. Д. Рецептор В-лимфоцитов, активация которого обеспечивает размножение клеток
9. Выберите правильные ответы.
Иммуноглобулины Е:
A. Вырабатываются макрофагами Б. Имеют тяжелые ε-цепи.
B. Встраиваются в мембрану Т-лимфоцитов
Г. Выполняют роль мембранных рецепторов антигенов на тучных клетках и базофилах
Д. Ответственны за проявление аллергических реакций
10. Выберите правильные ответы.
Метод разделения белков основан на различиях в их молекулярной массе:
A. Гель-фильтрация
Б. Ультрацентрифугирование
B. Электрофорез в полиакриламидном геле Г. Ионообменная хроматография
Д. Аффинная хроматография
11. Выберите правильный ответ.
Метод разделения белков основан на различиях в их растворимости в воде:
A. Гель-фильтрация Б. Высаливание
B. Ионообменная хроматография Г. Аффинная хроматография
Д. Электрофорез в полиакриламидном геле
ЭТАЛОНЫ ОТВЕТОВ К «ЗАДАНИЯМ ДЛЯ САМОКОНТРОЛЯ»
1. А, Б, В, Д
2. А, Б, В, Д
5. 1-В, 2-А, 3-Г
6. 1-В, 2-Б, 3-А
7. А, Б, Г, Д
8. 1-Г; 2-Б, 3-В
ОСНОВНЫЕ ТЕРМИНЫ И ПОНЯТИЯ
1. Олигомерные белки, протомер, четвертичная структура белков
2. Кооперативные изменения конформации протомеров
3. Эффект Бора
4. Аллостерическая регуляция функций белков, аллостерический центр и аллостерический эффектор
5. Молекулярные шапероны, белки теплового шока
6. Семейства белков (сериновые протеазы, иммуноглобулины)
7. IgM-, G-, Е-, А-связь структуры с функцией
8. Суммарный заряд белков, изоэлектрическая точка белков
9. Электрофорез
10. Высаливание
11. Гель-фильтрация
12. Ионообменная хроматография
13. Ультрацентрифугирование
14. Аффинная хроматография
15. Электрофорез белков плазмы крови
ЗАДАНИЯ ДЛЯ АУДИТОРНОЙ РАБОТЫ
1. Сравните зависимости степеней насыщения гемоглобина (Нв) и миоглобина (Mb) кислородом от его парциального давления в тканях
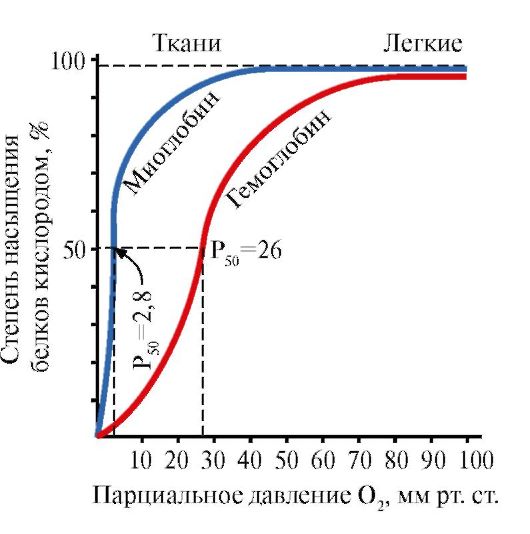 Рис. 1.34. Зависимость насыщения Мв и
НЬ
кислородом от его парциального давления
Рис. 1.34. Зависимость насыщения Мв и
НЬ
кислородом от его парциального давления
Обратите внимание, что форма кривых насыщения белков кислородом различна: для миоглобина - гипербола, для гемоглобина - сигмоидная форма.
1. сравните значения парциального давления кислорода, при котором Мв и Нв насыщены О 2 на 50%. Какой из этих белков характеризуется более высоким сродством к О 2 ?
2. какие особенности строения Мв определяют его высокое сродство к О 2 ?
3. какие особенности строения Нв позволяют ему отдавать О 2 в капиллярах покоящихся тканей (при относительно высоком парциальном давлении О 2) и резко увеличивать эту отдачу в работающих мышцах? Какое свойство олигомерных белков обеспечивает этот эффект?
4. вычислите, какое количество О 2 (в %) отдает оксигенированный гемоглобин покоящейся и работающей мышце?
5. сделайте выводы о связи структуры белка с его функцией.
2. Количество освобождаемого гемоглобином кислорода в капиллярах зависит от интенсивности процессов катаболизма в тканях (эффект Бора). Как изменения метаболизма в тканях регулируют сродство НЬ к O 2 ? Влияние СО 2 и Н+ на сродство НЬ к О 2
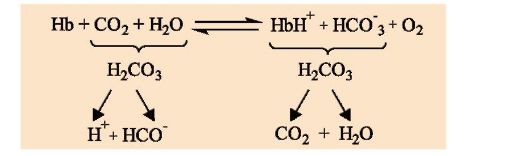 1. опишите эффект Бора.
1. опишите эффект Бора.
2. в каком направлении протекает процесс, представленный на схеме:
а) в капиллярах легких;
б) в капиллярах тканей?
3. в чем физиологическое значение эффекта Бора?
4. почему взаимодействие Нв с Н+ на участках, удаленных от гема, изменяет сродство белка к О 2 ?
3. Сродство НЬв к О 2 зависит от концентрации его лиганда - 2,3-бифосфо- глицерата, который является аллостерическим регулятором сродства Нв к О 2 . Почему взаимодействие лиганда в участке, удаленном от активного центра, влияет на функцию белка? Как 2,3-БФГ регулирует сродство НЬ к О 2 ? Для решения задачи ответьте на следующие вопросы:
1. где и из чего синтезируется 2.3-бифосфоглицерат (2,3-БФГ)? Напишите его формулу, укажите заряд данной молекулы.
2. с какой формой гемоглобина (окси или дезокси) взаимодействует БФГ и почему? В каком участке молекулы Нв происходит взаимодействие?
3. в каком направлении протекает процесс, представленный на схеме
а) в капиллярах тканей;
б) в капиллярах легких?
4. где должна быть более высокой концентрация комплекса
Нв-2,3-БФГ:
а) в капиллярах мышц, находящихся в состоянии покоя,
б) в капиллярах работающих мышц (при условии одинаковой концентрации БФГ в эритроцитах)?
5. как изменится сродство Нв к кислороду при адаптации человека к условиям высокогорья, если концентрация БФГ в эритроцитах при этом повышается? В чем физиологическое значение этого явления?
4. Разрушение 2,3-БФГ при хранении консервированной крови нарушает функции Нв. Как изменится сродство Нв к O 2 в консервированной крови, если концентрация 2,3-БФГ в эритроцитах может уменьшатся с 8 до 0,5 ммол/л. Можно ли переливать такую кровь тяжелобольным пациентам, если концентрация 2,3-БФГ восстанавливается не ранее чем через трое суток? Можно ли добавлением в кровь 2,3-БФГ восстановить функции эритроцитов?
5. Вспомните строение простейших молекул иммуноглобулинов. Какую роль играют иммуноглобулины в работе иммунной системы? Почему Ig часто называют бивалентами? Как структура Ig связана с их функцией? (Опишите на примере какого-либо класса иммуноглобулинов.)
Физико-химические свойства белков и методы их разделения.
6. Как суммарный заряд белка влияет на его растворимость?
а) определите суммарный заряд пептида при рН 7
Ала-Глу-Тре-Про-Асп-Лиз-Цис
б) как изменится заряд этого пептида при рН >7, рН <7, рН <<7?
в) что такое изоэлектрическая точка белка (ИЭТ) и в какой среде лежит
ИЭТ данного пептида?
г) при каком значении рН будет наблюдаться наименьшая растворимость данного пептида.
7. Почему кислое молоко в отличие от свежего при кипячении «сворачивается» (т.е. белок молока казеин выпадает в осадок)? В свежем молоке молекулы казеина имеют отрицательный заряд.
8. Для разделения индивидуальных белков используется метод гельфильтрации. Смесь, содержащую белки А, В, С с молекулярными массами, равными соответственно 160 000, 80 000 и 60 000, анализировали методом гель-фильтрации (рис. 1.35). Гранулы набухшего геля проницаемы для белков с молекулярной массой меньше 70 000. Какой принцип лежит в основе данного метода разделения? Какой из графиков правильно отражает результаты фракционирования? Укажите порядок выхода белков А, В и С с колонки.
 Рис. 1.35. Использование метода гель-фильтрации для разделения белков
Рис. 1.35. Использование метода гель-фильтрации для разделения белков
9. На рис. 1.36, А представлена схема электрофореза на бумаге белков сыворотки крови здорового человека. Относительные количества белковых фракций, полученных с помощью этого метода, составляют: альбумины 54-58%, α 1 -глобулины 6-7%, α 2 -глобулины 8-9%, β-глобулины 13%, γ-глобулины 11-12%.
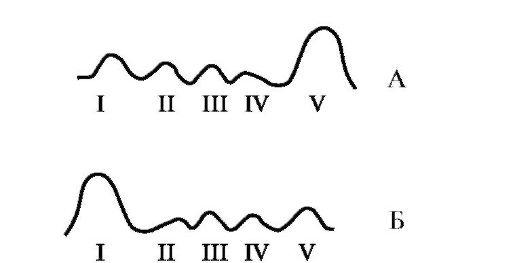 Рис. 1.36 Электрофорез на бумаге белков плазмы крови здорового человека (А) и больного (Б)
Рис. 1.36 Электрофорез на бумаге белков плазмы крови здорового человека (А) и больного (Б)
I - γ-глобулины; II - β-глобулины; III - α 2 -глобулин; IV - α 2 -глобулин; V - альбумины
Многие болезни сопровождаются количественными изменениями в составе сывороточных белков (диспротеинемии). Характер этих изменений учитывается при постановке диагноза и оценке тяжести и стадии заболевания.
С помощью данных, приведенных в табл. 1.5, сделайте предположение о заболевании, для которого характерен электрофоретический профиль, представленный на рис. 1.36.
Таблица 1.5. Изменение концентрации белков сыворотки крови при патологии
АК являются мономерными структурными единицами белковой молекулы из которых сложена полипептидная цепь. АК могут находиться в двух стерических формах: L- и D-. Эти формы зеркально симметричны. В них массивный боковой радикал R и Н-атом, стоящие при α-углероде меняются местами. Этих форм нет только у глицина, боковая цепь которого состоит из Н-атома. Боковые цепи сложены из остатков L- аминокислот, только они кодируются генами. D-остатки не кодируются при матричном синтезе белка, а синтезируются специальными ферментами. Рецемизация (переход L- в D-) при биосинтезе, а также спонтанно в белках практически не происходит, но часто встречается при химическом синтезе пептидов.
Белковая молекула характеризуется наличием прочных ковалентных и относительно слабых нековалентных связей . Такое сочетание ковалентных и нековалентных связей обеспечивает белковой молекуле определенную прочность и динамичность в процессе функционирования (рис.1).
а – электростатическое взаимодействие; б – водородные связи; в – взаимодействие неполярных боковых цепей, вызванное выталкиванием гидрофобных радикалов в «сухую» зону молекулами растворителя; г – дисульфидные связи (двойная изогнутая линия обозначает хребет полипептидной связи).
Рисунок 1 – Типы связей в белковой молекуле (по Филипповичу).
Ковалентные связи в молекуле белка могут быть двух типов – пептидные и дисульфидные. АК в белковой цепи связаны между собой пептидными связями С и N атомов. Пептидная, или кислотноамидная связь (-СО-NH- ), является типичной ковалентной связью. Пептидная связь возникает при взаимодействии карбоксильной группы одной АК и аминогруппы другой. Свободные амино- и карбоксильные группы образованного дипептида способны вновь вступать в реакцию поликонденсации с новыми молекулами АК, с образованием высокомолекулярного соединения. Таким образом, с помощью пептидной связи аминокислотные остатки соединяются друг с другом, образуя регулярный остов белковой молекулы, от которого отходят разнообразные боковые группы (R 1 …R М). Число звеньев боковой цепи (М) кодируется геном и составляет от нескольких десятков до многих тысяч. В процессе биосинтеза белка происходит соединение остатков отдельных аминокислот друг с другом в линейную последовательность:
NH-CH-CO-NH-CH-CO- …-NH-CH-CO-
Соединения, которые образуются в результате конденсации нескольких АК, получили название пептидов (ди-, три-, тетрапептиды и т. д.). В состав пептидов могут входить не только протеиногенные, но и непротеиногенные АК. Пептиды играют важную роль промежуточных продуктов в обмене веществ, и многие из них являются физиологически очень активными соединениями. Пептидами являются некоторые антибиотики (грамицидин, лихениформин), гормоны (инсулин, окситацин, вазопрессин), токсины (аманитины). Пептиды могут представлять собой замкнутую полипептидную цепочку, т. е. являться циклопептидами, а некоторые даже имеют бициклическое строение. Среди циклопептидов есть сильно токсичные вещества (ядовитый гриб бледная поганка (Amanita phalloides ).
Названия пептидов определяются наименованиями входящих в его состав АК, перечисляемых последовательно, начиная с N-конца, причем суффикс -ин- в названиях всех АК, за исключением С-концевой, имеющей свободную СООН-группу (карбоксильную), заменяется на суффикс -ил. Например, если в образовании три пептида принимают участие две молекулы аланина и одна молекула глицина, трипептид называют аланилаланилглицином или алаалагли. Сокращенно аминокислоты обозначают трехбуквенными символами (таблица 1).
Таблица 1 – Сокращенные обозначения аминокислот
Важную роль в стабилизации пространственной структуры белковой молекулы играют ковалентные дисульфидные связи(-S-S- ), которые образуются в результате окисления сульфгидрильных групп остатков цистеина. Дисульфидные связи могут образовываться между остатками цистеина двух полипептидных цепей или двумя остатками цистеина одной полипептидной цепи, стабилизируя при этом определенную конформацию белковой молекулы. В стабилизации конформации белковой молекулы существенную роль играют нековалентные связи и взаимодействия. К ним относятся гидрофобные, электростатические, ионные взаимодействия, а также водородные связи. Они поддерживают пространственное строение белка значительно слабее химических связей, фиксирующих последовательность мономеров (АК) в белковой цепи.
Гидрофобное взаимодействие возникает при сближении гидрофобных углеводородных и ароматических радикалов некоторых аминокислот (аланина, валина, лейцина, изолейцина, фенилаланина и триптофана). Процесс гидрофобного взаимодействия можно представить как перемещение неполярных групп полипептидной цепи (метильной -СН 3 , этильной -С 2 Н 5 , фенильной -С 6 Н 6) из воды в гидрофобные области, образуемые за счет ассоциации этих групп. Вследствие такого перемещения неполярные группы сказываются в непосредственной близости друг от друга во внутренней части молекулы, а гидрофильные группы размещаются на поверхности и контактируют с водой.
Водородные связи образуются между атомами водорода, ковалентно соединенными с атомом, содержащим неподеленную электронную пару, или другим электроотрицательным атомом. В биологических структурах водородная связь чаще всего образуется за счет атома водорода, связанного с кислородом или азотом. Водородные связи могут быть внутри- и межцепочечными. Внутрицепочечные водородные связи стабилизируют α-спиральные, а межцепочечные – β-складчатые структуры.
Ионные (солевые) связи. Они, предположительно, образуются между диссоциированными свободными карбоксильными группами (СОО -) моноаминодикарбоновых аминокислот (глутаминовой и аспарагиновой) и протонированными свободными аминогруппами (NH 3 +) диамино-монокарбоновых аминокислот. Ионные связи могут быть внутри- и межцепочечными.
Уровни структурной организации молекулы белка. Функциональные свойства белков определяются последовательностью АК и их пространственной структурой. С этой точки зрения выделяют четыре уровня : первичная, вторичная, третичная и четвертичная структуры.
Подпервичной структурой понимают качественный и количественный состав АК, а также их последовательность расположения в полипептидных цепях белковой молекулы. Молекула белка может иметь одну или несколько полипептидных цепей. Например, молекула фермента рибонуклеазы представляет одну полипептидную цепь, имеющую восемь остатков цистеина, образующих четыре внутримолекулярные дисульфидные связи. Гормон инсулин состоит из двух полипептидных цепей, связанных дисульфидными мостиками между остатками цистеина.
Вторичная структура показывает пространственную конфигурацию белковой молекулы. Выделяют три типа вторичной структуры: α-спиральная, β-складчатая и коллагеновая спираль.
В стабилизации вторичной структуры важную роль играют водородные связи , которые возникают между атомом водорода, соединенным с электроотрицательным атомом азота одной пептидной связи, и карбонильным атомом кислорода четвертой по счету от нее аминокислоты, и направлены они вдоль оси спирали. Энергетические расчеты показывают, что более эффективна правая α-спираль (рис. 2). Фибриллярные α-кератины (шерсть, кожа, перья) состоят из нескольких полипептидных цепей, имеющих правую α-спиральную конфигурацию, и образуют прочные суперспирали, выполняющие механические функции.
Рисунок 2 – α-спиральная конфигурация структуры белка
Другой тип вторичной структуры белка, получил название β-складчатой структуры или β-складчатого слоя. На рис. 3 показана модель такой структуры (а – вид сбоку, б – вид сверху). Точками на рисунке показаны межцепочечные водород-
Рисунок 3 – β-складчатая конфигурация структуры белка
ные связи. При таком пространственном расположении образуется система параллельно и антипараллельно размещенных фрагментов одной или нескольких полипептидных цепей. Полипептидные цепи в раскладках полностью вытянуты. Складки появляются из-за того, что плоскости двух соседних пептидных связей образуют некоторый угол. Система стабилизируется благодаря поперечным водородным связям между цепями, расположенными перпендикулярно по отношению к ориентации полипептидных связей. Расстояние между цепями составляет 0,95 нм, а период идентичности вдоль цепи – 0,70 нм для параллельных цепей и 0,65 нм для антипараллельных. Указанная структура характерна для фибриллярных белков (β-кератин, фиброин и др.). В частности, β-кератин характеризуется параллельным расположением полипептидных цепей, которые дополнительно стабилизируются межцепочечными S-S-связями. В фиброине шелка соседние полипептидные цепи антипараллельны.
Третий тип вторичной структуры - коллагеновая спираль . Она состоит из трех спирализованных цепей, имеющих форму стержня диаметром 1,5 нм и длиной около 300 нм. Спирализованные цепи закручиваются одна вокруг другой и образуют суперспираль. Расстояние между двумя АК остатками по оси спирали составляет 0,29 нм, а на один виток спирали приходится 3,3 остатка. Коллагеновая спираль стабилизируется водородными связями, возникающими между водородом пептидных NH-групп остатков АК одной цепи и кислородом СО-групп АК остатков другой цепи. Такая структура придает белку высокую упругость и прочность.
Третичная структура. Большинство белков в нативном состоянии имеют весьма компактную структуру, которая определяется размером, формой, полярностью АК радикалов, а также последовательностью АК (рис. 4). Образование нативной глобулярной структуры является многокомпонентным процессом, основанным на различных типах нековалентных взаимодействий. Превращение развернутой полипептидной цепи в компактную молекулу сопровождается гидрофобными взаимодействиями углеводородных радикалов таких АК, как лейцин, изолейцин, фенилаланин, триптофан, достаточно удаленных друг от друга в полипептидной цепи. Почти все неполярные или гидрофобные радикалы этих АК располагаются внутри глобулы и обеспечивают устойчивость ее структуры. Полярные или ионогенные радикалы (особенно аспарагиновой и глутаминовой кислот, аргинина и лизина) располагаются на внешней поверхности молекулы и находятся в гидратированном состоянии. В местах сгибов полипептидной цепи локализованы остатки таких АК, как пролин, изолейцин и серии, которые не способны образовывать α-спиральные структуры. Таким образом, между последовательностью АК в белке и его конформацией существует тесная взаимосвязь. Различия в аминокислотном составе и в последовательности отдельных АК остатков обусловливают возникновение в полипептидной цепи локальных неустойчивых точек, в которых стабильность α-спирали нарушена и под действием разнообразных молекулярных сил могут создаваться изгибы.
Рисунок 4 – Третичная структура белка
Существенное влияние на процесс формирования нативной конформации белка или его третичной структуры оказывают гидрофобные и ионогенные взаимодействия, водородные связи и др. Под действием этих сил достигается термодинамически целесообразная конформация белковой молекулы и ее стабилизация. После завершения процесса свертывания полипептидной цепи важную роль в стабилизации ее конформации играют ковалентные дисульфидные связи.
В настоящее время расшифрована третичная структура миоглобина, гемоглобина, РНК-азы, лизоцима, химотрипсина, карбоксипептидазы и других белков.
Под четвертичной структурой подразумевается характерный способ объединения и расположения в пространстве отдельных полипептидных цепей, составляющих одну функционально индивидуальную молекулу. По составу и сложности первичной, вторичной и третичной структуры субъединицы могут сильно отличаться. Например, молекула гемоглобина состоит из четырех субъединиц, которые объединены в мультимер с молекулярной массой 60000-70000, РНК-полимераза из Е. coli имеет пять субъединиц, а белок вируса табачной мозаики содержит несколько тысяч одинаковых субъединиц с молекулярной массой около 17500 каждая. В формировании четвертичной структуры принимают участие водородные связи, электростатические, Ван-дер-Ваальсовы и гидрофобные взаимодействия.
Для четвертичной структуры одних белков характерно глобулярное расположение субъединиц (гемоглобин), другие белки объединяются в спиральные четвертичные структуры по типу винтовой симметрии (вирус табачной мозаики). Четвертичная структура установлена для гемоглобина, вируса табачной мозаики, РНК-полимеразы, лактатдегидрогеназы, каталазы, аспартат-карбомоилазы и др.
Все процессы в клетке осуществляются при участии белков. Их функции чрезвычайно многообразны. Каждый данный белок как вещество с определенным химическим строением выполняет одну узкоспециализированную функцию и лишь в нескольких отдельных случаях – несколько взаимосвязанных.
Спускаясь от клеточного до молекулярного уровня мы встречаемся со следующими основными функциями белков:
1.Каталитическая (ферментативная) функция: Многочисленные биохимические реакции в живых организмах протекают в мягких условиях при температурах, близких к 40°С, и значениях рН близких к нейтральным. В этих условиях скорости протекания большинства реакций ничтожно малы, поэтому для их приемлемого осуществления необходимы специальные биологические катализаторы – ферменты. Даже такая простая реакция, как дегидратация угольной кислоты:
CO 2 + H 2 O HCO 3 - + H +
катализируется ферментом карбоангидразой. Вообще все реакции, за исключением реакции фотолиза воды 2H 2 O®4H + + 4e - + O 2 , в живых организмах катализируются ферментами. Как правило, ферменты – это либо белки, либо комплексы белков с каким-либо кофактором – ионом металла или специальной органической молекулой. Ферменты обладают высокой, иногда уникальной, избирательностью действия. Например, ферменты, катализирующие присоединение a-аминокислот к соответствующим т-РНК в процессе биосинтеза белка, катализируют присоединение только L-аминокислот и не катализируют присоединение D-аминокислот.
2. Транспортная функция белков. Белки служат для запасания и переноса кислорода (гемоглобин, гемоцианин). Эта функция напоминает ферментативную, но она отлична от нее, т.к. О 2 не претерпевает изменений.
Внутрь клетки должны поступать многочисленные вещества, обеспечивающие ее строительным материалом и энергией. В то же время все биологические мембраны построены по единому принципу – двойной слой липидов, в который погружены различные белки, причем гидрофильные участки макромолекул сосредоточены на поверхности мембран, а гидрофобные “хвосты” – в толще мембраны. Такая структура непроницаема для таких важных компонентов, как сахара, аминокислоты, ионы щелочных металлов. Их проникновение внутрь клетки осуществляется с помощью специальных транспортных белков, вмонтированных в мембрану клеток.
3. Регуляторные функции - низкомолекулярные полипептиды (инсулин, окситоцин), гормоны стимулируют функциональную активность в клетках других тканей и органов.
4. Защитная иммунологическая функция. Иммунная система обладает способностью отвечать на появление чужеродных частиц выработкой огромного числа лимфоцитов, способных специфически повреждать именно эти частицы, которыми могут быть чужеродные клетки, например патогенные бактерии, раковые клетки, надмолекулярные частицы, такие как вирусы, макромолекулы, включая чужеродные белки. Одна из групп лимфоцитов – В-лимфоциты , вырабатывает особые белки, выделяемые в кровеносную систему, которые узнают чужеродные частицы, образуя при этом высокоспецифичный комплекс на этой стадии уничтожения. Эти белки- иммуноглобулины высших организмов, защищают их от чужеродных биополимеров за счет своего специфического строения (функциональной группы).
5. Функция хранения, передачи химических и электрических сигналов.
6. Структурная функция. Наряду с белками, выполняющими тонкие высокоспециализированные функции, существуют белки, имеющие в основном структурное значение. Они обеспечивают механическую прочность и другие механические свойства отдельных тканей живых организмов. В первую очередь это коллаген - основной белковый компонент внеклеточного матрикса соединительной ткани. У млекопитающих коллаген составляет до 25% общей массы белков. В эластичных тканях - коже, стенках кровеносных сосудов, легких - помимо коллагена внеклеточный матрикс содержит белок эластин , способный довольно в широких пределах растягиваться и возвращаться в исходное состояние.
Еще один пример структурного белка - фиброин шелка, выделяемый гусеницами шелкопряда в период формирования куколки и являющийся основным компонентом шелковых нитей.
7. Двигательные белки. Мышечное сокращение является процессом, в ходе которого происходит превращение химической энергии, запасенной в виде макроэргических пирофосфатных связей в молекулах АТФ, в механическую работу. Непосредственными участниками процесса сокращения являются два белка - актин и миозин.
8. Рецепторная функция. Большое значение, в особенности для функционирования многоклеточных организмов, имеют белки-рецепторы , вмонтированные в плазматическую мембрану клеток и служащие для восприятия и преобразования различных сигналов, поступающих в клетку, как от окружающей среды, так и от других клеток. В качестве наиболее исследованных можно привести рецепторы ацетилхолина , находящиеся на мембране клеток в ряде межнейронных контактов, в том числе в коре головного мозга, и у нервно-мышечных соединений. Эти белки специфично взаимодействуют с ацетилхолином и отвечает на это передачей сигнала внутрь клетки. После получения и преобразования сигнала нейромедиатор должен быть удален, чтобы клетка подготовилась к восприятию следующего сигнала.
9. Токсины: Ряд живых организмов в качестве защиты от потенциальных врагов вырабатывают сильно ядовитые вещества - токсины. Многие из них являются белками, однако, встречаются среди них и сложные низкомолекулярные органические молекулы. В качестве примера такого вещества можно привести ядовитое начало бледной поганки - a-аманитин: Это соединение специфично блокирует синтез эукариотических и-РНК. Для человека смертельной дозой является несколько мг этого токсина.
Первичная и вторичная структура белков. Белки не являются статическими образованиями. Это структуры, которые могут претерпевать определенные конформационные изменения в процессе биологического функционирования. Анализ конформаций проводят исходя из различных уровней организации белковых молекул. Еще в 1959 г К.Линдерстрем-Ланг выделил четыре уровня структурной организации белков - первичную, вторичную, третичную и четвертичную структуру. Позже на основании сопоставления данных рентгеноструктурного анализа, калориметрии и других методов были выделены еще два уровня организации - сверхвторичные структуры и домены белков.
Аминокислотную последовательность называют первичной структурой белка. Изучение расположения аминокислот в белках представляет важный этап в изучении структуры белка. В настоящее время этот анализ проводится автоматически с помощью приборов секвинаторов. В последние годы используется новый метод определения аминокислотной последовательности. Выделяют фрагмент ДНК, содержащий структурный ген данного белка, расшифровывают последовательность нуклеотидов и переводят ее согласно генетическому коду в аминокислотную последовательность. Первичная структура - это одномерное представление белковой молекулы. Знание первичной структуры используется для предсказания вторичной и третичной структуры белка. Одновременное использование аминокислотной последовательности и кристаллографических карт электронной плотности позволяет восстановить пространственное расположение всех атомных групп в белке.
В полипептидной цепи пептидная группа является плоской и жесткой. Полипептидную цепь можно представить как последовательность однотипных плоскостей (пептидных групп), соединенных между собой одинарными связями. Вращение вокруг этих связей не является полностью свободным вследствие стерических ограничений. Угол поворота вокруг связей С – С а обозначают ψ, а угол поворота вокруг связей N – С а обозначают φ. Г.Рамачандран провел расчеты конформационных состояний полипептидной цепи с помощью ЭВМ и определил область возможных значений ψ и (графики Рамачандрана или конформационные карты). На конформационных картах значения углов ψ и φ в белках не являются произвольными, они четко ограничены конкретными областями, что свидетельствует о существовании ограниченного количества конформаций полипептидной цепи.
Под вторичной структурой белка понимают упорядоченное расположение полипептидной цепи, стабилизированное водородными связями между пептидными группами. Рассматривая этот структурный уровень, говорят о локальной конформации участков полипептидной цепи. Часто встречаемой и наиболее энергетически и стерически выгодной вторичной структурой является правая α– спираль, которая впервые была постулирована Л.Полингом и Р.Кори (1951) . Наиболее важные характеристики α– спирали: 1) число аминокислотных остатков на один шаг спирали составляет 3,6; 2) шаг спирали d = 0,54 нм; 3) трансляция на один остаток вдоль спирали Δd = 0,15 нм; 4) радиус α– спирали r = 0,23 нм; 5) водородные связи (параллельные оси спирали) образуются между каждой первой и четвертой пептидной группой; 6) для α– спирали φ = -57° и ψ = -47°. Как видно из поперечного среза α– спирали на каждом обороте ее происходит сдвиг вправо на 60°. В результате такого сдвига только через 10 оборотов 1-я пептидная группа точно будет совпадать с 36-й пептидной группой.
Вторичными структурами белковых молекул являются параллельные и антипараллельные β-складчатые листы (или β-структура). На конформационной карте Рамачандрана для β-слоя с антипараллельными цепями φ = -139° и ψ = +135° , для β-слоя с параллельными цепями φ = - 119° и ψ = +113°. Большинство из них имеют не более шести полипептидных цепей, стабилизированных водородными связями, и по шесть аминокислотных остатков по длине каждой цепи. Размеры такого листа: ширина t = 2,5 нм, длина l = 2,0 нм. Большинство складчатых листов имеют скрученную форму. Скручивание идет перпендикулярно вытянутым цепям.
Следующим уровнем организации белковых молекул являются сверхвторичные структуры. Примером таких структур является суперспиральные структуры. В них две α– спирали (в тропомиозине, легком меромиозине, парамиозине) или три α -спирали (в фибриногене) скручены друг относительно друга. Шаг суперспирали в легком меромиозине составляет α= 18,6 нм. На примере тропомиозина с известной аминокислотной последовательностью сделан вывод о том, что суперспираль стабилизируется гидрофобными взаимодействиями между отдельными α -спиралями.
Первичная структура цепи и формирование белковой глобулы
Одной из важнейших проблем физики белка является проблема связи между первичной структурой полипептидной цепи и пространственной строением глобулы. Биологически функциональна нативная пространственная структурa макромолекул, а генетически кодируется первичная структура. И почему молекула белка образует глобулу, по другому говоря, почему белок способен к самосборке и белок в этом состоянии уже может выполнять свои функции? Как было установлено Гуццо, для пространственной структуры белка имеет значение конкретное расположение аминокислот. Различают аминокислоты «неспиральные» не могут образовывать спирали и «спиральные» - могут изгибаться (асп, цис, тир, сер). От этого зависит закрученность, укладка молекулы. И еще особо важное значение для образования пространственной структуры белка имеет аминокислота глицин - это как универсальный шарнир может занимать самые различные положения.
В настоящее время предполагается, что самоорганизация белковой глобулы, не есть результат некого направленного процесса. Многие исследователи считают, что программа безошибочной самоорганизации закодирована в самой первичной структуре. Самоорганизация происходит стадийно, так что на каждом следующей стадии формируется все более сложная и стабилизированная структура.
Регулярные конформации полипептидных цепей, стабилизированные водородными связями (α и β – формы) устойчивы лишь в определенных условиях, Изменение температуры, рН, растворителя среды приводит к переходам конформации. Американец Доти установил, что переходы спираль-клубок протекают за очень короткое время. Переход характеризуется изменением вязкости, светорассеивания и т.д. Резкость перехода свидетельствует о кооперативном характере, т.е. каждое звено макромолекулы находится в закрепленном состоянии с помощью водородных связей. При действии посторонних факторов происходит изменение упаковки молекул, т.е. конформации.
Согласно ученому Птицину на первой стадии в развернутой белковой цепи образуются флуктурующие (измененные, непостоянные) зародыши спиральных участков с вытянутой структурой (места образ.). На второй стадии одна или несколько пар зародышей объединяются, образуя центры организации третичной структуры. На третьей стадии происходит рост центров за счет присоединения соседних участков цепи.
И на последней, четвертой стадии образуется единая компактная структура глобулы путем роста или объединения нескольких центров.
Домены и третичная структура белка
Третичная структура белка представляет собой термодинамически наиболее стабильную форму свертывания и укладки полипептидной цепи. Возникает вопрос, как происходит свертывание белка, каким образом одномерная информация, заложенная в последовательности аминокислот, реализуется в пространственную информацию? Эксперименты по денатурации и ренатурации белков показали, что процессы разрушения и образования компактной третичной структуры проходят достаточно быстро: нуклеаза стафилококков повторно свертывается за 1 с.
Для объяснения процесса свертывания используется нуклеационная модель. В этой модели допускается, что короткие сегменты полипептидной цепи очень быстро свертываются независимо друг от друга, а на втором этапе они сближаются, образуя компактную трехмерную структуру. Сегменты белка образуют α -спирали и β-слои с большой скоростью. Экспериментально показано, что переходы спираль - клубок проходят за время от 10 -6 до 10 -8 c.
В последнее время в белках выделен еще один важный уровень структурной организации. Анализ карт электронной плотности белков с молекулярной массой больше 20 000 показал, чтo белки состоят из нескольких глобулярных областей, слабо связанных между собой. Эти области получили название доменов. Индивидуальные домены часто можно выделить из белка с помощью протеолитических ферментов без потери ими функциональных свойств. Под доменом подразумевают область одной полипептидной цепи, заключенной в компактном объеме. Это такие участки цепи, которые свертываются и развертываются в белке независимо друг от друга.
Домен можно рассматривать как относительно автономную структурную единицу. С помощью сканирующей микрокалориметрии Привалов показал наличие в сложных белках отдельных кооперативных блоков, для которых характерны скачкообразные структурные переходы при тепловой денатурации. Оказалось, что во многих случаях такие кооперативные белки хорошо соответствует выделенным протеолитическим фрагментам белков. Это позволило идентифицировать кооперативные блоки с доменами белков. Часто выделенные протеолитические фрагменты имеет структурные свойства, подобные кооперативным блокам, т.е. совпадают их температуры плавления и энтальпии переходов, а также они сохраняют функциональные характеристики нативных белков. Домены связаны между собой очень ограниченным количеством пептидных связей, которые сравнительно легко разрываются под действием протеолитических ферментов.
В настоящее время с помощью сканирующей микрокалориметрии электронной микроскопии, протеолитического расщепления установлено доменное строение в таких высокомолекулярных белках, как иммуноглобулин, миозин, фибриноген и др.
Домены могут представлять собой важные промежуточные образования в процессе свертывания нативной структуры белков. Белки, состоящие из доменов, должны иметь более гибкую структуру, чем белки, в которых различные участки скреплены между собой. По-видимому, обратимые конформационные изменения, влияющие на функцию ферментов, связаны с междоменными перестройками без изменения структурной стабильности самих доменов.
Гипотеза расплавленной глобулы. Одним из способов изучения сворачивания полипептидной цепи в трехмерную структуру является денатурация и последующая ренатурация белковой молекулы.
Опыты К. Анфинсена с рибонуклеазой однозначно показывают возможность сборки именно той пространственной структуры, которая была нарушена в результате денатурации.
В данном случае восстановление нативной конформации не требует наличия никаких дополнительных структур. Какие же модели свертывания полипептидной цепи о соответствующую конформацию являются наиболее вероятными? Одной из распространенных гипотез самоорганизации белка является гипотеза расплавленной глобулы. В рамках этой концепции выделяют несколько этапов самосборки белков.
1. В развернутой полипептидной цепи с помощью водородных связей и гидрофобных взаимодействий образуются отдельные участки вторичной структуры, служащие как бы затравками для формирования полных вторичных и супервторичных структур.
2. Когда число этих участков достигает определенной пороговой величины, происходит переориентация боковых радикалов и переход полипептидной цепи в новую более компактную форму, причем число нековалентных связей значительно увеличивается. Характерной особенностью этой стадии является образование специфических контактов между атомами, находящимися на удаленных участках полипептидной цепи, но оказавшихся сближенными в результате образования третичной структуры.
3. На последнем этапе формируется нативная конформация белковой молекулы, связанная с замыканием дисульфидных связей и окончательной стабилизацией белковой конформации. Не исключена также неспецифическая агрегация частично свернутых полипептидных цепей, что можно квалифицировать как ошибки образования нативных белкоя. Частично свернутая полипептидная цепь (этап 2) называется расплавленной глобулой, а этап 3 является самым медленным при образовании зрелого белка.
В клетках имеется ряд каталитически неактивных белков, которые, тем не менее, вносят большой вклад в образование пространственных структур белков. Это так называемые шапироны и шапиронины. Один из первооткрывателей молекулярных шапиронов Л. Эллис называет их функциональным классом не связанных друг с другом семейств белков, которые помогают правильной нековалентной сборке других полипептидсодержащих структур in vivo, но не входят в состав собираемых структур и не участвуют к реализации их нормальных физиологических функций.
Шапироны помогают правильной сборке трехмерной белковой конформации путем образования обратимых нековалентных комплексов с частично свернутой полипептидной цепью, одновременно ингибируя неправильно образованные связи, ведущие к формированию функционально неактивных белковых структур. В перечень функций, свойственных шапиронам, входит зашита расплавленных глобул от агрегации, а также перенос новосинтезированных белков в различные локусы клеток. Шапироны преимущественно являются белками теплового шока, синтез которых резко усиливается при стрессовом температурном воздействии. Семейства этих белков найдены в микробных, растительных и животных клетках. Классификация шапиронов основана на их молекулярной массе, которая варьирует от 10 до 90 kDa. В основном функции шапиронов и шапиронинов различаются, хотя и те, и другие являются белками-помощниками процессов образования трехмерной структуры белков. Шапироны удерживают новосинтезированную полипептидную цепь в развернутом состоянии, не давая ей свернуться в отличную от нативной форму, а шапиронины обеспечивают условия для образования единственно правильной, нативной структуры белка.
Четвертичная структура белков
Образование хаотично сформированных агрегатов является ошибкой, которая приводит к появлению функционально неактивных белков, поэтому в клетках предусмотрены механизмы быстрой их деградации и распада на отдельные аминокислоты. Однако в природе существует немало генетически детерминированных агрегатов, включающих в себя несколько полипептидных цепей, образующих большие белковые макромолекулы. Четвертичной структурой называют ассоциированные между собой две или более субъединиц, ориентированных в пространстве. По-видимому, более правильно применительно к четвертичной структуре белков говорить не об агрегатах, а об ансамблях глобул. Характеризуя четвертичную структуру белков, следует исключать ее псевдоварианты. Так белковый гормон инсулин состоит из двух полипептидных цепей, но они не являются полноправными глобулами, а образуются в результате ограниченного протеолиза единой полипептидной цепи. Не являются белками с истинной четвертичной структурой и мультиферментные комплексы. Они представляют собой типичные надмолекулярные структуры. При образовании четвертичной структуры отдельные субъединицы взаимодействуют друг с другом исключительно при помощи нековалентных связей, в первую очередь водородных и гидрофобных. Весьма существенным является тот факт, что контактные поверхности взаимодействующих субъединиц комплементарны друг другу. В контактных участках расположены гидрофобные группировки, которые получили название «липкие пятна».
Взаимная ориентация электроотрицательных атомов, облегченная наличием комплементарных сайтов, способствует образованию большого числа водородных связей. Это обеспечивает реализацию кооперативного эффекта и стабилизацию макромолекулы. Кроме того, множественность нековалентных связей является основой передачи структурных перестроек от одной субъединицы на другие.
Белки, имеющие четвертичную структуру, часто называют олигомерными. Различают гомомерные и гетеромерные белки. К гомомерным относятся белки, у которых все субъединицы имеют одинаковое строение. В качестве примера можно привести белок каталазу, состоящую из четырех абсолютно равноценных субъединиц. У гетеромерных белков отдельные субъединицы не только отличаются по строению, но и могут выполнять различные функции. Например, белок РНК-полимераза состоит из пяти субъединиц различного строения и с неодинаковыми функциями.
Белки представляют собой полипептиды, молекулярная масса которых превышает 6000-10000 дальтон. Они состоят из большого числа аминокислотных остатков.
В отличие от низкомолекулярных пептидов, белки обладают хорошо развитой трехмерной пространственной структурой, которая стабилизируется различного рода сильными и слабыми взаимодействиями. Различают четыре уровня структурной организации белковой молекулы: первичную, вторичную, третичную и четвертичную структуры.
Первичная структура белка представляет собой последовательность аминокислотных остатков, соединенных между собой пептидными связями.
Впервые предположение о роли пептидных связей в построении белковых молекул было выдвинуто русским биохимиком А. Я. Данилевским, идеи которого легли в основу полипептидной теории строения белков, сформулированной немецким химиком Э. Фишером в 1902 г.
Основу первичной структуры белковой молекулы образует регулярно повторяющийся пептидный остов — NH-CH-CO-, а боковые радикалы аминокислот составляют ее вариабельную часть.
Первичная структура белка прочная, т. к. в основе ее построения лежат ковалентные по характеру пептидные связи, представляющие собой сильные взаимодействия;
Соединяясь между собой в различной последовательности, протеиногенные аминокислоты образуют изомеры. Из трех аминокислот можно построить шесть различных трипептидов. Например, из глицина, аланина и валина - гли-ала-вал, гли-вал-ала, ала-гли-вал, ала-вал-гли, вал-гли-ала и вал-ала-гли. Из четырех аминокислот можно образовать 24 тетрапептида, а из пяти - 120 пентапептидов. Из 20 аминокислот можно построить 2 432 902 008 176 640 000 полипептидов. При этом каждая аминокислота используется в построении рассмотренных полипептидных цепочек только один раз.
Многие природные полипептиды насчитывают в своем составе сотни и даже тысячи аминокислотных остатков, и каждая из 20 протеиногенных аминокислот может встречаться в их составе неоднократно. Поэтому число возможных вариантов полипептидных цепочек бесконечно велико. Однако в природе реализуются далеко не все теоретически возможные варианты аминокислотных последовательностей.
Первым белком, первичная структура которого была расшифрована, является бычий инсулин. Его молекула состоит из двух полипептидных цепочек, одна из которых содержит 21, а другая - 30 аминокислотных остатков. Цепочки соединяются между собой двумя дисульфидными связями. Еще одна дисульфидная связь располагается внутри короткой цепи. Последовательность расположения аминокислотных остатков в молекуле инсулина установил английский биохимик Ф. Сэнгер в 1953 г.
Таким образом, Ф. Сэнгер подтвердил полипептидную теорию строения белковой молекулы Э. Фишера и доказал, что белки - это химические соединения, обладающие определенной структурой, которую можно изобразить с помощью химической формулы. К настоящему времени расшифрованы первичные структуры нескольких тысяч белков.
Химическая природа каждого белка уникальна и тесно связана с его биологической функцией. Способность белка выполнять присущую ему функцию определяется его первичной структурой. Даже небольшие изменения в последовательности аминокислот в белке могут привести к серьезному нарушению в его функционировании, возникновению тяжелого заболевания.
Болезни, связанные с нарушениями первичной структуры белка, получили название молекулярных. К настоящему времени открыто несколько тысяч таких болезней.
Одной из молекулярных болезней является серповидноклеточная анемия, причина которой кроется в нарушении первичной структуры гемоглобина. У людей с врожденной аномалией структуры гемоглобина в полипептидной цепочке, состоящей из 146 аминокислотных остатков, в шестом положении находится валин, тогда как у здоровых людей на этом месте - глутаминовая кислота. Аномальный гемоглобин хуже транспортирует кислород, а эритроциты крови больных имеют серповидную форму. Заболевание проявляется в замедлении развития, общей слабости организма.
Первичная структура белка задана генетически. Это дает возможность организмам одного вида поддерживать постоянство набора белков. Однако у разных видов живых организмов белки, выполняющие одинаковую функцию, не идентичны по первичной структуре - на отдельных участках полипептидной цепи они могут иметь неодинаковые последовательности аминокислот. Такие белки называются гомологичными (греч. «гомология» - согласие).
Исследования кон формации белковых молекул показали, что полипептидные цепи не вытягиваются строго линейно, а определенным образом сворачиваются в пространстве, образуя вторичную структуру.
Вторичная структура белка представляет собой сочетание упорядоченных и аморфных участков полипептидной цепи.
Изучая кристаллические структуры соединений, содержащих амидные группы, американский биохимик Л. Полинг установил, что длина пептидной связи близка к длине двойной связи и составляет 0,1325 нм. Поэтому свободное вращение атомов углерода и азота вокруг пептидной связи затруднено.
Кроме того, атомы пептидных групп и α-углеродные атомы располагаются в полипептидной цепи приблизительно в одной плоскости. В связи с этим повороты в полипептидной цепи могут совершаться только по связям, примыкающим к углеродным атомам.
За счет поворотов пептидных групп вокруг α-углеродных атомов, как установили Л. Полинг и Р. Кори в начале 50-х годов прошлого века, полипептидная цепочка сворачивается в α-спираль и стабилизируется за счет образования максимально возможного числа водородных связей.
При образовании вторичной структуры белковой молекулы водородные связи возникают между атомами пептидных групп, расположенными на соседних витках ос-спирали друг против друга. Атом водорода, соединенный ковалентной связью с атомом азота, имеет некоторый положительный заряд. Атом кислорода, соединенный двойной связью с атомом углерода, имеет некоторый отрицательный заряд. Водородный атом, оказавшись напротив атома кислорода, связывается с ним водородной связью. Водородная связь слабая. Однако за счет образования большого числа этих связей обеспечивается сохранение строго упорядоченной структуры.
Водородные связи всегда направлены параллельно воображаемой оси а-спирали, а радикалы аминокислот - наружу от ее витков. Пептидные группы соединяются между собой водородными связями преимущественно через четыре аминокислотных остатка, так как именно их О-С- и H-N-группы оказываются пространственно сближенными.
А-Спираль является правозакрученной. Если смотреть на нее с торца, со стороны N-конца, то закручивание полипептидной цепочки происходит по часовой стрелке. Установлены параметры а-спирали. Расстояние между соседними витками (шаг спирали) составляет ∅54 нм, а внутренний диаметр спирали - 1,01 нм. Один полный виток спирали включает в себя 3,6 аминокислотных остатка. Полное повторение структуры α-спирали происходит каждые 5 витков, включающих в себя 18 аминокислотных остатков. Этот отрезок α-спирали называется периодом идентичности и составляет в длину 2,7 нм.
Полипептидные цепочки сворачиваются в а-спираль не на всем своем протяжении. Процентное содержание заспирализованных участков в белковой молекуле называется степенью спирализации . Белки существенно различаются по степени спирализации, например: для гемоглобина крови она очень высокая - 75%, для инсулина также довольно высокая - 60%, для альбумина куриного яйца значительно ниже - 45%, а для химотрипсиногена (неактивного предшественника фермента пищеварения) крайне низкая - всего 11%.
Различия в степени спирализации белков связаны с рядом факторов, мешающих регулярному образованию водородных связей между пептидными группами. К нарушению спирализации приводит, в частности, образование остатками цистеина дисульфидных связей, соединяющих различные участки одной или нескольких полипептидных цепей. В области, близкой к остатку иминокислоты пролина, вокруг α-углеродного атома которого невозможно вращение соседних атомов, в полипептидной цепи образуется изгиб.
Ряд протеиногенных аминокислот обладают такими радикалами, которые не позволяют им принимать участие в формировании α-спирали. Эти аминокислоты образуют параллельно расположенные складки, соединенные друг с другом водородными связями. Такой тип регулярного участка полипептидной цепи получил название структуры складчатого слоя, или β-структуры.
В отличие от а-спирали, имеющей стержневую форму, β-структура имеет форму складчатого листа. Она стабилизируется водородными связями, возникающими между пептидными группами, расположенными на соседних отрезках полипептидной цепи. Эти отрезки могут быть направлены либо в одну сторону - тогда образуется параллельная β-структура, либо в противоположные - в этом случае возникает антипараллельная β-структура.
Пептидные группы в β-структуре располагаются в плоскостях складок, а боковые радикалы аминокислот - над и под плоскостями. Расстояние между соседними участками полипептидной цепи в структуре складчатого слоя составляет 0,272 нм, что соответствует длине водородной связи между группами -СО- и -NH-. Сами водородные связи располагаются перпендикулярно направлению структуры складчатого слоя. Содержание β-структуры в различных белках колеблется в широких пределах.
Некоторые участки полипептидных цепочек не имеют какой-либо упорядоченной структуры и представляют собой беспорядочные клубки. Такие участки называются аморфными (греч. «аморфос» - бесформенный). Однако в каждом белке аморфные участки имеют свою фиксированную конформацию. При этом в отличие от относительно жестких участков - α-спирали и β-структуры - аморфные клубки могут сравнительно легко изменять свою конформацию.
Белки различаются по содержанию разных типов вторичной структуры. Например, в структуре гемоглобина обнаружены только α-спирали. во многих ферментах присутствуют различные сочетания как α-спиралей так и β-структур, среди иммуноглобулинов встречаются белки, имеющие только β-структуру. Наконец, встречаются и такие белки, у которых упорядоченные участки присутствуют в незначительном количестве, а большая часть полипептидной цепочки имеет аморфную структуру.
Полипептидные цепочки со сформированной вторичной структурой определенным образом располагаются в пространстве, создавая еще один уровень структурной организации белковой молекулы - третичную структуру.
Третичная структура белка образуется в результате специфической укладки упорядоченных и аморфных участков полипептидной цепи в некотором объеме пространства. Она поддерживается за счет сильных и слабых взаимодействий, возникающих между боковыми радикалами остатков аминокислот. К сильным взаимодействиям относится дисульфидная связь, а к слабым - водородная и ионная связи, а также гидрофобные взаимодействия.
Дисульфидная связь образуется при взаимодействии двух близко расположенных радикалов остатков цистеина, содержащих свободные сульфгидрильные группы.
Дисульфидные мостики могут соединять между собой не только отдельные участки внутри одной полипептидной цепи, но и (при образовании четвертичной структуры белка) различные полипептидные цепочки.
Водородная связь может возникать между боковыми радикалами остатков аминокислот, содержащих ОН-группы, например, между двумя остатками серина.
Кроме радикалов остатков серина, подобным образом водородные связи могут образовывать радикалы остатков треонина и тирозина.
В формировании третичной структуры белковой молекулы также принимают участие множество водородных связей, возникающих между боковыми радикалами, например: тирозина и глутаминовой кислоты, аспарагина и серина, лизина и глутамина и др.
Ионные связи возникают при сближении отрицательно заряженных радикалов остатков кислых аминокислот - аспарагиновой или глутаминовой - с положительно заряженными радикалами остатков основных аминокислот - лизина, аргинина или гистидина. Ионная связь между радикалами остатков аспарагиновой кислоты и лизина.
Гидрофобные взаимодействия возникают в воде, вследствие притяжения друг к другу неполярных радикалов остатков аминокислот. К аминокислотам с неполярными радикалами относятся, например, аланин, валин, лейцин, изолейцин, фенилаланин, метионин. Гидрофобное взаимодействие между боковыми радикалами остатков валина и аланина.
Чтобы избежать контакта с водой, неполярные радикалы остатков аминокислот стремятся собраться вместе внутри белковой молекулы. Белок сворачивается в компактное тело - глобулу (лат. «globulus» - шарик). Внутри глобулы образуется гидрофобное ядро, а снаружи нее находятся полярные радикалы остатков аминокислот, которые взаимодействуют с водой. Полярными радикалами обладают, например, кислые и основные аминокислоты, серии, треонин, тирозин, аспарагин, глутамин.
Таким образом, каждая белковая глобула окружена гидратной оболочкой, представленной так называемой «водяной шубой», включающей также структурированные молекулы воды, способные удерживать на поверхности глобулы до половины имеющихся в полипептидной цепочке гидрофобных радикалов. Этим обусловлена растворимость белка.
Благодаря множеству межрадикальных взаимодействий, отдельные участки белковой молекулы оказываются пространственно сближенными и зафиксированными относительно друг друга. В ходе образования третичной структуры белка формируется его активный центр. В результате белок приобретает способность выполнять свою биологическую функцию.
Первым белком, третичная структура которого была установлена, является миоглобин.
Третичные глобулы могут взаимодействовать между собой так, что возникает единая молекула. Такие глобулы называют субъединицами, а их объединение - четвертичной структурой белковой молекулы.
Четвертичная структура белка может строиться из различного числа субъединиц, удерживаемых вместе, главным образом, за счет слабых взаимодействий. Она присуща многим белкам.
Субъединицы, характерным образом расположенные в пространстве относительно друг друга, образуют олигомерный (мультимерный) комплекс. Способность белков к образованию таких структур позволяет объединять в единое целое несколько активных центров и взаимосвязанных функций, что очень важно для обеспечения протекания в клетке сложных обменных процессов.
Четвертичные структуры белков могут строиться из 2, 4, 6, 8,10, 12, 24 и более субъединиц и редко - из нечетного их числа. Например, четвертичную структуру гемоглобина образуют четыре попарно одинаковых субъединицы.
Четвертичная структура белковой молекулы является такой же уникальной, как и другие ее структуры. При этом вся трехмерная упаковка полипептидной цепи в пространстве определяется ее первичной структурой. Специфическая пространственная структура (конформация), в которой белковые молекулы обладают биологической активностью, называется нативиой (лат. nativus - врожденный).
Белки - это высокомолекулярные биополимерные органические соединения, мономерами которых являются аминокислоты. Белки были выделены в отдельный класс биологических молекул в XVIII в. в результате работ французского химика А. де Фуркруа. Впервые описал белки и предложил название протеины , что в современном понимании означает белок, голландский химик Е. Я. Берцелиус. Первое выделение белка (в виде клейковины) из пшеничной муки было осуществлено Я. Беккари. Особенностью исследований белков начале XXI в. одновременное получение данных о белковый состав целых клеток, тканей или организмов, чем занимается отдельная наука - протеомика .
Молекулярная масса белков от 5000 до 150000 Да и больше.
Одним из крупнейших единичных белков является титин (компонент саркомеров мышц), содержащий более 29 тыс. Аминокислот и имеет молекулярную массу 3000000 Да. Но самые большие по массе белки (более 40000000 Да) характерны для вирусов.
Химический состав . Состоят белки с С, Η, О, N ; в некоторых белках является S , часть белков образует комплексы с другими молекулами, которые содержат Р, Fe, Zn, Сu . Белки являются биополимеры из 20 различных мономеров - природных основных аминокислот. Белки могут образовывать интерполимерных комплексы с углеводами, липидами, нуклеиновыми кислотами, фосфорной кислотой и др.
Физико-химические свойства. Благодаря наличию свободных аминогрупп и карбоксильных групп белки характеризуются всеми свойствами кислот и оснований (амфотерные свойства ). Диссоциация аминокислот и карбоксильных белковых групп обусловливает электрофоретических подвижность белков. При низких значениях pH белкового раствора в нем преобладают положительно заряженные аминогруппы, поэтому белки находятся в катионной форме. При высоких значениях pH преобладают отрицательно заряженные СООН-группы и белки будут находиться в анионной форме. При некотором промежуточном значении pH аминогруппы и карбоксильные группы могут взаимодействовать между собой, тогда сумма зарядов равна нулю, и белки остаются неподвижными в электрическом поле (электрические свойства ). Высокая молекулярная масса оказывает белковым растворам свойств, характерных для коллоидных систем, а именно: способность к образованию гелей, высокая вязкость, малая скорость диффузии, высокая степень набухания, благодаря чему они связывают около 80-90% всей воды в организме (коллоидные свойства ). Распад белков происходит под действием кислот, щелочей или специфических ферментов-гидролаз, которые расщепляют их до пептидов и аминокислот. Синтез осуществляется с аминокислот с матричным принципом с помощью информационной РНК. Под влиянием различных чиникив белки могут сворачиваться и выпадать в осадок, теряя природные свойства. Отсутствие заряда и гидратной оболочки способствует сближению белковых молекул, их слипанию и выпадению в осадок. Это явление называется коагуляцией, она может быть обратной и необратимой. Необратимую коагуляцию можно рассматривать как денатурации белков. Денатурация - это процесс нарушения естественной структуры белков. При этом уменьшается растворимость белка, меняются форма и размеры молекул и др. Процесс денатурации является обратимым, то есть возвращение нормальных условиях сопровождается восста-
нием природной структуры белка. Такой процесс называется ренатурацией . Отсюда следует, что особенности белка определяются его первичной структурой. А вот процесс разрушения первичной структуры белков всегда необратим, он называется деструкцией . Свойства белков зависят от структуры, состава и последовательности расположения аминокислот.
Структура белков. Молекулы белков являются линейными полимерами, состоящие из аминокислот. Кроме последовательности аминокислот полипептидной цепи (первичная структура), для функционирования белков крайне важна трехмерная структура (вторичная третичная и четвертичная), которая содержится в результате взаимодействия структур ниже уровней и формируется в процессе свертывания белков. Трехмерная структура белков в нормальных природных условий, при которых белки выполняют свои биологические функции, называется нашивными состоянию белка, а сама структура - нативной конформацией Выделяют четыре уровня структуры белков.
Уровни организации белковых молекул
Первичная структура кодируется соответствующим геном, является специфической для каждого отдельного белка и в наибольшей степени определяет свойства сформированного белка. Вторичная структура представляет собой форму спирали (α-структуру) или структуру складчатого листа (β-конформация) и является термодинамически устойчивым состоянием полипептидной цепи и простой структурой конформации биомолекул. Примером белков с вторичной стуктуре в виде спирали являются белки-кератины (образуют волосы, ногти, перья и т.д.) и в виде складчатого листа - фиброин (белок шелка). Во вторичной структуре α-спиральные участки часто чередуются с линейными. Третичная структура возникает автоматически в результате взаимодействия аминокислотных остатков с молекулами воды. При этом гидрофобные радикалы "втягиваются" внутрь белковой молекулы, а гидрофильные группы ориентируются в сторону растворителя. Таким образом формируется компактная молекула белка, внутри которой практически отсутствуют молекулы воды. К белкам с третичной структурой относят миоглобин. Четвертичная структура возникает в результате сочетания нескольких субъединиц (протомеры ), что вместе выполняют общую

функцию. Такое сочетание называется белковым комплексом (мультимера , или эпимер ). Типичными белками четвертичной структуры является гемоглобин, СТМ, некоторые ферменты.
Конечная структура бывает очень сложной, а процесс ее принятия новосинтезированные по ли пептид ним цепочкой требует некоторого времени. Процесс принятия белком структуры называется свертыванием, или Фолдинг. Многие белки не способны завершить свертывания самостоятельно и достичь нативного состояния, часто через взаимодействие с другими белками клетки. Такие белки требуют внешней помощи от белков специального класса - молекулярных шаперонов. Большинство белков приобретает правильную конформации только в определенных условиях среды. При изменении этих условий белок денатурирует, меняя свою конформацию. Факторами, которые вызывают изменение конформации белков, является нагревание, излучение, сильные кислоты, сильные основания, концентрированные соли, тяжелые металлы, органические растворители и тому подобное.
Виды химических связей в белках. Аминокислоты способны образовывать ряд химических связей (пептидные, дисульфидные, водородные, ионные, гидрофобные) с различными функциональными группами, и это их свойство очень важно для структуры и функций белков.
Пептидный связь - это ковалентная азот-карбоновый полярный связь, которая образуется при взаимодействии NH 2 одной аминокислоты с СООН другой с выделением воды. Этот кислотоамидний связь (-CO-NH-) является основным химическим связью белковых молекул и определяет их первичную структуру и конформацию. Соединение, образующееся в результате конденсации двух аминокислот, является дипептид. На одном конце этой молекулы расположена аминогруппа, на другом - свободная карбоксильная. Благодаря этому дипептид может присоединять к себе другие аминокислоты.
Дисульфидная связь - это ковалентная полярный связь, которая образуется при взаимодействии сульфгидрильных групп (-SH ) радикалов серосодержащих аминокислот цистеина. Эта связь (-S-S-) может возникать как между различными участками одной полипептидной цепи, так и между различными цепями, определяя особенности белковых молекул. Устойчивость многих белков в значительной мере обусловлена количеством именно этих связей, как бы "прошивают" молекулы, придавая им прочности, нерастворимости (например, в коллагена кожи, кератина волос, шерсти).
Водородная связь - это полярный связь, возникает при взаимодействии электроположительного водорода с электроотрицательным кислорода в составе гидроксильной, карбоксильной и аминной групп разных аминокислот. Эти связи (-О-Н) гораздо слабее, чем пептидные, дисульфидные и ионные, но в силу своего количества (возникают между группами, которых больше всего в молекулах белков) они приобретают очень большое значение в стабилизации структуры белковых молекул.
Ионный связь - это электростатический полярный связь, возникающая между ионизированной положительно заряженной аминогруппой одной й аминокислоты и ионизированной отрицательно заряженной карбоксильной группой другой аминокислоты. Этот солевой связь (-СОО - HN 3+ -) может объединять как витки одного и более полипептидных цепей в белках третичной структуры, так и витки различных цепей в белках четвертичной структуры. В водной среде ионные связи значительно слабее, чем пептидные, и могут разрываться при изменении pH.
Гидрофобные взаимодействия - это неполярная связь между радикалами аминокислот, которые не несут электрического заряда и не растворяются в воде. Сближение этих радикалов обусловлено характером взаимодействия гидрофобных групп (-СН3, -С2Н5 и т. Д.) С водой. Эти связи (-R-R-) еще слабее, чем водородные, они поддерживают третичную и четвертичную структуру белков.
БИОЛОГИЯ + Гемомоглобин (от греч. Hаита - кровь и "лат. Globus - шар ) - сложный железосодержащий белок эритроцитов животных и человека; способен связываться с кислородом, обеспечивая его перенос в ткани. Кроме того, гемоглобин способен связывать в тканях небольшое количество сО, и освобождать его в лёгких. Гемоглобин с сложным белком класса хромопротеидов и содержит 1 ) белковую часть - глобин, которая состоит из четырех протомеры - двух идентичных а-цепей и двух идентичных β-цепей, 2 ) небелковую часть - гем, которая представлена четырьмя простетическими группами с координационным центром в виде Fe 2+ . Объединяются субъединицы водородными, ионными связями, но основной вклад в это взаимодействие вносят гидрофобные взаимодействия. Нормальным содержанием гемоглобина в крови человека вважасться: у мужчин - 130-170 г / л, у женщин - 120-150 г / л, у детей - 120-140 г / л. Гемоглобин высоко токсичен при попадании значительного его количества из эритроцитов в плазму крови (например, при переливании несовместимой крови ) . Учитывая высокую токсичность свободного гемоглобина, в организме существуют специальные системы для его связывания и обезвреживания. В частности, одним из компонентов системы обезвреживания гемоглобина является особый плазменный белок гаптоглобин, специфически связывает свободный глобин и глобин в составе гемоглобина.