В длинноватых периодах системы Менделеева, включающих так называемые вставные декады, содержится по десять элементов, у каких число электронов в наружной оболочке равно двум (два -электрона) и которые различаются лишь числом -электронов во второй снаружи оболочке. Такими элементами являются, например, элементы от скандия до цинка или от иттрия до кадмия.
Вторая снаружи оболочка играет меньшую роль в проявлении химических свойств, чем наружная оболочка, ибо связь электронов наружной оболочки с ядром слабее, чем во второй снаружи . Поэтому элементы, в атомах которых наружные оболочки построены одинаково и различны лишь вторые снаружи оболочки, гораздо меньше различаются друг от друга по химическим свойствам, чем элементы с различным строением наружных оболочек. Так, все элементы вставных декад, образующие в совокупности так называемые побочные подгруппы основных восьми групп менделеевской системы, являются металлами они все характеризуются переменной валентностью. В шестом периоде системы Менделеева , кроме вставной декады, имеются ещё 14 следующих за лантаном элементов, у каких различие в строении электронных оболочек проявляется лишь в третьей снаружи электронной оболочке (идёт заполнение /-мест в четвёртой оболочке при наличии заполненных мест Эти элементы (лантаниды) на-23
В результате опытов по определению зарядов атомных ядер к 4 г. общее число известных элементов - от водорода (Z=1) до урана (Z = 92) - составило 86. Пропущенными в системе оказались шесть элементов с атомными номерами = 43, 61, 72, 75, 85, 87. Однако, несмотря на эти пробелы, было уже ясно, что в первом периоде системы Менделеева должны находиться два элемента - водород и гелий, во 2-м и третьем - по восемь элементов, в четвёртом и пятом - по восемнадцать, в шестом - тридцать два элемента.13
До выяснения строения шестого периода системы Менделеева элемент № 72 искали среди редкоземельных элементов, и даже отдельные учёные объявляли уже об открытии этого элемента. Когда выяснилось, что в шестом периоде системы Менделеева
содержатся 32 элемента, из них 14 редкоземельных, то Н. Бор указал, что элемент № 72 стоит уже за редкоземельными, в четвёртой группе, и является, как ожидал Менделеев, аналогом циркония.
Точно так же Бор указал, что элемент № 75 стоит в седьмой группе и является предсказанным Менделеевым аналогом марганца. Действительно, в 3 г. в цирконовых рудах был открыт элемент № 72, названный гафнием, причём оказалось, что всё, называвшееся до того цирконием, было по сути смесью циркония и гафния.
В том же 3 г. были предприняты поиски элемента № 75 в разных минералах, где, исходя из родства с марганцем, ожидалось наличие этого элемента. Химические операции для выделения этого элемента также основывались на предполагаемой близости его по свойствам к марганцу. Поиски увенчались в 5 г. открытием нового элемента, названного рением.24
Но это не исчерпывало ещё всех возможностей искусственного получения новых элементов. Граница периодической системы в области лёгких ядер задана водородом, ибо не может быть элемента с зарядом ядра меньше единицы.
Но в области тяжёлых ядер эта граница отнюдь не задана ураном. По правде, отсутствие в природе более тяжёлых, чем уран, элементов говорит только о том, что периоды полураспада таких элементов значительно меньше возраста Земли. Поэтому среди трёх древ естественного радиоактивного распада, включающих изотопы с массовыми числами А = 4п, 4л- -2 и 4 4-3, сохранились лишь ветви, начинающиеся долгопериодными изотопами ТЬ, и 2 и Все короткопериодные ветви, образно выражаясь, высохли и отвалились в незапамятные времена. Кроме того, полностью высохло и погибло четвёртое древо радиоактивного распада, включающее изотопы с массовыми числами Л = 4га + 1, если когда-либо и были на Земле изотопы этого ряда.
Как известно, в четвёртом и пятом периодах системы Менделеева содержится по 18 элементов, в шестом же периоде находится 32 элемента, ибо между элементом третьей группы лантаном (№ 57) и элементом четвёртой группы гафнием (№ 72) стоят ещё четырнадцать схожих с лантаном редкоземельных элементов.
После выяснения строения седьмого периода системы Д. И. Менделеева стало ясно, что в периодической системе за первым периодом из двух элементов следуют два периода по восьми элементов, затем два периода по восемнадцати элементов и два периода по тридцать два элемента. Во 2-м таком периоде, который должен заканчиваться элемен-. том № , пока нехватает ещё семнадцати элементов из них двух нехватает для завершения семейства актинидов, а элемент № должен уже располагаться в четвёртой группе периодической системы, являясь аналогом гафния.
При п + / = 5 заполняются уровни л = 3, 1 = 2 (М), л = 4, / = 1 (4р) и, наконец, л = 5, / = О (55). Если до кальция заполнение электронных уровней шло в порядке возрастания номеров электронных оболочек (15, 25, 2р, Зз, Зр, 45), то после заполнения 5-мест четвёртой электронной оболочки вместо продолжения заполнения этой оболочки /7-электронами начинается заполнение предыдущей, третьей, оболочки -электронами. Всего в каждой оболочке может быть, как ясно из сказанного выше, 10 -электронов. Соответственно этому за кальцием в периодической системе следуют 10 элементов от скандия (3 452) до цинка (3 452), в атомах которых заполняется -слой третьей оболочки, и лишь затем заполняется р-слой четвёртой оболочки-от галлия (3(Щз р) до криптона ЗйЩз р). В рубидии и стронции, начинающих пятый период, появляются 55- и 552-электроны.19
Исследования последних пятнадцати лет привели к искусственному получению ряда короткопериодных. изотопов ядер элементов от ртути до урана, к воскрешению давно погибших в природе родителей урана, протактиния и тория - заурановых элементов от № 93 до № -и к воссозданию четвёртого ряда распада, включающего изотопы с массовыми числами /4 = 4ге- -1. Этот ряд можно условно назвать рядом распада нептуния, потому что самым долгоживущим в ряду омвзался изотоп элемента № 93 - период полураспада которого близок к 2 млн. лет.
Шестой период начинается заполнением двух мест для s-электронов в шестой оболочке, так что строение наружных оболочек атомов элемента № 56 - бария - имеет вид 4s j0 d 05s2p66s2. Очевидно, что при дальнейшем увеличении числа электронов в атомах элементов, следующих за барием, может итти заполнение оболочек или 4/-, или bd- или, наконец, бр-электронами. Уже в четвёртом и пятом периодах системы Менделеева , содержащих по 18 элементов, заполнение d-мест второй снаружи оболочки происходило раньше заполнения р-мест наружной оболочки. Так и в шестом периоде заполнение 6/7-мест начинается только с элемента № 81-таллия.- В атомах же двадцати четырёх элементов, расположенных между барием и таллием, идёт заполнение четвёртой оболочки /-электронами и пятой оболочки d-элек-тронами.
Закономерности изменения активности d-элементов в периоде
Рубрики
Выберите рубрику 1. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА НЕФТИ, ПРИРОДНОГО ГАЗА 3. ОСНОВЫ РАЗРАБОТКИ НЕФТЯНЫХ МЕСТОРОЖДЕНИЙ И ЭКСПЛУАТА 3.1. Фонтанная эксплуатация нефтяных скважин 3.4. Эксплуатация скважин погружными электроцентробежны 3.6. Понятие о разработке нефтяных и газовых скважин 7. МЕТОДЫ ВОЗДЕЙСТВИЯ НА ПРИЗАБОЙНУЮ ЗОНУ ПЛАСТА ОСНОВНЫЕ УЗЛЫ ИСПЫТАТЕЛЯ ПЛАСТОВ ВИНТОВЫЕ ЗАБОЙНЫЕ ДВИГАТЕЛИ АВАРИЙНЫЕ И ОСОБЫЕ РЕЖИМЫ РАБОТЫ ЭЛЕКТРООБОРУДОВАНИЯ АГРЕГАТЫ ДЛЯ РЕМОНТА И БУРЕНИЯ СКВАЖИН АНАЛИЗ ПРИЧИН МАЛОДЕБИТНОСТИ СКВАЖИН АНАЛИЗ ТЕХНОЛОГИЙ КАПИТАЛЬНЫХ РЕМОНТОВ СКВАЖИН Арматура устьевая АСФАЛЬТОСМОЛО-ПАРАФИНОВЫЕ ОТЛОЖЕНИЯ Без рубрики БЕЗДЫМНОЕ СЖИГАНИЕ ГАЗА БЕСШТАНГОВЫЕ СКВАЖИННЫЕ НАСОСНЫЕ УСТАНОВКИ блогун БЛОКИ ЦИРКУЛЯЦИОННЫХ СИСТЕМ. борьба с гидратами БОРЬБА С ОТЛОЖЕНИЕМ ПАРАФИНА В ПОДЪЕМНЫХ ТРУБАХ бурение Бурение боковых стволов БУРЕНИЕ НАКЛОННО НАПРАВЛЕННЫХ И ГОРИЗОНТАЛЬНЫХ СКВАЖИН Бурение скважин БУРИЛЬНАЯ КОЛОННА БУРОВЫЕ АВТОМАТИЧЕСКИЕ СТАЦИОНАРНЫЕ КЛЮЧИ БУРОВЫЕ АГРЕГАТЫ И УСТАНОВКИ ДЛЯ ГЕОЛОГО-РАЗВЕДОЧНОГО БУРЕНИЯ БУРОВЫЕ ВЫШКИ БУРОВЫЕ НАСОСЫ БУРОВЫЕ НАСОСЫ БУРОВЫЕ РУКАВА БУРОВЫЕ УСТАНОВКИ В МНОГОЛЕТНЕМЕРЗЛЫХ ПОРОДАХ (ММП) ВЕНТИЛИ. ВИДЫ НЕОДНОРОДНОСТЕЙ СТРОЕНИЯ НЕФТЯНЫХ ЗАЛЕЖЕЙ Виды скважин ВИНТОВЫЕ ПОГРУЖНЫЕ НАСОСЫ С ПРИВОДОМ НА УСТЬЕ ВЛАГОСОДЕРЖАНИЕ И ГИДРАТЫ ПРИРОДНЫХ ГАЗОВ СОСТАВ ГИДРАТ Влияние различных факторов на характеристики ВЗД ВОПРОСЫ ОПТИМИЗАЦИИ РАБОТЫ СИСТЕМЫ ПЛАСТ — УЭЦН ВЫБОР ОБОРУДОВАНИЯ И РЕЖИМА РАБОТЫ УЭЦН ВЫБОР СТАНКА-КАЧАЛКИ Газлифтная установка ЛН Газлифтная эксплуатация нефтяных скважин Газлифтный способ добычи нефти ГАЗЫ НЕФТЯНЫХ И ГАЗОВЫХ МЕСТОРОЖДЕНИЙ И ИХ СВОЙСТВА ГИДРАТООБРАЗОВАНИЕ В ГАЗОКОНДЕНСАТНЫХ СКВАЖИНАХ ГИДРАТООБРАЗОВАНИЕ В СИСТЕМЕ СБОРА НЕФТИ гидрозащита погружного электродвигателя ГИДРОКЛЮЧ ГКШ-1500МТ гидропоршневой насос Глава 8. СРЕДСТВА И МЕТОДЫ ГРАДУИРОВКИ И ПОВЕРКИ РАСХОДОИЗМЕРИТЕЛЬНЫХ СИСТЕМ ГЛУБИННЫЕ НАСОСЫ Горизонтальное бурение ГОРНО-ГЕОЛОГИЧЕСКИЕ УСЛОВИЯ БУРЕНИЯ НЕФТЯНЫХ И ГАЗОВЫХ СКВАЖИН ГРАНУЛОМЕТРИЧЕСКИЙ (МЕХАНИЧЕСКИЙ) СОСТАВ ПОРОД ДАЛЬНИЙ ТРАНСПОРТ НЕФТИ И ГАЗА ДЕФОРМАЦИОННЫЕ МАНОМЕТРЫ Диафрагменные электронасосы ДИЗЕЛЬ-ГИДРАВЛИЧЕСКИЙ АГРЕГАТ САТ-450 ДИЗЕЛЬНЫЕ И ДИЗЕЛЬ-ГИДРАВЛИЧЕСКИЕ АГРЕГАТЫ ДИНАМОМЕТРИРОВАНИЕ УСТАНОВОК ДНУ С ЛМП КОНСТРУКЦИИ ОАО «ОРЕНБУРГНЕФТЬ» добыча нефти добыча нефти в осложненых условиях ДОБЫЧА НЕФТИ С ПРИМЕНЕНИЕМ ШСНУ ЖИДКОСТНЫЕ МАНОМЕТРЫ ЗАБОЙНЫЕ ДВИГАТЕЛИ Закачка растворов кислот в скважину ЗАПОРНАЯ АРМАТУРА. ЗАЩИТа НЕФТЕПРОМЫСЛОВОГО ОБОРУДОВАНИЯ ОТ КОРРОЗИИ ЗАЩИТА ОТ КОРРОЗИИ НЕФТЕПРОМЫСЛОВОГО ОБОРУДОВАНИЯ ИЗМЕНЕНИЕ КУРСА СТВОЛА СКВАЖИНЫ измерение давления, расхода, жидкости, газа и пара ИЗМЕРЕНИЕ КОЛИЧЕСТВА ЖИДКОСТЕЙ И ГАЗОВ ИЗМЕРЕНИЕ РАСХОДА ЖИДКОСТЕЙ, ГАЗОВ И ПАРОВ ИЗМЕРЕНИЕ УРОВНЯ ЖИДКОСТЕЙ ИЗМЕРЕНИЯ ПРОДУКЦИИ МАЛОДЕБИТНЫХ ИНФОРМАЦИОННЫЕ ТЕХНОЛОГИИ В НЕФТЕГАЗОДОБЫЧЕ ИСПЫТАНИЕ СКВАЖИННЫХ ЭЛЕКТРОНАГРЕВАТЕЛЕЙ Исследование глубинно-насосных скважин ИССЛЕДОВАНИЕ ЭФФЕКТИВНОСТИ кабель УЭЦН капитальный ремонт скважин Комплекс оборудования типа КОС и КОС1 КОНСТРУКЦИЯ ВИНТОВОГО ШТАНГОВОГО НАСОСА КОНСТРУКЦИЯ КЛАПАННОГО УЗЛА коррозия Краны. КРЕПЛЕНИЕ СКВАЖИН КТППН МАНИФОЛЬДЫ Маятниковая компоновка Меры безопасности при приготовлении растворов кислоты МЕТОДИКА РАСЧЕТА БУРИЛЬНЫХ КОЛОНН МЕТОДЫ БОРЬБЫ С ОТЛОЖЕНИЯМИ ПАРАФИНА В ФОНТАННЫХ СКВАЖИНАХ Методы воздействия на призабойную зону для увеличения нефтеотдачи пластов МЕТОДЫ И СРЕДСТВА ИЗМЕРЕНИЯ УРОВНЯ ЖИДКОСТЕЙ Методы изучения разрезов скважин. МЕТОДЫ КОСВЕННЫХ ИЗМЕРЕНИЙ ДАВЛЕНИЯ МЕТОДЫ УДАЛЕНИЯ СОЛЕЙ МЕХАНИЗМЫ ПЕРЕДВИЖЕНИЯ И ВЫРАВНИВАНИЯ БУРОВЫХ УСТАНОВОК МЕХАНИЗМЫ ПЕРЕМЕЩЕНИЯ И ВЫРАВНИВАНИЯ МЕХАНИЗМЫ ПРИ СПУСКО-ПОДЪЕМНЫХ ОПЕРАЦИЙ ПРИ БУРЕНИИ НАГРУЗКИ, ДЕЙСТВУЮЩИЕ НА УСТАНОВКУ Наземное оборудование Насосная эксплуатация скважин НАСОСНО-КОМПРЕССОРНЫЕ ТРУБЫ неоднородный пласт Нефть и нефтепродукты Новости портала НОВЫЕ ТЕХНОЛОГИЧЕСКИЕ И ТЕХНИЧЕСКИЕ ОБЕСПЕЧЕНИЕ ЭКОЛОГИЧЕСКОЙ БЕЗОПАСНОСТИ ПРОЦЕССОВ ДОБЫЧИ ОБОРУДОВАНИЕ ГАЗЛИФТНЫХ СКВАЖИН ОБОРУДОВАНИЕ ДЛЯ МЕХАНИЗАЦИИ СПУСКО-ПОДЪЕМНЫХ ОПЕРАЦИЙ Оборудование для нефти и газа ОБОРУДОВАНИЕ ДЛЯ ОДНОВРЕМЕННОЙ РАЗДЕЛЬНОЙ ЭКСПЛУАТАЦ ОБОРУДОВАНИЕ ДЛЯ ПРЕДУСМОТРЕНИЯ ОТКРЫТЫХ ФОНТАНОВ ОБОРУДОВАНИЕ ОБЩЕГО НАЗНАЧЕНИЯ Оборудование ствола скважины, законченной бурением ОБОРУДОВАНИЕ УСТЬЯ КОМПРЕССОРНЫХ СКВАЖИН ОБОРУДОВАНИЕ УСТЬЯ СКВАЖИНЫ Оборудование устья скважины для эксплуатации УЭЦН ОБОРУДОВАНИЕ ФОНТАННЫХ СКВАЖИН ОБОРУДОВАНИЕ ФОНТАННЫХ СКВАЖИН обработка призабойной зоны ОБРАЗОВАНИЕ ГИДРАТОВ И МЕТОДЫ БОРЬБЫ С НИМИ ОБРАЗОВАНИЕ КРИСТАЛЛОГИДРАТОВ В НЕФТЯНЫХ СКВАЖИНАХ ОБЩИЕ ПОНЯТИЯ О ПОДЗЕМНОМ И КАПИТАЛЬНОМ РЕМОНТЕ ОБЩИЕ ПОНЯТИЯ О СТРОИТЕЛЬСТВЕ СКВАЖИН ОГРАНИЧЕНИЕ ПРИТОКА ПЛАСТОВЫХ ВОД Опасные и вредные физические факторы ОПРЕДЕЛЕНИЕ ДАВЛЕНИЯ НА ВЫХОДЕ НАСОСА ОПРОБОВАНИЕ ПЕРСПЕКТИВНЫХ ГОРИЗОНТОВ ОПТИМИЗАЦИЯ РЕЖИМА РАБОТЫ ШСНУ ОПЫТ ЭКСПЛУАТАЦИИ ДНУ С ГИБКИМ ТЯГОВЫМ ЭЛЕМЕНТОМ ОСВОЕНИЕ И ИСПЫТАНИЕ СКВАЖИН ОСВОЕНИЕ И ПУСК В РАБОТУ ФОНТАННЫХ СКВАЖИН ОСЛОЖНЕНИЯ В ПРОЦЕССЕ УГЛУБЛЕНИЯ СКВАЖИНЫ ОСНОВНЫЕ ПОНЯТИЯ И ПОЛОЖЕНИЯ ОСНОВНЫЕ ПОНЯТИЯ И ПОЛОЖЕНИЯ ОСНОВНЫЕ СВЕДЕНИЯ О НЕФТЯНЫХ, ГАЗОВЫХ И ГАЗОКОНДЕНСАТНЫ ОСНОВЫ ГИДРАВЛИЧЕСКИХ РАСЧЕТОВ В БУРЕНИИ ОСНОВЫ НЕФТЕГАЗОДОБЫЧИ ОСНОВЫ ПРОЕКТИРОВАНИЯ НАПРАВЛЕННЫХ СКВАЖИН ОСНОВЫ ПРОМЫШЛЕННОЙ БЕЗОПАСНОСТИ ОЧИСТКА БУРЯЩЕЙСЯ СКВАЖИНЫ ОТ ШЛАМА ОЧИСТКА ПОПУТНЫХ ГАЗОВ пайка и наплавка ПАКЕР ГИДРОМЕХАНИЧЕСКИЙ ДВУХМАНЖЕТНЫЙ ПГМД1 ПАКЕРЫ ГИДРОМЕХАНИЧЕСКИЕ, ГИДРАВЛИЧЕСКИЕ И МЕХАНИЧЕСКИЕ ПАКЕРЫ ДЛЯ ИСПЫТАНИЯ КОЛОНН ПАКЕРЫ РЕЗИНОВО-МЕТАЛЛИЧЕСКОГО ПЕРЕКРЫТИЯ ПРМП-1 ПАКЕРЫ И ЯКОРИ ПАРАМЕТРЫ И КОМПЛЕКТНОСТЬ ЦИРКУЛЯЦИОННЫХ СИСТЕМ Параметры талевых блоков для работы с АСП ПЕРВИЧНОЕ ВСКРЫТИЕ ПРОДУКТИВНЫХ ПЛАСТОВ ПЕРВИЧНЫЕ СПОСОБЫ ЦЕМЕНТИРОВАНИЯ ПЕРЕДВИЖНЫЕ НАСОСНЫЕ УСТАНОВКИ И АГРЕГАТЫ ПЕРЕРАБОТКА ЛОВУШЕЧНЫХ НЕФТЕЙ (НЕФТЕШЛАМОВ) ПЕРИОДИЧЕСКИЙ ГАЗЛИФТ ПЕРСПЕКТИВЫ ИСПОЛЬЗОВАНИЯ ДНУ ПОВЫШЕНИЕ ЭФФЕКТИВНОСТИ ПОВЫШЕНИЕ ЭФФЕКТИВНОСТИ РАБОТЫ ШСНУ Погружение насосов под динамический уровень Подземное оборудование фонтанных скважин ПОДЪЕМ ВЯЗКОЙ ЖИДКОСТИ ПО ЗАТРУБНОМУ ПРОСТРАНСТВУ СКВАЖИНЫ ПОРОДОРАЗРУШАЮЩИЕ ИНСТРУМЕНТЫ ПОРШНЕВЫЕ МАНОМЕТРЫ Потери давления при движении жидкости по нкт Правила безопасности при эксплуатации скважин Правила ведения ремонтных работ в скважинах РД 153-39-023-97 ПРЕДУПРЕЖДЕНИЕ ОБРАЗОВАНИЯ СОЛЕЙ ПРЕДУПРЕЖДЕНИЯ ОБРАЗОВАНИЯ АСПО ПРЕДУПРЕЖДЕНИЯ ОБРАЗОВАНИЯ АСПО при работе ШГН ПРЕИМУЩЕСТВА ДЛИННОХОДОВЫХ Приготовление растворов кислот. ПРИГОТОВЛЕНИЕ, ОЧИСТКА БУРОВЫХ РАСТВОРОВ ПРИМЕНЕНИЕ СТРУЙНЫХ КОМПРЕССОРОВ ДЛЯ УТИЛИЗАЦИИ ПРИМЕНЕНИЕ УЭЦН В СКВАЖИНАХ ОАО «ОРЕНБУРГНЕФТЬ» ПРИНЦИП ДЕЙСТВИЯ И ОСОБЕННОСТИ КОНСТРУКЦИИ ДНУ С ЛМП ПРИЧИНЫ И АНАЛИЗ АВАРИЙ ПРОГНОЗИРОВАНИЕ ОТЛОЖЕНИЯ НОС ПРИ ДОБЫЧЕ НЕФТИ ПРОЕКТИРОВАНИЕ ТРАЕКТОРИИ НАПРАВЛЕННЫХ СКВАЖИН ПРОЕКТИРОВАНИЕ, ОБУСТРОЙСТВО И АНАЛИЗ РАЗРАБОТКИ УГЛЕВОДОРОДНЫХ МЕСТОРОЖДЕНИЙ Производительность насоса ПРОМЫВКА СКВАЖИН И БУРОВЫЕ РАСТВОРЫ ПРОМЫСЛОВЫЕ ИССЛЕДОВАНИЯ ПРОМЫСЛОВЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ ЗОН ОБРАЗОВАНИЯ НОС ПРОМЫСЛОВЫЙ СБОР И ПОДГОТОВКА НЕФТИ, ГАЗА И ВОДЫ ПРОТИВОВЫБРОСОВОЕ ОБОРУДОВАНИЕ ПУТИ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ЭКСПЛУАТАЦИИ СКВАЖИН РАЗМЕЩЕНИЕ ЭКСПЛУАТАЦИОННЫХ И НАГНЕТАТЕЛЬНЫХ СКВАЖИН НА Разное РАЗРУШЕНИЕ ГОРНЫХ ПОРОД РАСПРЕДЕЛЕНИЕ ОБРЫВОВ ПО ДЛИНЕ КОЛОННЫ ШТАНГ РАСЧЕТ ДНУ РАСЧЕТ ПРОИЗВОДИТЕЛЬНОСТИ ДНУ Регулирование свойств цементного раствора и камня с помощью реагентов Режимы добывающих и нагнетательных скважин. РЕЗЕРВЫ СНИЖЕНИЯ ЭНЕРГОПОТРЕБЛЕНИЯ ПРИ ЭКСПЛУАТАЦИ РЕМОНТЫ ПО ЭКОЛОГИЧЕСКОМУ ОЗДОРОВЛЕНИЮ ФОНДА СКВАЖИН РОЛЬ ФОНТАННЫХ ТРУБ САМОХОДНЫЕ УСТАНОВКИ С ПОДВИЖНЫМ… СЕТКА РАЗМЕЩЕНИЯ СКВАЖИН СИСТЕМЫ УЛАВЛИВАНИЯ ЛЕГКИХ УГЛЕВОДОРОДОВ Скважинные уплотнители (пакеры) Скважинные центробежные насосы для добычи нефти СОСТАВ И НЕКОТОРЫЕ СВОЙСТВА ВОД НЕФТЯНЫХ И ГАЗОВЫХ МЕСТ СПЕЦИАЛЬНЫЙ НЕВСТАВНОЙ ШТАНГОВЫЙ НАСОС СПОСОБЫ ДОБЫЧИ НЕФТИ, ПРИМЕНЯЕМЫЕ НА МЕСТОРОЖДЕНИЯХ ОАО СПОСОБЫ ОЦЕНКИ СОСТОЯНИЯ ПЗП СРАВНИТЕЛЬНЫЕ ИСПЫТАНИЯ НАСОСНЫХ УСТАНОВОК СРЕДСТВА И МЕТОДЫ ПОВЕРКИ СЧЕТЧИКОВ КОЛИЧЕСТВА ГАЗОВ СРЕДСТВА И МЕТОДЫ ПОВЕРКИ СЧЕТЧИКОВ КОЛИЧЕСТВА ЖИДКОСТЕЙ СТАДИИ РАЗРАБОТКИ МЕСТОРОЖДЕНИЙ Станки-качалки Струйные насосы струйный насос СЧЕТЧИКИ КОЛИЧЕСТВА ГАЗОВ СЧЕТЧИКИ КОЛИЧЕСТВА ЖИДКОСТЕЙ ТАЛЕВЫЕ МЕХАНИЗМЫ ТЕМПЕРАТУРА И ДАВЛЕНИЕ В ГОРНЫХ ПОРОДАХ И СКВАЖИНАХ Теоретические основы безопасности ТЕХНИКА ИЗМЕРЕНИЯ РАСХОДА Техническая физика ТРАЕКТОРИЮ ПЕРЕМЕЩЕНИЯ ЗАБОЯ СКВАЖИНЫ Трубы УКАЗАНИЯ ПО РАСЧЕТУ ТОКОВ КОРОТКОГО ЗАМЫКАНИЯ УСЛОВИЯ ПРИТОКА ЖИДКОСТИ И ГАЗА В СКВАЖИНЫ Установки гидропоршневых насосов для добычи нефти Установки погружных винтовых электронасосов Установки погружных диафрагменных электронасосов Устьевое оборудование УТЯЖЕЛЕННЫЕ БУРИЛЬНЫЕ ТРУБЫ УЭЦН уэцн полностью ФАКТОРЫ, ВЛИЯЮЩИЕ НА ИНТЕНСИВНОСТЬ ОБРАЗОВАНИЯ АСПО Физико-механические свойства пород-коллекторов ФИЗИЧЕСКАЯ ХАРАКТЕРИСТИКА ГАЗОВ НЕФТЯНЫХ И ГАЗОВЫХ МЕСТ ФИЛЬТРЫ Фонтанный способ добычи нефти ЦЕМЕНТИРОВАНИЕ СКВАЖИН ЦИРКУЛЯЦИОННЫЕ СИСТЕМЫ БУРОВЫХ УСТАНОВОК Шлакопесчаные цементы Шлакопесчаные цементы совместного помола Штанги насосные (ШН) ШТАНГОВЫЕ НАСОСНЫЕ УСТАНОВКИ (ШСНУ) ШТАНГОВЫЕ НАСОСЫ ДЛЯ ПОДЪЕМА ВЯЗКОЙ НЕФТИ ШТАНГОВЫЕ СКВАЖИННЫЕ НАСОСЫ Штанговые скважинные насосы ШСН ЭКСПЛУАТАЦИЯ ГАЗОВЫХ СКВАЖИН эксплуатация малодебитных скважин ЭКСПЛУАТАЦИЯ МАЛОДЕБИТНЫХ СКВАЖИН НА НЕПРЕРЫВНОМ РЕЖИМЕ ЭКСПЛУАТАЦИЯ ОБВОДНЕННЫХ ПАРАФИНСОДЕРЖАЩИХ СКВАЖИН ЭКСПЛУАТАЦИЯ СКВАЖИН ЭКСПЛУАТАЦИЯ СКВАЖИН УЭЦН ЭЛЕКТРОДЕГИДРАТОР. ЭЛЕКТРОДИАФРАГМЕННЫЙ НАСОС энергосбережение скважинного электронасосного агрегата ЯКОРИd-элементы и их соединения обладают рядом характерных свойств: переменные состояния окисления; способность к образованию комплексных ионов; образование окрашенных соединений.
Цинк не входит в число переходных элементов. Его физические и химические свойства не позволяют относить его к переходным металлам. В частности, в своих соединениях он обнаруживает только одно состояние окисления и не проявляет каталитической активности.
d-Элементы обладают некоторыми особенностями по сравнению с элементами главных подгрупп.
1. У d-элементов лишь небольшая часть валентных электронов делокализована по всему кристаллу (тогда как у щелочных и щелочноземельных металлов валентные электроны полностью отданы в коллективное пользование). Остальные d-электроны участвуют в образовании направленных ковалентных связей между соседними атомами. Таким образом, эти элементы в кристаллическом состоянии обладают не чисто металлической связью, а ковалентно-металлической. Поэтому все они твердые (кроме Hg) и тугоплавкие (за исключением Zn, Cd) металлы.
Наиболее тугоплавки металлы VВ и VIВ подгрупп. У них заполняется электронами половина d-подуровня и реализуется максимально возможное число неспаренных электронов, а следовательно, наибольшее число ковалентных связей. Дальнейшее заполнение приводит к уменьшению числа ковалентных связей и падению температур плавления.
2. Вследствие незаполненности d-оболочек и наличия близких по энергии незаполненных ns- и np-уровней, d-элементы склонны к комплексообразованию; их комплексные соединения, как правило, окрашены и парамагнитны.
3. d-Элементы чаще, чем элементы главных подгрупп, образуют соединения переменного состава (оксиды, гидриды, карбиды, силициды, нитриды, бориды). Кроме того, они образуют сплавы между собой и с другими металлами, а также интерметаллические соединения.
4. Для d-элементов характерен большой набор валентных состояний (табл. 8.10) и, как следствие этого, изменение кислотно-основных и окислительно-восстановительных свойств в широких пределах.
Поскольку часть валентных электронов находится на s-орбиталях, то проявляемые ими низшие степени окисления как правило равны двум. Исключение составляют элементы, ионы которых Э +3 и Э + имеют устойчивые конфигурации d 0 , d 5 и d 10: Sc 3+ , Fe 3+ , Cr + , Cu + , Ag + , Au + .
Соединения, в которых d-элементы находятся в низшей степени окисления, образуют кристаллы ионного типа, в химических реакциях проявляют основные свойства и являются, как правило, восстановителями.
Устойчивость соединений, в которых d-элементы находятся в высшей степени окисления (равной номеру группы),увеличивается в пределах каждого переходного ряда слева направо, достигая максимума для 3d-элементов у Mn, а во втором и третьем переходных рядах – у Ru и Os соответственно. В пределах одной подгруппы стабильность соединений высшей степени окисления уменьшается в ряду 5d > 4d > 3d, о чем свидетельствует характер изменения энергии Гиббса (изобарно-изотермического потенциала) однотипных соединений, например:
Это явление связано с тем, что при увеличении главного квантового числа в пределах одной подгруппы происходит уменьшение разности энергий (n – 1)d- и ns-подуровней. Этим соединениям свойственны ковалентно-полярные связи. Они имеют кислотный характер и являются окислителями (CrO 3 и K 2 CrO 4 , Mn 2 O 7 и KMnO 4).
Соединения, в которых d-электроны находятся в промежуточных степенях окисления, проявляют амфотерные свойства и окислительно-восстановительную двойственность.
5. Сходство d-элементов с элементами главных подгрупп Э(0) в полной мере проявляется у элементов третьей группы ns 2 np 1 и (n – 1)d 1 ns 2 . С возрастанием номера группы оно уменьшается; элементы VIIIА подгруппы – газы, VIIIВ – металлы. В первой группе снова появляется отдаленное сходство (все элементы – металлы), а элементы IВ подгруппы – хорошие проводники; это сходство усиливается во второй группе, так как d-элементы Zn, Cd и Hg не участвуют в образовании химической связи.
6. d-элементы IIIВ–VIIВ подгрупп в высших степенях окисления по свойствам подобны соответствующим p-элементам. Так, в высших степенях окисления Mn (VII) и Cl (VII) являются электронными аналогами. Подобие электронных конфигураций (s 2 p 6) приводит к подобию свойств соединений семивалентных марганца и хлора. Mn 2 O 7 и Cl 2 O 7 в обычных условиях малоустойчивые жидкости, являющиеся ангидридами сильных кислот с общей формулой НЭО 4 . В низших степенях окисления марганец и хлор имеют различное электронное строение, что обусловливает резкое отличие свойств их соединений. Например, низший оксид хлора Cl 2 O (s 2 p 4) – газообразное вещество, являющееся ангидридом хлорноватистой кислоты (HClO), тогда как низший оксид марганца MnO (d 5) представляет собой твердое кристаллическое вещество основного характера.
7. Как известно, восстановительная способность металла определяется не только его энергией ионизации (М – ne – → М n + ; +∆H иониз), но и энтальпией гидратации образовавшегося катиона (М n + + mH 2 O → М n + ·mH 2 O; –∆H гидр). Энергии ионизации d-элементов в сравнении с другими металлами велики, но они компенсируются большими энтальпиями гидратации их ионов. Вследствие этого электродные потенциалы большинства d-элементов отрицательны.
В периоде с ростом Z восстановительные свойства металлов уменьшаются, достигая минимума у элементов IВ группы. Тяжелые металлы VIIIВ и IВ групп за свою инертность названы благородными.
Окислительно-восстановительные тенденции соединений d-элементов определяются изменением устойчивости высших и низших степеней окисления в зависимости от положения их в периодической системе. Соединения с максимальной степенью окисления элемента проявляют исключительно окислительные свойства, а с низшей – восстановительные. Mn(OH) 2 легко окисляется на воздухе Mn(OH) 2 + 1/2O 2 = MnO 2 + H 2 O. Соединения Mn(IV) легко восстанавливаются до Mn (II): MnO 2 + 4HCl = MnCl 2 + Cl 2 + 2H 2 O, но сильными окислителями окисляется до Mn (VII). Перманганат-ион MnO 4 – может быть только окислителем.
Поскольку для d-элементов в пределах подгруппы устойчивость высших степеней окисления сверху вниз растет, то окислительные свойства соединений высшей степени окисления резко падают. Так, соединения хрома (VI) (CrO 3 , K 2 CrO 4 , K 2 Cr 2 O 7) и марганца(VII) (Mn 2 O 7 , KMnO 4) – сильные окислители, а WO 3 , Re 2 O 7 и соли соответствующих им кислот (H 2 WO 4 , HReO 4) восстанавливаются с трудом.
8. На кислотно-основные свойства гидроксидов d-элементов влияют те же факторы (величина ионного радиуса и заряд иона), что и на гидроксиды p-элементов.
Гидроксиды низших степеней окисления d-элементов обычно проявляют основные свойства, а отвечающие высшим степеням окисления – кислотные. В промежуточных степенях окисления гидроксиды амфотерны. Особенно отчетливо изменение кислотно-основных свойств гидроксидов при изменении степени окисления проявляется в соединенинях марганца. В ряду Mn(OH) 2 – Mn(OH) 3 – Mn(OH) 4 – H 2 MnO 4 – HMnO 4 свойства гидроксидов меняются от слабого основания Mn(OH) 2 через амфотерные Mn(OH) 3 и Mn(OH) 4 к сильным кислотам H 2 MnO 4 и HMnO 4 .
В пределах одной подгруппы гидроксиды d-элементов одинаковой степени окисления характеризуются увеличением основных свойств при движении сверху вниз. Например, в IIIВ группе Sc(OH) 3 – слабое, а La(OH) 3 – сильное основание. Элементы IVВ группы Ti, Zn, Hf образуют амфотерные гидроксиды Э(OH) 4 , но кислотные свойства их ослабевают при переходе от Ti к Hf.
9. Отличительной особенностью переходных элементов является образование фаз переменного состава. Это, во-первых, твердые растворы внедрения и замещения и, во-вторых, соединения переменного состава. Твердые растворы образуются элементами с близкими электроотрицательностями, атомными радиусами и одинаковыми кристаллическими решетками. Чем больше отличаются элементы по своей природе, тем менее они растворяются друг в друге и тем более склонны к образованию химических соединений. Такие соединения могут иметь как постоянный, так и переменный состав. В отличие от твердых растворов, в которых сохраняется решетка одного из компонентов, для соединений характерно образование новой решетки и новых химических связей. Другими словами, к химическим соединениям относят лишь те фазы переменного состава, которые резко отличаются по строению и свойствам от исходных.
Для соединений переменного состава характерны следующие особенности:
а) Состав этих соединений зависит от способа получения. Так, в зависимости от условий синтеза оксиды титана имеют состав TiO 1,2–1,5 и TiO 1,9–2,0 ; карбиды титана и ванадия – TiC 0,6–1,0 и VС 0,58–1,09 , нитрид титана TiN 0,45–1,00 .
б) Соединения сохраняют свою кристаллическую решетку при значительных колебаниях количественного состава, то есть имеют широкую область гомогенности. Так, TiC 0,6–1,0 , как следует из формулы, сохраняет решетку карбида титана при недостатке в ней до 40 % атомов углерода.
в) Природа связи в таких соединениях определяется степенью заполнения d-орбиталей металла. Электроны внедренного неметалла заселяют вакантные d-орбитали, что приводит к усилению ковалентности связей. Именно поэтому доля металлической связи в соединениях начальных элементов d-рядов (IV–V групп) понижена.
Наличие ковалентной связи в них подтверждается большими положительными энтальпиями образования соединений, более высокими твердостью и температурой плавления, меньшей электропроводностью по сравнению с образующими их металлами.
Медь - элемент одиннадцатой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 29. Обозначается символом Cu (лат. Cuprum). Простое вещество медь (CAS-номер: 7440-50-8) - этопластичный переходный металл золотисто-розового цвета (розового цвета при отсутствии оксидной плёнки). C давних поршироко применяется человеком.
ОПРЕДЕЛЕНИЕ
Калий - первый элемент четвертого периода. Он расположен в I группе главной (А) подгруппе Периодической таблицы.
Относится к элементам s — семейства. Металл. Элементы-металлы, входящие в эту группу, носят общее название щелочных. Обозначение - K. Порядковый номер - 19. Относительная атомная масса - 39,102 а.е.м.
Электронное строение атома калия
Атом калия состоит из положительно заряженного ядра (+19), внутри которого есть 19 протонов и 20 нейтронов, а вокруг, по 4-м орбитам движутся 19 электронов.
Рис.1. Схематическое строение атома калия.
Распределение электронов по орбиталям выглядит следующим образом:
1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 .
Внешний энергетический уровень атома калия содержит 1 электрон, который является валентным. Степень окисления калия равна +1. Энергетическая диаграмма основного состояния принимает следующий вид:
Возбужденного состояния, несмотря на наличие вакантных 3p — и 3d -орбиталей нет.
Примеры решения задач
ПРИМЕР 1
| Задание | Атом элемента имеет следующую электронную конфигурацию 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 3 . Укажите: а) заряд ядра; б) число завершенных энергетических уровней в электронной оболочке этого атома; в) максимально возможную степень окисления; г) валентность атома в соединении с водородом. |
| Решение | Для того, чтобы ответить на поставленные вопросы, сначала нужно определить общее число электронов в атоме химического элемента. Это можно сделать, сложив все электроны, имеющиеся в атоме, не учитывая их распределения по энергетическим уровням:
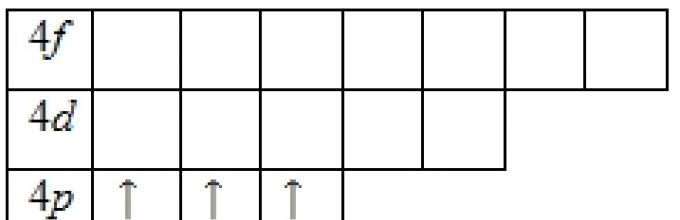
2+2+6+2+6+10+2+3 = 33. Это мышьяк (As). Теперь ответим на вопросы: а) заряд ядра равен +33; б) атом имеет четыре уровня, из которых завершенными являются три; в) запишем энергетическую диаграмму для валентных электронов атома мышьяка в основном состоянии. Мышьяк способен переходит в возбужденное состояние: электроны s -подуровня распариваются и один из них переходит на вакантную d -орбиталь. Пять неспаренных электронов свидетельствуют о том, что максимально возможная степень окисления мышьяка равна +5; г) Валентность мышьяка в соединении с водородом равна III (AsH 3). |
В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете … Википедия
Период строка периодической системы химических элементов, последовательность атомов по возрастанию заряда ядра и заполнению электронами внешней электронной оболочки. Периодическая система имеет семь периодов. Первый период, содержащий 2 элемента … Википедия
104 Лоуренсий ← Резерфордий → Дубний … Википедия
Д. И. Менделеева, естественная классификация химических элементов, являющаяся табличным (или др. графическим) выражением периодического закона Менделеева (См. Периодический закон Менделеева). П. с. э. разработана Д. И. Менделеевым в 1869… … Большая советская энциклопедия
Менделеев Дмитрий Иванович - (Dmitry Ivanovich Mendeleyev) Биография Менделеева, научная деятельность Менделеева Информаци о биографии Менделеева, научная деятельность Менделеева Содержание Содержание 1. Биография 2. Член русского народа 3. Научная деятельность Периодическая … Энциклопедия инвестора
Периодическая система химических элементов (таблица Менделеева) классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона,… … Википедия
Периодическая система химических элементов (таблица Менделеева) классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона,… … Википедия
Периодическая система химических элементов (таблица Менделеева) классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона,… … Википедия
Химических элементов (таблица Менделеева) классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским… … Википедия
Понятие переходный элемент обычно используется для обозначения любого элемента с валентными d- или f-электронами. Эти элементы занимают в периодической таблице переходное положение между электроположительными s-элементами и электроотрицательными p-элементами.
d-Элементы принято называть главными переходными элементами. Их атомы характеризуются внутренней застройкой d-подоболочек. Дело в том, что s-орбиталь их внешней оболочки обычно заполнена уже до того, как начинается заполнение d-орбиталей в предшествующей электронной оболочке. Это означает, что каждый новый электрон, добавляемый в электронную оболочку очередного d-элемента, в соответствии с принципом заполнения, попадает не на внешнюю оболочку, а на предшествующую ей внутреннюю подоболочку. Химические свойства этих элементов определяются участием в реакциях электронов обеих указанных оболочек.

d-Элементы образуют три переходных ряда - в 4-м, 5-м и 6-м периодах соответственно. Первый переходный ряд включает 10 элементов, от скандия до цинка. Он характеризуется внутренней застройкой 3d-орбиталей. Орбиталь 4s заполняется раньше, чем орбиталь 3d, потому что имеет меньшую энергию (правило Клечковского).
Следует, однако, отметить существование двух аномалий. Хром и медь имеют на своих 4s-орбиталях всего по одному электрону. Дело в том, что полузаполненные или полностью заполненные подоболочки обладают большей устойчивостью, чем частично заполненные подоболочки.
В атоме хрома на каждой из пяти 3d-орбиталей, образующих 3d-подоболочку, имеется по одному электрону. Такая подоболочка является полузаполненной. В атоме меди на каждой из пяти 3d-орбиталей находится по паре электронов. Аналогичная аномалия наблюдается у серебра.
Все d-элементы являются металлами.
Электронные конфигурации элементов четвертого периода от скандия до цинка:


Хром
Хром находится в 4-м периоде, в VI группе, в побочной подгруппе. Это металл средней активности. В своих соединениях хром проявляет степени окисления +2, +3 и +6. CrO - типичный основный оксид, Cr 2 O 3 - амфотерный оксид, CrO 3 - типичный кислотный оксид со свойствами сильного окислителя, т. е. рост степени окисления сопровождается усилением кислотных свойств.

Железо
Железо находится в 4-м периоде, в VIII группе, в побочной подгруппе. Железо - металл средней активности, в своих соединениях проявляет наиболее характерные степени окисления +2 и +3. Известны также соединения железа, в которых оно проявляет степень окисления +6, которые являются сильными окислителями. FeO проявляет основные, а Fe 2 O 3 - амфотерные с преобладанием основных свойств.

Медь
Медь находится в 4-м периоде, в I группе, в побочной подгруппе. Ее наиболее устойчивые степени окисления +2 и +1. В ряду напряжений металлов медь находится после водорода, ее химическая активность не очень велика. Оксиды меди: Cu2O CuO. Последний и гидроксид меди Cu(OH)2 проявляют амфотерные свойства с преобладанием основных.
Цинк
Цинк находится в 4-м периоде, во II-группе, в побочной подгруппе. Цинк относится к металлам средней активности, в своих соединениях проявляет единственную степень окисления +2. Оксид и гидроксид цинка являются амфотерными.