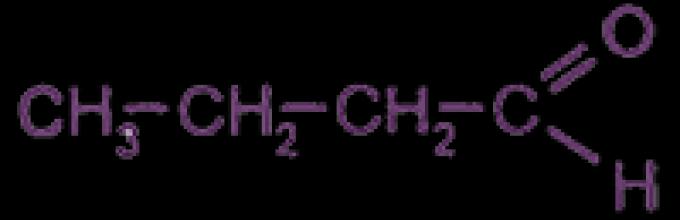(для простейшего альдегида R=H)
Классификация альдегидов
По строению углеводородного радикала:
Предельные; например:

Непредельные; например:

Ароматические; например:

Алициклические; например:

Общая формула предельных альдегидов

Гомологический ряд, изомерия, номенклатура

Альдегиды изомерны другому классу соединений - кетонам

например:

Альдегиды и кетоны содержат карбонильную группу ˃C=O, поэтому называются карбонильными соединениями.
Электронное строение молекул альдегидов
Атом углерода альдегидной группы находится в состоянии sp 2 -гибридизации, поэтому все σ-связи в этой группе располагаются в одной плоскости. Облака р-электронов, образующих π-связь, перпендикулярны этой плоскости и легко смещаются к более электроотрицательному атому кислорода. Поэтому двойная связь C=O (в отличие от двойной связи C=C в алкенах) сильно поляризована.
Физические свойства

Химические свойства
Альдегиды - реакционноспособные соединения, вступающие в многочисленные реакции. Наиболее характерны для альдегидов:
а) реакции присоединения по карбонильной группе; реагенты типа НХ присоединяются следующим образом:

б) реакции окисления связи C-H альдегидной группы, в результате которых образуются карбоновые кислоты:
I. Реакции присоединения
1. Гидрирование (образуются первичные спирты

2. Присоединение спиртов (образуются полуацетали и ацетали)

В избытке спирта в присутствии HCl полуацетали превращаются в ацетали:

II. Реакции окисления
1. Реакция «серебряного зеркала»

Упрощённо:

Эта реакция является качественной реакцией на альдегидную группу (на стенках реакционного сосуда образуется зеркальный налет металлического серебра).
2. Реакция с гидроксидом меди (II)

Эта реакция также является качественной реакцией на альдегидную групп у (выпадает красный осадок Сu 2 O).
Формальдегид окисляется различными O-содержащими окислителями сначала до муравьиной кислоты и далее - до Н 2 СO 3 (СO 2 + Н 2 O):

III. Реакции ди-, три- и полимеризации
1. Альдольная конденсация

2. Тримеризация ацетальдегида

3. Полимеризация формальдегида
При длительном хранении формалина (40%-ный водный раствор формальдегида) в нем происходит полимеризация с образованием белого осадка параформа:

IV. Реакция поликонденсации формальдегида с фенолом

Лекция № 11
АЛЬДЕГИДЫ И КЕТОНЫ
План
1. Методы получения.
2. Химические свойства.
2.1. Реакции нуклеофильного
присоединения.
2.2. Реакции по a -углеродному атому.
2.3.
Лекция № 11
АЛЬДЕГИДЫ И КЕТОНЫ
План
1. Методы получения.
2. Химические свойства.
2.1. Реакции нуклеофильного
присоединения.
2.2. Реакции по a -углеродному атому.
2.3. Реакции окисления и восстановления.
Альдегиды и кетоны содержат карбонильную группу
С=О. Общая формула:
1. Методы получения.

2. Химические
свойства.
Альдегиды и кетоны – один из наиболее реакционноспособных классов
органических соединений. Их химические свойства определяются присутствием
карбонильной группы. Вследствие большого различия в электроотрицательностях
углерода и кислорода и высокой поляризуемости p
-связи связь С=О обладает значительной полярностью
(m
С=О
=2,5-2,8 D). Атом углерода карбонильной
группы несет эффективный положительный заряд и является объектом для атаки
нуклеофилов. Основной тип реакций альдегидов и кетонов – реакции
нуклеофильного присоединения Ad
N . Кроме того, карбонильная группа оказывает влияние на
реакционную способность связи С-Н в
a
-положении, повышая ее кислотность.
Таким образом, молекулы альдегидов и кетонов
содержат два основных реакционных центра – связь С=О и связь С-Н в
a
-положении:

2.1. Реакции нуклеофильного
присоединения.
Альдегиды и кетоны легко присоединяют нуклеофильные реагенты по С=О связи.
Процесс начинается с атаки нуклеофила по карбонильному атому углерода. Затем
образующийся на первой стадии тетраэдрический интермедиат присоединяет протон и
дает продукт присоединения:

Активность карбонильных соединений в
Ad
N –реакциях зависит от величины
эффективного положительного заряда на карбонильном атоме углерода и объема
заместителей у карбонильной группы. Электронодонорные и объемистые заместители
затрудняют реакцию, электроноакцепторные заместители повышают реакционную
способность карбонильного соединения. Поэтому альдегиды в
Ad
N –реакциях активнее, чем
кетоны.
Активность карбонильных соединений повышается в
присутствии кислотных катализаторов, которые увеличивают положительный заряд на
карбонильном атоме углерода:

Альдегиды и кетоны присоединяют воду, спирты,
тиолы, синильную кислоту, гидросульфит натрия, соединения типа
NH
2 X. Все реакции присоединения
идут быстро, в мягких условиях, однако образующиеся продукты, как правило,
термодинамически не устойчивы. Поэтому реакции протекают обратимо, и содержание
продуктов присоединения в равновесной смеси может быть низким.
Присоединение воды.
Альдегиды и кетоны присоединяют воду с
образованием гидратов. Реакция протекает обратимо. Образующиеся гидраты
термодинамически не стабильны. Равновесие смещено в сторону продуктов
присоединения только в случае активных карбонильных соединений.

Продукт гидратации трихлоруксусного альдегида
хлоральгидрат – устойчивое кристаллическое соединение, которое используется в
медицине как успокаивающее и снотворное средство.
Присоединение спиртов и
тиолов.
Альдегиды присоединяют спирты с образованием полуацеталей
. При избытке спирта и в присутствии кислотного катализатора
реакция идет дальше – до образования ацеталей

Реакция образования полуацеталя протекает как
нуклеофильное присоединение и ускоряется в присутствии кислот или
оснований.

Процесс образования ацеталя идет как
нуклеофильное замещение ОН группы в полуацетале и возможен только в условиях
кислотного катализа, когда группа ОН превращается в хорошую уходящую группу
(H
2 O).

Образование ацеталей – обратимый процесс. В
кислой среде полуацетали и ацетали легко гидролизуются. В щелочной среде
гидролиз не идет. Реакции образования и гидролиза ацеталей играют важную роль в
химии углеводов.
Кетоны в аналогичных условиях кеталей не
дают.
Тиолы как более сильные нуклеофилы, чем спирты,
образуют продукты присоединения и с альдегидами, и с кетонами.
Присоединение синильной
кислоты
Синильная кислота присоединяется к карбонильным соединением в условиях
основного катализа с образованием циангидринов.

Реакция имеет препаративное значение и
используется в синтезе
a
-гидрокси- и
a
-аминокислот (см. лек. № 14). Плоды некоторых растений
(например, горький миндаль) содержат циангидрины. Выделяющаяся при их
расщеплении синильная кислота оказывает отравляющее действие
.
Присоединение бисульфита
натрия.
Альдегиды и метилкетоны присоединяют бисульфит натрия NaHSO 3 c образованием бисульфитных производных.

Бисульфитные производные карбонильных соединений
– кристаллические вещества, не растворимые в избытке раствора бисульфита натрия.
Реакция используется выделения карбонильных соединений из смесей. Карбонильное
соединение может быть легко регенерировано обработкой бисульфитного производного
кислотой
или щелочью.
Взаимодействие с соединениями общей
формулы NH
2 X.
Реакции протекают по общей схеме как процесс
присоединения-отщепления. Образующийся на первой стадии продукт присоединения не
устойчив и легко отщепляет воду.

По приведенной схеме с карбонильными
соединениями реагируют аммиак, первичные амины, гидразин, замещенные гидразины,
гидроксиламин.

Образующиеся производные представляют собой
кристаллические вещества, которые используют для выделения и идентификации
карбонильных соединений.
Имины (основания Шиффа) являются промежуточными
продуктами во многих ферментативных процессах (трансаминирование под действием
кофермента пиридоксальфосфата; восстановительное аминирование кетокислот при
участии кофермента НАД
Н). При каталитическом гидрировании иминов образуются
амины. Процесс используется для синтеза аминов из альдегидов и кетонов и
называется восстановительным аминированием.
Восстановительное аминирование протекает in vivo
в ходе синтеза аминокислот (см. лек. № 16)
2.2. Реакции по a -углеродному атому.
Кето-енольная таутомерия.
Водород в
a
-положении к карбонильной группе обладает кислотными
свойствами, так как образующийся при его отщеплении анион стабилизируется за
счет резонанса.

Результатом протонной подвижности атома водорода
в
a
-положении
является способность карбонильных соединений к образованию енольных форм за счет
миграции протона из
a
-положения к атому кислорода карбонильной группы.

Кетон и енол являются таутомерами
.
Таутомеры – это изомеры, способные быстро и обратимо превращаться друг в друга
за счет миграции какой-либо группы (в данном случае – протона). Равновесие между
кетоном и енолом называют кето-енольной таутомерией.
Процесс енолизации катализируется кислотами и
основаниями. Енолизация под действием основания может быть представлена
следующей схемой:
Большинство карбонильных соединений существуют
преимущественно в кетонной форме. Содержание енольной формы возрастает с
увеличением кислотности карбонильного соединения, а также в случае
дополнительной стабилизации енольной формы за счет водородной связи или за счет
сопряжения.
Таблица 8. Содержание енольных форм и
кислотность карбонильных соединений
Например, в 1,3-дикарбонильных соединениях
подвижность протонов метиленовой группы резко увеличивается за счет
электроноакцепторного влияния двух карбонильных групп. Кроме того, енольная
форма стабилизируется за счет наличия в ней системы сопряженных
p
-связей и внутримолекулярной
водородной связи.

Если соединение в енольной форме представляет
собой сопряженную систему с высокой энергией стабилизации, то енольная форма
преобладает. Например, фенол существует только в енольной форме.
Енолизация и образование енолят-анионов являются
первыми стадиями реакций карбонильных соединений, протекающих по
a
-углеродному атому. Важнейшими
из них являются галогенирование
и альдольно-кротоновая
конденсация
.
Галогенирование.
Альдегиды и кетоны легко вступают в реакцию с галогенами (Cl 2 ,
Br 2 , I 2 ) с образованием
исключительно
a
-галогенпроизводных.

Реакция катализируется кислотами или
основаниями. Скорость реакции не зависит от концентрации и природы галогена.
Процесс протекает через образование енольной формы (медленная стадия), которая
затем реагирует с галогеном (быстрая стадия). Таким образом, галоген не
участвует в скорость
—определяющей стадии
процесса.

Если карбонильное соединение содержит несколько
a
-водородных
атомов, то замещение каждого последующего происходит быстрее, чем предыдущего,
вследствие увеличения их кислотности под действием электроноакцепторного влияния
галогена. В щелочной среде ацетальдегид и метилкетоны дают
тригалогенпроизводные, которые затем расщеплятся под действием избытка щелочи с
образованием тригалогенметанов (галоформная реакция)
.
Расщепление трииодацетона протекает как реакция
нуклеофильного замещения. группы CI
3 — гидроксид-анионом, подобно S
N -реакциям в карбоксильной группе (см. лек. №12).
Иодоформ выпадает из реакционной смеси в виде
бледно-желтого кристаллического осадка с характерным запахом. Иодоформную
реакцию используют в аналитических целях для обнаружения соединений типа
СH
3 -CO-R, в том числе в
клинических лабораториях для диагностики сахарного диабета.
Реакции конденсации.
В присутствии каталитических количеств кислот
или щелочей карбонильные соединения, содержащие
a
-водородные атомы,
претерпевают конденсацию с образованием
b
-гидроксикарбонильных соединений.

В образовании связи С-С участвуют карбонильный
атом углерода одной молекулы (карбонильной компоненты
) и
a
-углеродный атом другой
молекулы (метиленовой компоненты
). Эта реакция носит название альдольной конденсации
(по названию продукта конденсации ацетальдегида –
альдоля).
При нагревании реакционной смеси продукт легко
дегидратируется с образованием
a
,b
-непредельного карбонильного
соединения.

Такой тип конденсации носит название кротоновой
(по названию продукта конденсации ацетальдегида – кротонового
альдегида).
Рассмотрим механизм альдольной конденсации в
щелочной среде. На первой стадии гидроксид-анион отрывает протон из
a
-положения карбонильного
соединения с образованием енолят-аниона. Затем енолят анион как нуклеофил
атакует карбонильный атом углерода другой молекулы карбонильного соединения.
Образующийся тетраэдрический интермедиат (алкоксид-анион) является сильным
основанием и отрывает далее протон от молекулы воды.

При альдольной конденсации двух различных
карбонильных соединений (перекрестная альдольная конденсация) возможно
образование 4-х разных продуктов. Однако этого можно избежать, если одно из
карбонильных соединений не содержит
a
-водородных атомов (например, ароматические альдегиды
или формальдегид) и не может выступать в качестве метиленовой компоненты.

В качестве метиленовой компоненты в реакциях
конденсации могут выступать не только карбонильные соединения, но и другие
С-Н-кислоты. Реакции конденсации имеют препаративное значение, так как позволяют
наращивать цепь углеродных атомов. По типу альдольной конденсации и
ретроальдольного распада (обратный процесс) протекают многие биохимические
процессы: гликолиз, синтез лимонной кислоты в цикле Кребса, синтез нейраминовой
кислоты.
2.3. Реакции окисления и
восстановления
Восстановление
Карбонильные соединения восстанавливаются до
спиртов в результате каталитического гидрирования или под действием
восстановителей, которые являются донорами гидрид-анионов.

[H]: H 2 /кат., кат. – Ni, Pt,
Pd;
LiAlH 4 ; NaBH 4 .
Восстановление карбонильных соединений
комплексными гидридами металлов включает нуклеофильную атаку карбонильной группы
гидрид-анионом. При последующем гидролизе образуется спирт.
Аналогично происходит восстановление
карбонильной группы in vivo под действием кофермента НАД
Н, который является
донором гидрид-иона (см. лек. №19).
Окисление
Альдегиды окисляются очень легко практически
любыми окислителями, даже такими слабыми, как кислород воздуха и соединения
серебра (I) и меди
(II).
Две последние реакции используются как
качественные на альдегидную группу.
В присутствии щелочей альдегиды, не содержащие
a
-водородных атомов
диспропорционируют с образованием спирта и кислоты (реакция Канницаро).
2HCHO + NaOH ® HCOONa + CH 3 OH
Это является причиной того, что водный раствор
формальдегида (формалин) при длительном хранении приобретает кислую
реакцию.
Кетоны устойчивы к действию окислителей в
нейтральной среде. В кислой и щелочной средах под действием сильных
окислителей
(KMnO 4 ) они
окисляются с разрывом связи С-С. Расщепление углеродного скелета происходит по
двойной углерод-углеродной связи енольных форм карбонильного соединения, подобно
окислению двойных связей в алкенах. При этом образуется смесь продуктов,
содержащая карбоновые кислоты или карбоновые кислоты и кетоны.
Органическая химия - наука весьма сложная, но интересная. Ведь соединения одних и тех же элементов, в разном количестве и последовательности способствует образованию различных по Давайте рассмотрим соединения карбонильной группы под названием "кетоны" (химические свойства, физические особенности, методы их синтеза). А также сравним их с другими веществами этого же рода - альдегидами.
Кетоны
Это слово является общим названием для целого класса веществ органической природы, в молекулах которых карбонильная группа (С=О) связана с двумя углеродными радикалами.
По своему строению кетоны близки к альдегидам и карбоновым кислотам. Однако в них присутствуют сразу два атома С (карбон или углерод), соединенных с С=О.
Формула
Общая формула веществ этого класса выглядит следующим образом: R 1 -CO-R 2 .
Чтобы она была более понятна, как правило, ее записывают так.

В ней С=О - это карбонильная группа. А R 1 и R 2 - это углеродные радикалы. На их месте могут быть различные соединения, но в их составе обязательно должен быть углерод.
Альдегиды и кетоны
Физические и химические свойства этих групп веществ довольно схожи между собой. По этой причине их часто рассматривают вместе.

Дело в том, что альдегиды тоже содержат в своих молекулах карбонильную группу. У них с кетонами даже формулы весьма схожи. Однако если у рассматриваемых веществ С=О присоединяется к 2 радикалам, то у альдегидов он только один, вместо второго - атом гидрогена: R-CO-H.
В качестве примера можно привести формулу вещества этого класса - формальдегида, более известного всем, как формалин.

Исходя из формулы CH 2 O, видно, что его карбонильная группа связана не с одним, а сразу с двумя атомами Н.
Физические свойства
Прежде чем разобраться с химическими свойствами альдегидов и кетонов, стоит рассмотреть их физические особенности.

- Кетоны - это легкоплавкие или жидкости с летучестью. Низшие представители этого класса отлично растворяются в Н 2 О и неплохо взаимодействуют с происхождения.
Отдельные представители (например, СН 3 СОСН 3) замечательно растворяются в воде, причем абсолютно в любых пропорциях.
В отличие от спиртов и карбоновых кислот, кетоны обладают большей летучестью, при одинаковой молекулярной массе. Этому способствует невозможность этих соединений создавать связи с Н, как это могут H-CO-R. - Разные виды альдегидов могут пребывать в различных агрегатных состояниях. Так высшие R-CO-H - это нерастворимые твердые вещества. Низшие - это жидкости, часть из которых отлично смешивается с Н 2 О, однако отдельные из них только растворимы в воде, но не более.
Простейший из веществ данного вида - муравьиный альдегид - это газ, которому свойственен острый запах. Данное вещество отлично растворимо в Н 2 О.
Наиболее известные кетоны
Существует немало веществ R 1 -CO-R 2 , однако известных из них не так уж много. В первую очередь это диметилкетон, который мы все знаем как ацетон.

Также его коллега-растворитель - бутанон или как его правильно называть - метилэтилкетон.
Среди других кетонов, химические свойства которых активно используются в промышленности - ацетофенон (метилфенилкетон). В отличие от ацетона и бутанона, его запах довольно приятен, из-за чего он используется в парфюмерии.
К примеру, циклогексанон относится к типичным представителям R 1 -CO-R 2 , и чаще всего используется в производстве растворителей.
Нельзя не упомянуть о дикетонах. Такое название носят R 1 -CO-R 2 , у которых не одна, а две карбонильные группы в составе. Таким образом, их формула выглядит: R 1 -CO-CO-R 2 . Одним из наиболее простых, но широко используемых в пищевой промышленности представителей дикетонов является диацетил (2,3-бутандион).
Перечисленные вещества - это всего лишь небольшой список синтезированных учеными кетонов (химические свойства рассмотрены ниже). На самом деле их больше, но не всем найдено применение. Тем более стоит учитывать то, что многие из них токсичны.
Химические свойства кетонов
- Кетоны способны присоединять к себе Н (реакция гидрирования). Однако для произведения этой реакции необходимо присутствие катализаторов в виде атомов металлов никеля, кобальта, купрума, платины, палладия и других. В результате реакции R 1 -CO-R 2 эволюционируют до вторичных спиртов.
Также при взаимодействии с гидрогеном в присутствии щелочных металлов или амальгамы Mg из кетонов получаются гликоли. - Кетоны, обладающие хотя бы одним альфа-гидрогенным атомом, как правило, попадают под воздействие таутомеризации кето-енольной. Она катализируется не только с помощью кислот, но и основ. Обычно кето-форма являет собою более стабильное явление, нежели енольная. Данное равновесие дает возможность синтезировать кетоны путем гидратации алкинов. Относительная стабилизация енольной кето-формы сопряжением приводит к довольно сильной кислотности R 1 -CO-R 2 (если сравнивать их с алканами).
- Данные вещества могут вступать в реакции с аммиаком. Однако они протекают весьма медленно.
- Кетоны взаимодействуют с В результате возникают α-оксинитрилы, омыление которых способствует появлению α-гидроксикислот.
- Вступление в реакцию с алкилмагнийгалогенидами приводит к формированию вторичных спиртов.
- Присоединение к NaHSO 3 способствует возникновению гидросульфитных (бисульфитных) производных. Стоит помнить, что в реакцию в жирном ряду вступать способны лишь метилкетоны.
Помимо кетонов, подобно взаимодействовать с гидросульфитом натрия могут и альдегиды.
При нагревании с раствором NaHCO 3 (пищевая сода) или минеральной кислотой, производные от NaHSO 3 могут разлагаться, сопровождаясь выделением свободного кетона. - В процессе реакции R 1 -CO-R 2 с NH 2 OH (гидроксиламин) образуются кетоксимы и как побочный продукт - Н 2 О.
- При реакциях с участием гидразина образуются гидразоны (соотношение взятых веществ - 1:1) или азины (1:2).
Если полученный из-за реакции продукт (гидразон) под действием температуры прореагирует с едким калием, выделиться N и предельные углеводороды. Данный процесс именуется реакцией Кижнера. - Как уже было сказано выше, альдегиды и кетоны химические свойства и получения процесс имеют похожие. При этом ацетали R 1 -CO-R 2 образуются более сложные, нежели ацетали R-CO-H. Они появляются в результате действия на кетоны эфиров ортомуравьиной и ортокремниевой кислот.
- В условиях с большей концентрацией щелочей (к примеру, при нагревании с концентрированной H₂SO₄) R 1 -CO-R 2 подвергаются межмолекулярной дегидратации с формированием непредельных кетонов.
- Если в реакции с R 1 -CO-R 2 присутствуют щелочи, кетоны подвергаются альдольной конденсации. Вследствие этого образуются β-кетоспирты, способные с легкостью лишаться молекулы Н 2 О.
- Довольно показательно проявляют себя химические свойства кетонов на примере ацетона, прореагировавшего с окисью мезитила. В таком случае образуется новое вещество под названием «форон».
- Также к химическим свойствам рассматриваемого органического вещества можно отнести реакцию Лейкарта-Валлаха, которая способствует восстановлению кетонов.
Из чего получают R1-CO-R2
Ознакомившись со свойства рассматриваемых веществ, стоит узнать наиболее распространенные способы их синтеза.
- Одной из наиболее известных реакций для получения кетонов является алкилирование и ацилирование ароматических соединений в присутствии катализаторов кислотного характера (AlCl 3 , FeCI 3 , минеральных кислот, окислов, катионообменных смол и т.п.). Данный способ известен под названием реакция Фриделя-Крафтса.
- Кетоны синтезируются при помощи гидролиза кетиминов и виц-диолов. В случае с последними необходимо присутствие как катализаторов.
- Также для получения кетонов применяется гидратация гомологов ацетилена или как ее называют - реакция Кучерова.
- Реакции Губена-Геша.
- Циклизация Ружички пригодна для синтеза циклокетонов.
- Также данные вещества добывают из третичных пероксоэфиров при помощи перегруппировки Криге.
- Существует несколько способов синтеза кетонов во время реакций окисления вторичных спиртов. В зависимости от действующего соединения выделяются 4 реакции: Сверна, Корнблюма, Кори-Кима и Парика-Деринга.
Сфера применения
Разобравшись с химическими свойствами и получением кетонов, стоит узнать, где же используются данные вещества.

Как уже упоминалось выше, большинство из них используется в химической промышленности в качестве растворителей для лаков и эмалей, а также при производстве полимеров.
Помимо этого, некоторые R 1 -CO-R 2 неплохо зарекомендовали себя как ароматизаторы. В таком качестве кетоны (бензофенон, ацетофенон и другие) применяются в парфюмерии и кулинарии.
Также ацетофенон используется как компонент для изготовления снотворного.

Бензофенон, благодаря способности поглощать вредное излучение, - является частым ингредиентом антизагарной косметики и одновременно консервантом.
Влияния R1-CO-R2 на организм
Узнав, что за соединения называются кетонами (химические свойства, применение, синтез и другие данные о них), стоит ознакомиться с биологическими особенностями данных веществ. Иными словами, узнать, как же они действуют на живые организмы.
Несмотря на довольно частое использования R 1 -CO-R 2 в промышленности, стоит всегда помнить, что такие соединения очень токсичны. Многие из них обладают канцерогенными и мутагенными свойствами.
Особые представители способны вызывать раздражение на слизистых оболочках, вплоть до ожогов. Алициклические R 1 -CO-R 2 могут воздействовать на организм, как наркотики.
Однако не все вещества такого рода вредны. Дело в том, что некоторые из них принимают активное участие в метаболизме биологических организмов.
Также кетоны - это своеобразные маркеры нарушений углеродного обмена и дефицита инсулина. При анализе мочи и крови присутствие R 1 -CO-R 2 свидетельствует о различных расстройствах метаболизма, в том числе гипергликемии и кетоацидозе.
Альдегидами называют соединения, молекулы которых содержат карбонильную группу, соединенную с атомом водорода, т.е. общая формула альдегидов может быть записана как
где R – углеводородный радикал, который может быть разной степени насыщенности, например, предельный или ароматический.
Группу –СНО называют альдегидной.
Кетоны – органические соединения, в молекулах которых содержится карбонильная группа, соединенная с двумя углеводородными радикалами. Общую формулу кетонов можно записать как:
где R и R’ – углеводородные радикалы, например, предельные (алкилы) или ароматические.
Гидрирование альдегидов и кетонов
Альдегиды и кетоны могут быть восстановлены водородом в присутствии катализаторов и нагревании до первичных и вторичных спиртов соответственно:
Окисление альдегидов
Альдегиды легко могут быть окислены даже такими мягкими окислителями, как гидроксид меди и аммиачный раствор оксида серебра.
При нагревании гидроксида меди с альдегидом происходит исчезновение изначального голубого окрашивания реакционной смеси, при этом образуется кирпично-красный осадок оксида одновалентной меди:
В реакции с аммиачным раствором оксида серебра вместо самой карбоновой кислоты образуется ее аммонийная соль, поскольку находящийся в растворе аммиак реагирует с кислотами:
Кетоны в реакцию с гидроксидом меди (II) и аммиачным раствором оксида серебра не вступают. По этой причине эти реакции являются качественными на альдегиды. Так реакция с аммиачным раствором оксида серебра при правильной методике ее проведения приводит к образованию на внутренней поверхности реакционного сосуда характерного серебряного зеркала.
Очевидно, что если мягкие окислители могут окислить альдегиды, то само собой это могут сделать и более сильные окислители, например, перманганат калия или дихромат калия. При использовании данных окислителей в присутствии кислот образуются карбоновые кислоты:
Химические свойства карбоновых кислот
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Карбоксильная групп а:
Как можно видеть, карбоксильная группа состоит из карбонильной группы –С(О)- , соединенной с гидроксильной группой –ОН.
В связи с тем, что к гидроксильной группе непосредственно прикреплена карбонильная, обладающая отрицательным индуктивным эффектом связь О-Н является более полярной, чем в спиртах и фенолах. По этой причине карбоновые кислоты обладают заметно более выраженными, чем спирты и фенолы, кислотными свойствами. В водных растворах они проявляют свойства слабых кислот, т.е. обратимо диссоциируют на катионы водорода (Н+) и анионы кислотных остатков:
Реакции образования солей
С образованием солей карбоновые кислоты реагируют с:
1) металлами до водорода в ряду активности:
2) аммиаком
3) основными и амфотерными оксидами:
4) основными и амфотерными гидроксидами металлов:
5) солями более слабых кислот – карбонатами и гидрокарбонатами, сульфидами и гидросульфидами, солями высших (с большим числом атомов углерода в молекуле) кислот:
Систематические и тривиальные названия некоторых кислот и их солей представлены в следующей таблице:
| Формула кислоты | Название кислоты тривиальное/систематическое | Название соли тривиальное/систематическое |
| HCOOH | муравьиная/ метановая | формиат/ метаноат |
| CH 3 COOH | уксусная/ этановая | ацетат/ этаноат |
| CH 3 CH 2 COOH | пропионовая/ пропановая | пропионат/ пропаноат |
| CH 3 CH 2 CH 2 COOH | масляная/ бутановая | бутират/ бутаноат |
Следует помнить и обратное: сильные минеральные кислоты вытесняют карбоновые кислоты из их солей как более слабые:
Реакции с участием ОН группы
Карбоновые кислоты вступают в реакцию этерификации с одноатомными и многоатомными спиртами в присутствии сильных неорганических кислот, при этом образуются сложные эфиры:
Данного типа реакции относятся к обратимым, в связи с чем с целью смещения равновесия в сторону образования сложного эфира их следует осуществлять, отгоняя более летучий сложный эфир при нагревании.
Обратный реакции этерификации процесс называют гидролизом сложного эфира:
Необратимо данная реакция протекает в присутствии щелочей, поскольку образующаяся кислота реагирует с гидроксидом металла с образованием соли:
Реакции замещения атомов водорода в углеводородном заместителе
При проведении реакций карбоновых с хлором или бромом в присутствии красного фосфора при нагревании происходит замещение атомов водорода при α-атоме углерода на атомы галогена:
В случае большей пропорции галоген/кислота может произойти и более глубокое хлорирование:
Реакции разрушения карбоксильной группы (декарбоксилирование)
Особые химические свойства муравьиной кислоты
Молекула муравьиной кислоты, несмотря на свои малые размеры, содержит сразу две функциональные группы:
В связи с этим она проявляет не только свойства кислот, но также и свойства альдегидов:
При действии концентрированной серной кислоты муравьиная кислота разлагается на воду и угарный газ.
Альдегиды и кетоны – это производные углеводородов, в молекулах которых имеется карбонильная группа. Альдегиды по строению отличаются от кетонов положением карбонильной группы. О физических свойствах альдегидов и кетонов, а также об их классификации и номенклатуре говорим в этой статье.
Физические свойства
В отличие от спиртов и фенолов, для альдегидов и кетонов не характерно образование водородных связей, именно поэтому их температуры кипения и плавления значительно ниже. Так, формальдегид – газ, уксусный альдегид кипит при температуре 20,8 градусов, тогда как метанол кипит при температуре 64,7 градусов. Аналогично фенол – кристаллическое вещество, а бензальдегид – жидкость.
Формальдегид – бесцветный газ с резким запахом. Остальные члены ряда альдегидов – жидкости, а высшие альдегиды являются твердыми веществами. Низшие члены ряда (формальдегид, ацетальдегид) – растворимы в воде, имеют резкий запах. Высшие альдегиды хорошо растворимы в большинстве органических растворителях (спирты, эфиры), у альдегидов С 3 -С 8 весьма неприятный запах, а высшие альдегиды применяются в парфюмерии из-за цветочных запахов.

Рис. 1. Таблица классификация альдегидов и кетонов.
Общая формула альдегидов и кетонов выглядит следующим образом:
- формула альдегидов – R-COH
- формула кетонов – R-CO-R
Классификация и номенклатура
Альдегиды и кетоны отличаются по типу углеродной цепи, в которой находится карбонильная группа. Рассмотрим соединения жирного ряда и ароматические:
- ациклические, предельные . Первым членом гомологического ряда альдегидов является муравьиный альдегид (формальдегид, метаналь) – CH 2 =O.
Муравьиный альдегид применяется как антисептик. С его помощью осуществляется дезинфекция помещений, протравливание семян.
Второй член альдегидного ряда – уксусный альдегид (ацетальдегид, этаналь). Он применяется как промежуточный продукт при синтезе уксусной кислоты и этилового спирта из ацетилена.

Рис. 2. Формула уксусный альдегид.
- непредельные . Необходимо упомянуть такой непредельный альдегид, как акролеин (пропеналь). Этот альдегид образуется при термическом разложении глицерина и жиров, составной частью которых является глицерин.
- ароматические . Первым членом гомологического ряда ароматических альдегидов является бензольный альдегид (бензальдегид). Также можно отметить такой альдегид растительного происхождения, как ванилин (3-метокси-4-гидроксибензальдегид).

Рис. 3. Формула ванилин.
Кетоны могут быть чисто ароматические и жиро-ароматические. Чисто ароматическим является, например, дифенилкетон (бензофенон). Жирно-ароматическим является, например, метил-фенилкетон (ацетофенон)
Что мы узнали?
На уроках химии 10 класса важнейшей задачей является изучение альдегидов и кетонов. В альдегидах атом углерода карбонильной группы является первичным, а в кетонах вторичным. Поэтому в альдегидах карбонильная группа всегда связана с атомом водорода. Альдегидная группа обладает большей химической активностью, чем кетонная, особенно в реакциях окисления.
Тест по теме
Оценка доклада
Средняя оценка: 4.2 . Всего получено оценок: 166.